
【题目】一定温度下,在固定容积、体积为2L的密闭容器中充入1molN2和3molH2发生反应,当反应进行到10s末时达到平衡,此时容器中c(NH3)=0.15mol·L-1。下列有关判断不正确的是
A.反应达平衡时N2的转化率为7.5%
B.反应进行到10s末时,H2的平均反应速率是0.0225mol·(L·s)-1
C.该反应达到平衡时的标志是容器中气体密度不再改变
D.再往该容器中充入1molN2和3molH2,重新达到平衡时c(NH3)=0.30mol/L
【答案】B
【解析】
试题分析:发生反应:N2(g)+3H2(g) ![]() 2NH3(g)。A.平衡时容器中c(NH3)=0.15mol/L,则氮气的浓度变化量=0.15mol/L×
2NH3(g)。A.平衡时容器中c(NH3)=0.15mol/L,则氮气的浓度变化量=0.15mol/L×![]() =0.075mol/L,故氮气的转化率=
=0.075mol/L,故氮气的转化率=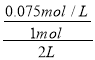 ×100%=15%,故A错误;B.10s末时达到平衡时容器中c(NH3)=0.15mol/L,故v(NH3)=
×100%=15%,故A错误;B.10s末时达到平衡时容器中c(NH3)=0.15mol/L,故v(NH3)=![]() =0.015mol/(L.s),v(H2)=
=0.015mol/(L.s),v(H2)=![]() v(NH3)=0.0225mol/(L.s),故B正确;C.容器内反应混合气体的密度始终不变,故容器中气体密度不改变不能说明平衡到达平衡,故C错误;D.再往该容器中充入1mol N2和3mol H2,等效为在原平衡基础上体积缩小一倍,若平衡不移动,平衡时氨气的浓度为0.3mol/L,体积缩小一倍,则压强增大一倍,平衡向正反应方向移动,故平衡时氨气的浓度大于0.3mol/L,故D错误;故选B。
v(NH3)=0.0225mol/(L.s),故B正确;C.容器内反应混合气体的密度始终不变,故容器中气体密度不改变不能说明平衡到达平衡,故C错误;D.再往该容器中充入1mol N2和3mol H2,等效为在原平衡基础上体积缩小一倍,若平衡不移动,平衡时氨气的浓度为0.3mol/L,体积缩小一倍,则压强增大一倍,平衡向正反应方向移动,故平衡时氨气的浓度大于0.3mol/L,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验 编号 | HA物质的量 浓度(mol/L) | NaOH物质的量 浓度(mol/L) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请回答:
(1)从①组情况分析,HA是__________(填“强酸”或“弱酸”)。
(2)②组情况表明,c__________(填“>”、“<”或“=”)0.2 mol/L。混合液中离子浓度c(A-)与c(Na+)的大小关系是__________。
(3)从③组实验结果分析,说明HA的电离程度__________(填“>”、“<”或“=”)NaA的水解程度,该混合溶液中离子浓度由大到小的顺序是__________________。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=________mol·L-1。写出该混合溶液中下列算式的精确结果(不能近似计算)。
c(Na+)-c(A-)=________mol·L-1;
c(OH-)-c(HA)=________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有Cl2的六个集气瓶甲,乙、丙、丁、戊、己中各注入下列液体中的一种,经过震荡, 现象如下所示,则中、乙、丙、丁、戊、己中注入的液体分别是
①AgNO3溶液②NaOH溶液③水④淀粉-KI溶液⑤FeCl2与KSCN混合液⑥NaBr溶液

A. ②①④⑥⑤③ B. ②⑥①③④⑤ C. ②⑥③④①⑤ D. ②①③④⑥⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于取代反应的是( )
①溴乙烷与氢氧化钠水溶液共热 ②溴乙烷与氢氧化钠的乙醇溶液共热
③甲烷与氯气 ④乙炔与氯化氢在一定条件下制氯乙烯
A.①② B.②④ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次递增的五种常见元素。A、B元素组成的气态化合物M的水溶液呈碱性,C元素是地壳中含量最多的元素,D的单质在C的单质中燃烧后的产物可以使品红溶液褪色,E是金属元素。
(1)写出A、C两种元素组成的化合物A2C2的电子式: ;
(2)A、B、C三种元素可组成一种强酸U,M在适当条件下被U吸收生成一种盐。该盐的水溶液的PH (填大于,小于或等于)7,原因是 ;(用离子方程式表示)
(3)若将E金属投入盐酸中,生成了浅绿色溶液N。则N的酸性溶液与A2C2反应的离子方程式为 ;
(4)R是B的氧化物,通常情况下呈红棕色。现有一试管R,欲使元素B全部转化为它的最高价氧化物对应的水化物,故进行如下实验操作:将盛有R的试管倒扣在水槽中, ;
(5)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式: ,放电时,溶液中的H+移向 (填正或负极)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铝制易拉罐收集满CO2,加入过量NaOH浓溶液,立即把口封闭。发现易拉罐“咔咔”作响并变瘪了,过了一会儿,易拉罐又作响并鼓起来,下列有关判断正确的是
A.导致易拉罐变瘪的离子反应是CO2+OH![]()
![]()
B.导致易拉罐又鼓起来的反应是Al3++3![]()
![]() Al(OH)3↓+3CO2↑
Al(OH)3↓+3CO2↑
C.上述过程中共发生了三个化学反应,且反应结束后的溶液呈碱性
D.若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别处于第二、第三周期的主族元素A和B,它们的离子电子层结构相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B的原子序数分别是( )
A.m、n
B.3、7
C.m﹣2、10﹣n
D.m+2、n+10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com