
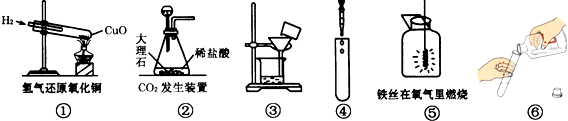
| A、①④⑥ | B、④⑥ |
| C、①②④⑤ | D、④⑤⑥ |


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
| A、两者相等 | B、前者大 |
| C、后者大 | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
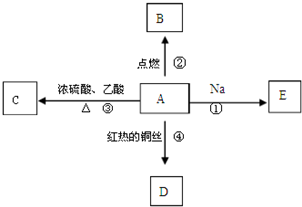 A是乙醇的同系物,其分子中只有1个甲基,相对分子质量为60,它能进行如图所示的多种反应:
A是乙醇的同系物,其分子中只有1个甲基,相对分子质量为60,它能进行如图所示的多种反应:查看答案和解析>>
科目:高中化学 来源: 题型:
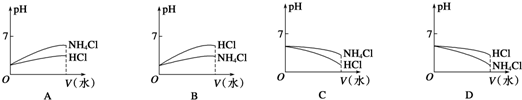
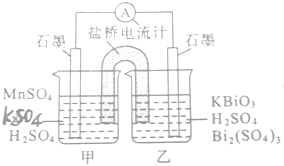
查看答案和解析>>
科目:高中化学 来源: 题型:
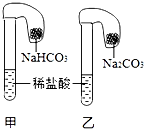 按如图装置进行实验,气球中装有等质量的Na2CO3与NaHCO3,试管中装有等浓度的足量的稀盐酸,把两种药品同时倒入试管中,下列说法正确的是( )
按如图装置进行实验,气球中装有等质量的Na2CO3与NaHCO3,试管中装有等浓度的足量的稀盐酸,把两种药品同时倒入试管中,下列说法正确的是( )| A、甲中气球膨胀得大 |
| B、两气球膨胀一样大 |
| C、甲中消耗的盐酸多 |
| D、乙中气球膨胀得快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它玻璃仪器 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol/L) | c1 | c2 | 0.4 |
| A、若升高温度,反应的平衡常数减小,则正反应为吸热 |
| B、反应5min内,v(PCl3)=0.08 mol?L-1?min-1 |
| C、当容器中Cl2为1.2mol时,可逆反应达到平衡状态 |
| D、平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
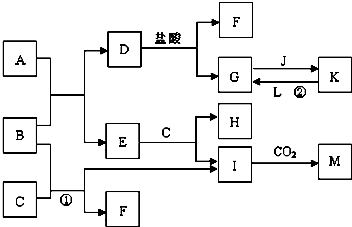 如图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去.常温常压下,A是红棕色金属氧化物,B、D和L都是生产生活中常见的金属单质,B元素是地壳中含量最多的金属元素,F和J为常见的非金属元素的气体单质,且F呈无色、J呈黄绿色,L单质呈紫红色,E和M都是典型的两性化合物;C是氯碱工业的主要产品之一,俗名烧碱;C与K在溶液中反应时有红褐色沉淀生成.
如图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去.常温常压下,A是红棕色金属氧化物,B、D和L都是生产生活中常见的金属单质,B元素是地壳中含量最多的金属元素,F和J为常见的非金属元素的气体单质,且F呈无色、J呈黄绿色,L单质呈紫红色,E和M都是典型的两性化合物;C是氯碱工业的主要产品之一,俗名烧碱;C与K在溶液中反应时有红褐色沉淀生成.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com