
【题目】光气(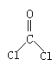 )界面缩聚法合成一种高分子化合物聚碳酸酯G的合成路线如图所示:
)界面缩聚法合成一种高分子化合物聚碳酸酯G的合成路线如图所示:
已知:2 +2NaCl
+2NaCl
(1)C的核磁共振氢谱只有一组吸收峰,C的化学名称为___。
(2)E的分子式为___,H中含有的官能团是氯原子和___,B的结构简式为___。
(3)写出F生成G的化学方程式___。
(4)F与I以1:2的比例发生反应时的产物K的结构简式为___。
(5)H→I时有多种副产物,其中一种含有3个环的有机物的结构简式为___。
(6)4-氯-1,2-二甲苯的同分异构体中属于芳香族化合物的有___种。
(7)写出用2-溴丙烷与D为原料,结合题中信息及中学化学所学知识合成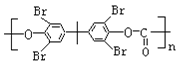 的路线,无机试剂任取。______(已知:一般情况下,溴苯不与NaOH溶液发生水解反应)。
的路线,无机试剂任取。______(已知:一般情况下,溴苯不与NaOH溶液发生水解反应)。
例:CH3CH2OH![]() CH2=CH2
CH2=CH2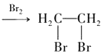
【答案】丙酮 C15H16O2 羧基 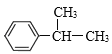 n
n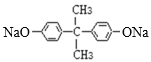 +n
+n ![]()
![]()
![]() +2nNaCl
+2nNaCl 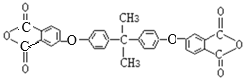
 13
13 
【解析】
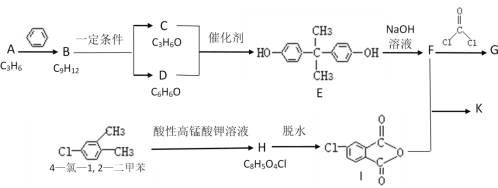
A分子式是C3H6,结构简式为CH2=CH-CH3,与苯发生加成反应产生B: ,B在一定条件下反应产生C:
,B在一定条件下反应产生C:![]() 和D:
和D:![]() ,C、D在一定条件下反应产生E:
,C、D在一定条件下反应产生E: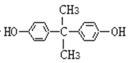 ,E与NaOH溶液反应产生F:
,E与NaOH溶液反应产生F: ,F与光气
,F与光气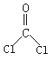 发生反应产生G:
发生反应产生G:![]() ;
;![]() 被酸性KMnO4溶液氧化产生H:
被酸性KMnO4溶液氧化产生H: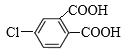 ,H分子中含有2个羧基,脱去1分子水,生成I:
,H分子中含有2个羧基,脱去1分子水,生成I: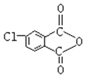 ,F与I以1:2的比例发生反应得到K
,F与I以1:2的比例发生反应得到K  。
。
(7)2-溴丙烷与NaOH的水溶液共热反应产生2-丙醇,然后发生催化氧化产生丙酮;D是![]() ,与浓溴水在Fe作催化剂时发生反应产生
,与浓溴水在Fe作催化剂时发生反应产生 ,丙酮与
,丙酮与 反应产生
反应产生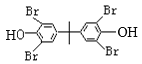 ,该物质与NaOH溶液反应产生
,该物质与NaOH溶液反应产生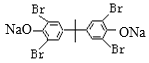 ,
, 与光气反应产生
与光气反应产生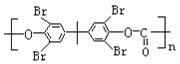 。
。
根据上述分析可知A是CH2=CH-CH3,B是 ,C是
,C是![]() ,D是
,D是![]() ,E:
,E: ,F是
,F是 ,G是
,G是![]() ,H是
,H是 ,I是
,I是 ,K是
,K是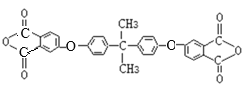 。
。
(1)C结构简式为![]() ,根据物质结构可知C的化学名称为丙酮;
,根据物质结构可知C的化学名称为丙酮;
(2)E结构简式是 ,可知其分子式为C15H16O2,H结构简式为
,可知其分子式为C15H16O2,H结构简式为 ,分子中含有的官能团是氯原子和羧基,B的结构简式为
,分子中含有的官能团是氯原子和羧基,B的结构简式为 。
。
(3)F结构简式是 ,F与光气
,F与光气 发生反应产生G:
发生反应产生G:![]() ;生成G的化学方程式为:n
;生成G的化学方程式为:n +n
+n
![]()
![]() +2nNaCl。
+2nNaCl。
(4)F与I以1:2的比例发生反应时的产物K的结构简式为 。
。
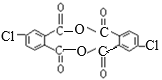
(5)H的结构简式为: ,2个H分子的四个羧基发生分子间脱水反应产生的一种含有3个环的有机物的结构简式为
,2个H分子的四个羧基发生分子间脱水反应产生的一种含有3个环的有机物的结构简式为 。
。
(6)4-氯-1,2-二甲苯的属于芳香族化合物的同分异构体中,若只有一个侧链,可能为-CH2CH2Cl、-CHClCH3两种同分异构体;若有2个侧链,可能是-CH3、-CH2Cl;-Cl、-CH2CH3两种情况,两个取代基的位置有邻、间、对三种位置,因此有两个取代基的同分异构体的种类为2×3=6种;若有三个取代基,分别是-CH3、-CH3、-Cl,取代基三个都相邻的有2种不同的位置,三个取代基都相间的有1种,有两个取代基相邻的有3种不同的情况,所以符合4-氯-1,2-二甲苯的属于芳香族化合物所有同分异构体共有2+6+2+1+3=14种,去掉4-氯-1,2-二甲苯,则4-氯-1,2-二甲苯的芳香族化合物的同分异构体共有13种。
(7)2-溴丙烷与NaOH的水溶液共热反应产生2-丙醇,2-丙醇发生催化氧化产生丙酮;D是![]() ,与浓溴水在Fe作催化剂时发生反应产生
,与浓溴水在Fe作催化剂时发生反应产生 ,丙酮与
,丙酮与 反应产生
反应产生 ,该物质与NaOH溶液反应产生
,该物质与NaOH溶液反应产生 ,
, 与光气反应产生
与光气反应产生 。故合成路线为:
。故合成路线为:
 。
。


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:
【题目】一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量是( )
A. 1.4gB. 2.2gC. 4.4gD. 在2.2g和4.4g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置完成了浓硫酸和SO2性质实验(夹持装置已省略)。请回答:
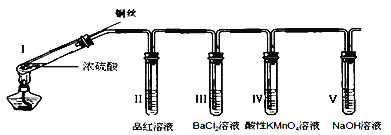
(1)下列说法正确的是__________。
A.反应后,将试管Ⅰ中的白色固体加入水中,溶液呈蓝色
B.取下试管Ⅲ并不断振荡,试管中出现浑浊,是因为生成了BaSO4
C.试管Ⅳ中KMnO4溶液褪色,说明SO2具有氧化性
D.试管V中的NaOH溶液可用Na2CO3溶液代替
(2)取下试管Ⅱ,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色再次变浅。解释“无色→红色→颜色变浅”变化的原因______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s)═CuSO4(s)+5H2O(l)△H=+Q2kJmol-1则Q1、Q2的关系为
A. Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或折开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则反应P4(白磷)+3O2=P4O6的反应热ΔH为

A.-1 638 kJ/molB.+1 638 kJ/molC.-126 kJ/molD.+126 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然化合物α-damascone可用于制作“香水”,其结构为: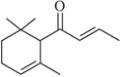 有关该化合物的下列说法不正确的是
有关该化合物的下列说法不正确的是
A.分子式为C13H20OB.该化合物可发生聚合反应
C.1 mol该化合物完全燃烧消耗19 mol O2D.与溴的CCl4溶液反应生成的产物经水解、稀硝酸酸化后可用AgNO3溶液检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g。另取等质量的合金溶于过量稀硝酸中,生成了6.72LNO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为
A.22.1gB.27.2gC.30gD.30.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al的混合物投入![]() 的稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示。则下列说法正确的是
的稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示。则下列说法正确的是![]()
![]()
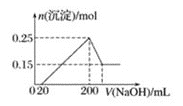
A.Mg、Al的混合物与![]() 的稀硫酸恰好完全反应
的稀硫酸恰好完全反应
B.生成![]() 的体积为
的体积为![]()
C.当加入20mL氢氧化钠溶液时,溶液中的溶质只有硫酸镁和硫酸铝
D.NaOH溶液的物质的量浓度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。请回答下列问题:
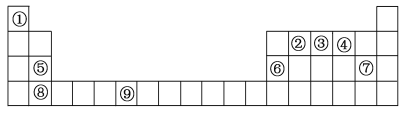
(1)上述元素中,属于s区的是__________ (填元素符号)。
(2)写出元素⑨的基态原子的价电子排布图________。
(3)元素的第一电离能:③________④(选填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为________;该分子为________分子(选填“极性”或“非极性”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com