
【题目】将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g。另取等质量的合金溶于过量稀硝酸中,生成了6.72LNO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为
A.22.1gB.27.2gC.30gD.30.2g
【答案】B
【解析】
将合金加入热氢氧化钠溶液中,铝发生反应,减少的质量就是铝的质量,n(Al)=![]() =
=![]() =0.1mol,m(氢氧化铝)=n(氢氧化铝)×M=0.1mol×78g∕mol=7.8g;n(NO)总=0.3mol.根据方程式Al+4HNO3=Al(NO3)3+NO↑+2H2O可知铝放出NO气体0.1mol.镁和铝放出的一氧化氮为0.3-0.1=0.2mol.镁和铝质量和为11.9-2.7=9.2g,根据3Mg+8HNO3=3Mg(NO3)2+2NO↑+4H2O,Fe+4HNO3=Fe(NO3)3+NO↑+2H2O就可以求出各自的质量,进而求出它们转化得到的沉淀的质量。
=0.1mol,m(氢氧化铝)=n(氢氧化铝)×M=0.1mol×78g∕mol=7.8g;n(NO)总=0.3mol.根据方程式Al+4HNO3=Al(NO3)3+NO↑+2H2O可知铝放出NO气体0.1mol.镁和铝放出的一氧化氮为0.3-0.1=0.2mol.镁和铝质量和为11.9-2.7=9.2g,根据3Mg+8HNO3=3Mg(NO3)2+2NO↑+4H2O,Fe+4HNO3=Fe(NO3)3+NO↑+2H2O就可以求出各自的质量,进而求出它们转化得到的沉淀的质量。
根据上述分析可知,n(Mg)=0.15mol,n(Fe)=0.1mol.Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量=0.15mol×58g∕mol+0.1mol×78g∕mol+0.1mol×107g∕mol=27.2g,选项为:B。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】向乙酸、乙醇、乙酸乙酯和水的平衡体系中加入少量含有18O的![]() ,达到新平衡后,体系中含有18O的物质是
,达到新平衡后,体系中含有18O的物质是
A. 乙酸、乙醇 B. 乙醇、乙酸乙酯
C. 乙醇、乙酸乙酯和水 D. 乙酸、乙醇、乙酸乙酯和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
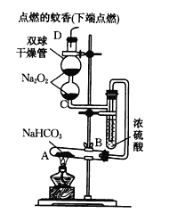
(1)在A试管内发生反应的化学方程式是_____________。
(2)B装置的作用是____________。
(3)在双球干燥管内发生反应的化学方程式为___________________,该反应中氧化剂为________,氧化产物为________,每有1molNa2O2发生反应,转移电子数目为________。
(4)双球干燥管内观察到的实验现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气(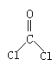 )界面缩聚法合成一种高分子化合物聚碳酸酯G的合成路线如图所示:
)界面缩聚法合成一种高分子化合物聚碳酸酯G的合成路线如图所示:
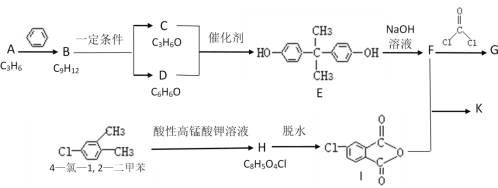
已知:2 +2NaCl
+2NaCl
(1)C的核磁共振氢谱只有一组吸收峰,C的化学名称为___。
(2)E的分子式为___,H中含有的官能团是氯原子和___,B的结构简式为___。
(3)写出F生成G的化学方程式___。
(4)F与I以1:2的比例发生反应时的产物K的结构简式为___。
(5)H→I时有多种副产物,其中一种含有3个环的有机物的结构简式为___。
(6)4-氯-1,2-二甲苯的同分异构体中属于芳香族化合物的有___种。
(7)写出用2-溴丙烷与D为原料,结合题中信息及中学化学所学知识合成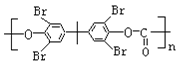 的路线,无机试剂任取。______(已知:一般情况下,溴苯不与NaOH溶液发生水解反应)。
的路线,无机试剂任取。______(已知:一般情况下,溴苯不与NaOH溶液发生水解反应)。
例:CH3CH2OH![]() CH2=CH2
CH2=CH2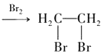
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是()
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=+2b kJ/mol
B.C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l);ΔH=-2b kJ/mol
O2(g)=2CO2(g)+H2O(l);ΔH=-2b kJ/mol
C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=-2b kJ/mol
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=-b kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为____。
(2)反应前A的物质的量浓度是____。
(3)10 s末,生成物D的浓度为__。
(4)A与B的平衡转化率之比为___。
(5)反应过程中容器内气体的平均相对分子质量变化是_(填“增大”、“减小”或“不变”,下同),气体的密度变化是___。
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度____;②增大A的浓度_____;
③恒容下充入氖气________。
(7)下列叙述能说明该反应已达到化学平衡状态的是(填标号)___;
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.A的体积分数不再发生变化
D.器内气体密度不再发生变化
E.相同时间内消耗n mol的B的同时生成2n mol的D
(8)将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s) ![]() NH3(g)+HI(g),2HI(g)
NH3(g)+HI(g),2HI(g) ![]() H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为___。
H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,A元素形成的-2价阴离子比氦的核外电子数多8 个。B元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质。C为原子核内12个中子的第IIA族金属元素,当2.4g C与足量热水反应时,在标准状况下放出气体2.24L。D的M层上有7个电子。
(1)填元素符号:A______,C_______,D_______。
(2)B、C、D最高价氧化物的水化物的化学式依次为_______,其中碱性最强的是________。
(3)比较D的气态氢化物与HF的稳定性:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 的分子式均为C5H8O2,下列说法正确的是( )
的分子式均为C5H8O2,下列说法正确的是( )
A.x分子中碳原子均位于同一平面
B.x、y均能与NaOH溶液发生反应
C.y、z均能与![]() 反应生成
反应生成![]()
D.与它们互为同分异构体的链状羧酸有6种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com