


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应物的转化率 |
| B、反应混和物的浓度 |
| C、正、逆反应速率 |
| D、反应混和物的压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度,溶液颜色由蓝色变为粉红色 |
| B、将CoCl2固体溶于大量水中得到粉红色溶液 |
| C、若用 CoCl2固体作空气湿度指示剂,则湿度增大时,颜色由蓝色变为粉红色 |
| D、将CoCl2溶于浓盐酸,可得到蓝色溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
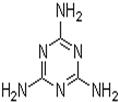 近期有两件事引起了人们的极大关注.“问题奶粉”其问题主要是掺杂了三聚氰胺,该物质的结构如图,
近期有两件事引起了人们的极大关注.“问题奶粉”其问题主要是掺杂了三聚氰胺,该物质的结构如图,查看答案和解析>>
科目:高中化学 来源: 题型:


| 操作步骤(加入试剂) | 实验现象 | 结论 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com