
【题目】(1)在标准状况下,某气体A的密度是1.25 g·L-1,则它的摩尔质量是________;该气体在相同温度和压强下其相对于氢气的密度是______。若该气体是单质,同质量的A与氧气所含的分子数之比为_______________。
(2)某物质的相对分子质量为M,在温度为T时的溶解度为S g,此时测得饱和溶液的密度为d g·cm-3,则该饱和溶液中该物质的物质的量浓度为_______(用代数式表示)。
(3)现实验室要用质量分数为40%的浓氢氧化钠(密度为1.2 g·mL-1)来配制浓度为0.6 mol·L-1的稀氢氧化钠100 mL,问需要这种浓碱的体积是______ mL。
(4)下列有关实验操作或判断不正确的是________。
A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大
B.用干燥的pH试纸测定氯水的pH
C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸并搅拌
D.观察钾元素焰色反应的操作:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察
E.制备氢氧化亚铁时,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中
【答案】 28g/mol 14 8:7 1000Sd/[(100+S)M] 5 BD
【解析】(1)摩尔质量是指单位物质的量的物质所具有的质量,标况下1mol气体为22.4L,则气体A的摩尔质量M=ρVm=1.25 g/L×22.4L/mol=28g/mol。根据pV=nRT,可得p![]() =
=![]() RT,同温同压下,密度与摩尔质量成正比,所以该气体在同温同压下相对H2的密度=
RT,同温同压下,密度与摩尔质量成正比,所以该气体在同温同压下相对H2的密度=![]() =14。气体质量相同时,物质的量之比与摩尔质量成反比,所以同质量时
=14。气体质量相同时,物质的量之比与摩尔质量成反比,所以同质量时![]() ;气体的物质的量与分子数成正比,所以同质量的A与氧气所含的分子数之比为8:7。
;气体的物质的量与分子数成正比,所以同质量的A与氧气所含的分子数之比为8:7。
故答案为:28g/mol;14;8:7。
(2)取该饱和溶液(100+S)g,则溶液中溶剂质量为100g,溶质为Sg。n(溶质)= ![]() ;溶液的体积V=
;溶液的体积V= ![]() =
= ![]() ,则该饱和溶液中溶质的物质的量浓度为c=
,则该饱和溶液中溶质的物质的量浓度为c= ![]() 。
。
(3)用浓NaOH溶液配制稀溶液过程中NaOH物质的量保持不变,即C浓×V浓=C稀×V稀。40%的浓NaOH溶液中c(NaOH)= ![]() =12mol/L,所以0.6mol/L×100mL=12mol/L×V浓,则V浓=5mL。需要这种浓碱的体积是5.0mL。
=12mol/L,所以0.6mol/L×100mL=12mol/L×V浓,则V浓=5mL。需要这种浓碱的体积是5.0mL。
(4)A、定容时俯视刻度线,会导致溶液体积偏小,所配溶液浓度偏大,故A正确;B、氯水具有漂白性,会漂白pH试纸,所以不能用pH试纸测氯水的pH,故B错误;C、由于浓硫酸稀释过程中放出大量的热,且浓硫酸密度大于水,所以配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌,故C正确;D、将铂丝放在稀盐酸中洗涤后,应先灼烧至无色,再用铂丝蘸取固体氯化钾,进行实验,故D错误;E、氢氧化亚铁易被空气中的氧气氧化为氢氧化铁,应隔绝空气制取,所以滴加NaOH溶液时,应将滴管伸入硫酸亚铁溶液中,故E正确。故选BD。


 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】根据已学知识,请你回答下列问题:
(1)最外层电子排布为4s24p1的原子的核电荷数为 . 某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4 , 该元素的名称是 .
(2)根据VSEPR模型,PO43﹣的分子立体结构为:;乙醇易溶于水的原因是;HClO4的酸性强于HClO的原因是;
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体为 .
(4)某元素核外有三个电子层,最外层电子数是核外电子总数的 ![]() ,写出该元素原子的电子排布式是 . 写出铬元素在周期表中的位置 , 它位于区.
,写出该元素原子的电子排布式是 . 写出铬元素在周期表中的位置 , 它位于区.
(5)如图是氯化铯晶体的晶胞示意图(晶体中最小的重复结构单元),已知晶体中2个最近的Cs+核间距为a pm,氯化铯(CsCl)的相对分子质量M,NA为阿伏伽德罗常数,则氯化铯晶体的密度为g/cm3 . 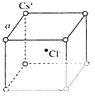
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ba(OH)2、CuSO4、HCl可以归为一类,下列物质可以和它们归为一类( )
A. 75%的酒精溶液 B. 硝酸钠 C. Fe(OH)3胶体 D. 豆浆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SnSO4用于合金、马口铁、汽缸活塞、钢丝等酸性电镀,电子器件的光亮镀锡等.另外,还用于铝合金制品涂层氧化着色,印染工业用作媒染剂,有机溶液中双氧水去除剂等.工业上SnSO4的制备路线如图: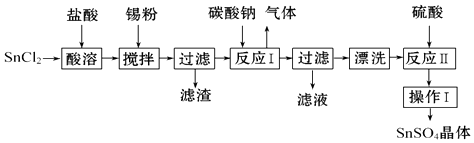
已知:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化.
Ⅱ.SnCl2易水解生成碱式氯化亚锡.
回答下列问题:
(1)锡原子的核外电子数为50,与碳元素同主族,锡元素在周期表中的位置是 .
(2)操作Ⅰ是、、过滤、洗涤.
(3)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因: .
(4)加入锡粉的作用有两个:①调节溶液pH,② .
(5)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是 .
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 .
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,反应为Sn+2HCl═SnCl2+H2↑;
②加过量FeCl3氧化Sn2+生成Sn4+;
③用已知浓度的盐酸酸化过的K2Cr2O7滴定生成的FeCl2 , 反应的化学方程是:6FeCl2+K2Cr2O7+14HCl═6FeCl3+2KCl+2CrCl3+7H2O.
取1.360g锡粉,经上述各步反应后,共用去0.100molL﹣1K2Cr2O7溶液33.00mL,则锡粉中锡的质量分数是 . (保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图) 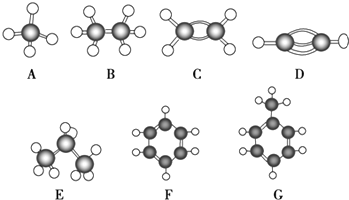
据此回答下列问题:
(1)常温下含碳量最高的气态烃是(填对应字母).
(2)能够发生加成反应的烃有(填数字)种.
(3)一卤代物种类最多的是(填对应字母) .
(4)写出实验室制取C的化学方程式 .
(5)写出F发生溴代反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐中含有一定量的镁、铁等物质,加碘盐中碘的损失主要由于杂质、水份、空气中的氧气以及光照,受热而引起的. 已知:氧化性:IO3﹣>Fe3+>I2还原性:S2O32﹣>I﹣
反应式:3I2+6OH﹣═5I﹣+IO3﹣+3H2O,KI+I2KI3
(1)某学习小组对加碘盐进行了如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+).用适量蒸馏水溶解,并加稀硫酸酸化,将所得溶液分3份:第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显示淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入足量的KIO3固体后,滴加淀粉试剂,溶液不变色. ①该红色物质是(用化学式表示);CCl4中显示紫红色的物质是(用电子式表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为;
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失.写出潮湿环境中KI与氧气反应的化学方程式: . 将I2溶于KI溶液,在低温条件下,可制得KI3H2O.该物质作为食盐加碘剂是否合适?
(填“是”或“否”),并说明理由: .
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是 .
A.Na2S2O3
B.AlCl3
C.Na2CO3
D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人体必需的微量元素,在肺部,血红蛋白中血红素的Fe2+与O2结合,把O2送到各个组织器官。铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)【铁元素的分离】 称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。在坩埚中高温灼烧黑木耳,使之完全灰化。用酸充分溶解,过滤,滤液备用。
①浸泡液检测不出铁元素的原因是________。
②滤液中铁元素的存在形式是Fe2+、________。
(2)【配制溶液】 将滤液配制成100 mL 溶液。选择合适的仪器完成“铁元素的分离”、
“配制溶液”2个实验,下列仪器不必使用的是_______。

(3)【铁元素含量测定】 研学小组提出如下测量方案:
Ⅰ.沉淀法:向溶液中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。评价该测量方案是否可行________。
Ⅱ.比色法:流程示意如下:
![]()
① 用离子方程式解释加入H2O2的目的是________。
② 溶液a的颜色是________。
③ 溶液颜色越深,光的透过能力越差,即透光率越小。若不加H2O2,测出黑木耳中铁元素的含量________(填“偏大”或“偏小”)。
(4)亚铁盐易被氧化,但在体内Fe2+参与O2的运输却不被氧化。蛋白质是一种既有亲水部分、又有疏水部分的大分子,为血红素提供了疏水环境。

可见,氧化还原反应能否发生与_________有关。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com