
【题目】高温、催化剂条件下,某反应达到平衡,平衡常数K=c(CO)·c(H2O)/c(CO2)·c(H2)恒容时,温度升高,H2浓度减小.下列说法正确的是
A. 该反应的焓变为负值
B. 升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
C. 2CO2(g)+2H2(g)2CO(g)+2H2O(g) 的平衡常数K1=K2
D. 若恒容、恒温下充入CO,则K值变大
科目:高中化学 来源: 题型:
【题目】形成酸雨的原理之一可表示如下:

请回答下列问题:
(1)未污染的雨水的pH一般小于7大于5.6,这是由于溶解了___的缘故;酸雨的pH小于5.6,主要含有硫酸、___和一些有机酸等。
(2)图中三个反应不属于氧化还原反应的是___(填标号);写出反应②的化学方程式___。
(3)某研究性学习小组取来雨水做水样进行测定,随时间的推移雨水样品的pH值会变小,主要原因是为___(用化学方程式表示)。
(4)你认为减少酸雨产生的途径可采取的措施是____。(选填字母编号)
①少用煤做燃料 ②把工厂的烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
(5)从保护环境的角度出发,一些工厂采用“钙基固硫法”,即在含硫的煤中混入生石灰后燃烧,大部分SO2最终将转化为_____。
(6)汽车尾气中的CO,NO排放也是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个“催化转化器”,使CO与NO反应,生成两种无毒气体,其中之一是N2。写出NO与CO反应的化学方程式___,此反应的缺点是在一定程度上提高空气的酸度,其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铁粉与水蒸气在不同温度下反应,所得黑色固体产物的成分不同,某化学小组的同学为测定该固体产物的组成,称取168mg纯铁粉,按下列步骤进行实验:
①如图所示连接好装置检查气密性装入药品
②打开K,加热某装置,一段时间后,再加热另一装置;
③反应完成后,关闭K,停止加热,冷却后读取收集到的气体的体积

回答下列问题:
(1)实验中先点燃___________处的酒精灯,该操作在将D中的导管伸入量筒中准备收集气体之______ (填“前”或“后”)
(2)下列实验操作的目的是:
①将铁粉和石棉绒混合均匀___________;
②关闭K___________。
(3)判断铁粉与水蒸气反应已经完成的现象是___________。
(4)有同学认为用D装置测量气体的体积时,伸入量筒中的导管应适当加长,该同学的理由是___________。
(5)用改进后的正确装置进行实验,收集到气体的体积为67.2mL(已换算成标准状况),则固体产物的组成为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。

请回答下列问题:
(1)在“图1”中,曲线____填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g)![]() CH3OH(g)的△H= _________________________ 。
CH3OH(g)的△H= _________________________ 。
(2)下列说法正确的是 (_________)
A.起始充入的CO的物质的量为1mol
B.增加CO的浓度,H2的转化率会增大
C.容器中压强恒定时,反应达到平衡状态
(3)从反应开始到建立平衡,υ(CO)= _______;达到平衡时,c(H2)= ____ ,该温度下CO(g)+2H2(g) ![]() CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)。
CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工厂生产的氯气和氢气可以进一步用于生产盐酸,主要过程如下:

(1)其中关键的一步为氯气和氢气在燃烧管口燃烧生成HCl,氯气有毒,应采取的措施是____。合成盐酸厂要求合成气中的HCl的含量要大于97%,试用最简便的方法进行分析是否含量大于97%____。
(2)氯碱工厂生产的氯气和氢氧化钠溶液可以用于制取“84消毒液”,反应的化学方程式为__。
(3)某同学欲证明盐酸与氯化氢气体性质不同,他分别向A、B、C三支洁净试管中各放入一片干燥的蓝色石蕊试纸,然后往A试管内加入盐酸,试纸显___色,往B试管中通入干燥的氯化氢气体,试纸显___色.最后向C试管中加入物质___(填化学式),他之所以加入这种物质的理由是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意回答下列问题(填字母)

(1)写出上图中序号①~③仪器的名称:
①____②____③____。
(2)分离Na2CO3溶液和CH3COOC2H5(液体,难溶于水):选___,操作名称为___。
(3)用CCl4提取碘水中的碘,选____,操作名称为___。
(4)粗盐提纯,选____,操作名称为____。
(5)石油中得到汽油和煤油,选____,操作名称为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废液中Cr2O7可通过下列反应转化成铬黄(PbCrO4):
Cr2O![]() (aq)+2Pb2+(aq)+H2O(l)
(aq)+2Pb2+(aq)+H2O(l) ![]() 2PbCrO4(s)+2H+(aq) ΔH<0
2PbCrO4(s)+2H+(aq) ΔH<0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是 ( )。
A. 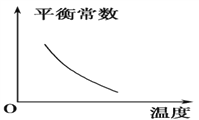 B.
B. 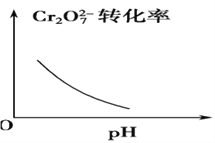
C.  D.
D. 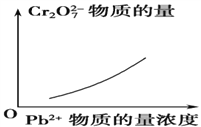
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净的CaCO3与100 mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )

A.OE段表示的平均速率最快
B.EF段,用盐酸表示该反应的平均反应速率为0.4 mol·L-1·min-1
C.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2∶6∶7
D.F点收集到的CO2的量最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL1mol·L-1元酸HA溶液中,不断滴加1mol·L-1的NaOH溶液所加碱的体积与-lgc水(H+)的关系如图所示。c水(H+)为溶液中水电离的c(H+)。下列说法不正确的是

A. 常温下,Kα(HA)的数量级为10-4
B. a、b两点pH均为7
C. 从a点到b点,水的电离程度先增大后减小
D. 溶液的导电性逐渐增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com