
����Ŀ����֪������ˮ�����ڲ�ͬ�¶��·�Ӧ�����ú�ɫ�������ijɷֲ�ͬ��ij��ѧС���ͬѧΪ�ⶨ�ù���������ɣ���ȡ168mg�����ۣ������в������ʵ�飺
����ͼ��ʾ���Ӻ�װ�ü��������װ��ҩƷ
�ڴ�K������ijװ�ã�һ��ʱ����ټ�����һװ�ã�
�۷�Ӧ��ɺر�K��ֹͣ���ȣ���ȴ���ȡ�ռ�������������

�ش��������⣺
(1)ʵ�����ȵ�ȼ___________���ľƾ��ƣ��ò����ڽ�D�еĵ���������Ͳ�����ռ�����֮______ (����ǰ����������)
(2)����ʵ�������Ŀ���ǣ�
�ٽ����ۺ�ʯ����Ͼ���___________��
�ڹر�K___________��
(3)�ж�������ˮ������Ӧ�Ѿ���ɵ�������___________��
(4)��ͬѧ��Ϊ��Dװ�ò�����������ʱ��������Ͳ�еĵ���Ӧ�ʵ��ӳ�����ͬѧ��������___________��
(5)�øĽ������ȷװ�ý���ʵ�飬�ռ�����������Ϊ67.2mL(�ѻ���ɱ�״��)��������������Ϊ___________��
���𰸡�A �� ����������ˮ�����ĽӴ�������Ա��ַ�Ӧ ��ֹ��ȴʱ��װ���ڵ�ѹǿ�½����콫��������װ�ã�Ӱ��H2����IJⶨ ��Ͳ��Һ�治�ٷ����仯 ������̫�̣���ȴʱ�����岻�ܻ����������������ƫ��������̫�������ܲ��ײ�����Ͳ�У�Ҳ���״���Ͳ��ȡ�� FeO
��������
(1)��װ���ں��п�����������Fe�ڼ���ʱ�ᷢ����ѧ��Ӧ������Ҫ�ȼ���A���ƾ��ƣ�ʹװ���ڳ���ˮ������Ȼ���ټ���B���ƾ��ƣ�����A���ƾ���Ӧ�����ռ�H2�IJ���֮����У�
(2)�����ʵĴ���״̬��Ӱ�컯ѧ��Ӧ���ʵĽǶȷ�������ѹǿӰ�����ʵ��ռ������ȷ�������Ŀ�ģ�
(3)��Ӧ������H2��������ˮ�����壬����Ӧ���ٷ�������������������
(4)�����������������������������������
(5)�ȼ���Fe��H2�����ʵ���������H2��Fe��ˮ��Ӧ�IJ����������������Ļ�ѧʽ��
(1)װ���еĿ�����Fe�ᷢ����Ӧ��Ӱ��ʵ��ⶨ�����Ҫ�ȼ���A���ľƾ��ƣ���ˮ�����ų�װ���ڵĿ������Է��������Ⱥ��������Ӧ����Ӧ��װ���ڻ�����H2�����뽫װ���ڵ�����ȫ���ռ�����Ͳ�У�������������������ƫС���ʼ���AǰҪ�Ȱ�D���ռ�װ�ð�װ�ã�����ȼA���ƾ����ڽ�D�еĵ���������Ͳ�����ռ�����֮����У�
(2)��Fe�ǹ������ʣ�Ϊ����ˮ������Fe�۷�Ӧ�ĽӴ����������ʹ��ʯ���ޣ�ʹFe�۸�����ʯ�����ϣ�
�ڷ�Ӧ��ɺر�K��ֹͣ���ȣ���ȴ���ȡ�ռ����������������ر�KĿ���Ƿ�ֹ��ȴʱ��װ���ڵ�ѹǿ�½����콫��������װ�ã�Ӱ��H2����IJⶨ��
(3)������ˮ�������ɺ�ɫ��������۵���ɫ�������֣�ֻ�ܸ��ݷ�Ӧ������H2�������ԣ��ò��ٲ������壬�����������������仯��Ϊ��Ӧ��ɵı�־��
(4)��ͬѧ��Ϊ��Dװ�ò�����������ʱ��������Ͳ�еĵ���Ӧ�ʵ��ӳ�����ԭ���Ƿ�Ӧ���ڼ���ʱ���еģ��������������¶ȸ�ʱ������¶Ƚ���ʱ�����С��������̫�̣���ȴʱ�����岻�ܻ����������������ƫ����������̫�������ܾͲ��ײ�����Ͳ�У���Ӧ����ʱ������Ҳ���״���Ͳ��ȡ����
(5)n(Fe)=0.168g��56g/mol=0.003mol��n(H2)=0.0672L��22.4L/mol=0.003mol��n (Fe)��n (O) =1��1�����Ը��ݵ����غ㡢Ԫ���غ㣬�ɵ÷�Ӧ����ʽΪFe+H2O(g)![]() FeO+H2�������ù��廯ѧʽΪFeO��
FeO+H2�������ù��廯ѧʽΪFeO��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У����������ֻ�����Ӧ���͵�����������ԭ��Ӧ����
A.2FeCl3+Cu=2FeCl2+CuCl2
B.CuSO4+H2S=CuS��+H2SO4
C.Cu2(OH)2CO3![]() 2CuO+CO2��+H2O
2CuO+CO2��+H2O
D.4Fe(OH)2+O2+2H2O=4Fe(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú����Ҫ�Ļ���ԭ�ϣ���ú��ȼ�ϲ����˷ѣ���������ú�к�����Ļ����FeS2��ȼ��ʱ����SO2������ɻ�����Ⱦ������һ������3���˿ڵ�С�ͳ��У�ƽ��ÿ��ȼú5kg������ú��FeS25%����ȼ��ʱ����90%��Sת��ΪSO2��������������У��Լ��㣺
��1���ó��н�������ȼ����úһ�꣨365�죩��������ŷ�SO2������������ٶ֣�______
��2��������ЩSO2ȫ���ܻ��գ�������98%��H2SO4���ٶ֣�____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������100 mL 1.0 mol��L��1��ϡ�����Ҫ�õ�������(����)
A.������ƽB.�ձ�C.��ͲD.100 mL����ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼΪij��ѧ��Ӧ����һʱ��ͼ����t1ʱ�������¶Ȼ�����ѹǿ��������ͼ��ʾ�仯�ķ�Ӧ��

A. 4NH3��g��+5O2��g��![]() 4NO��g��+6H2O��g����H��0
4NO��g��+6H2O��g����H��0
B. 2SO2��g��+O2��g��![]() 2SO3��g����H�� 0
2SO3��g����H�� 0
C. H2��g��+I2��g��![]() 2HI��g����H��0
2HI��g����H��0
D. C��s��+H2O��g��![]() CO��g��+H2��g����H��0
CO��g��+H2��g����H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʵ���Ҫ���������ʽṹ����ش��������⣺
(1)��֪Ԫ��M���������Ca5(PO4)3F��һ��Ԫ�ء�Ԫ��M����̬ԭ�����ʧȥ��1������5��������������(�������ܣ��÷���I1��I��ʾ)�����ʾ��
I1 | I2 | I3 | I4 | I5 | |
������(kJ/mol) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
Ԫ��M����̬�������ϼ���___________�ۣ����̬ԭ�ӵ����Ų�ʽΪ___________��
(2)������ͭ��Һ�м��������ˮ�����γ�[Cu(NH3)4]SO4����Һ������Һ�������ܽ���ά�ء�
��[Cu(NH3)4]SO4�������ӵ����幹����___________��
�ڳ���Ԫ���⣬[Cu(NH3)4]SO4������Ԫ�صĵ縺����С�����˳��Ϊ___________��
��NF3��NH3�Ŀռ乹����ͬ������ԭ�ӵĹ���ӻ����;�Ϊ___________����NF3������Cu2+�γɻ�ѧ������ԭ����___________��
(3)һ��Hg-Ba-Cu-O���³������ϵľ���(������)��ͼ��ʾ��

�ٸ����ʵĻ�ѧʽΪ___________��
����֪�þ���������Ba2+�ļ��Ϊcpm�������Ba2+�����Hg+��ĿΪ___________�������ߵ���̾���Ϊ___________pm��(�г�����ʽ���ɣ���ͬ)
��������ʵ�Ħ������ΪM�������ӵ�������ֵΪNA����þ�����ܶ�Ϊ___________g��cm��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������Ԫ��ԭ�Ӹ����Ӳ���������ɵĵ�����Ϊ2n2��n��ʾ���Ӳ�����������X�����ϵ�Ԫ��ԭ�Ӹ����Ӳ���������ɵĵ�����Ϊn(n+1)��n��ʾ���Ӳ�������������Ԫ��ԭ�ӵĵ����Ų������������������ͬ���ش��������⣺
��1��X�����ϵ�������Ϊ5��Ԫ��ԭ������������Ϊ___����
��2��X�����ϵ�������Ϊ9��Ԫ��ԭ�ӵĽṹʾ��ͼΪ___����Ԫ������___Ԫ�أ���������ǽ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¡����������£�ij��Ӧ�ﵽƽ�⣬ƽ�ⳣ��K=c(CO)��c(H2O)/c(CO2)��c(H2)����ʱ���¶����ߣ�H2Ũ�ȼ�С������˵����ȷ����
A. �÷�Ӧ���ʱ�Ϊ��ֵ
B. �����¶ȣ�����Ӧ���������淴Ӧ���ʼ�С��ƽ�������ƶ�
C. 2CO2(g)+2H2(g)2CO(g)+2H2O(g) ��ƽ�ⳣ��K1=K2
D. �����ݡ������³���CO����Kֵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2Sȼ�ϵ��Ӧ��ǰ���dz��������õ��ʾ��ͼ���¡�����˵����ȷ���ǣ� ��
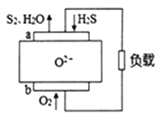
A. �缫a������ B. O2-�ɵ缫a����缫b
C. �缫 a �ķ�ӦʽΪ��2H2S+2O2--4e-=S2+2H2O D. ��ͨ��1.12LO2��ת�Ƶ�����0.2NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com