
【题目】下列反应中,不属于四种基本反应类型但属于氧化还原反应的是
A.2FeCl3+Cu=2FeCl2+CuCl2
B.CuSO4+H2S=CuS↓+H2SO4
C.Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
D.4Fe(OH)2+O2+2H2O=4Fe(OH)3
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互溶,其固溶体为面心立方晶格。铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。
(1)基态钴原子的价电子排布图为___________。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体(如下图)。科学研究表明,顺式分子具有抗癌活性。

①吡啶分子是大体积平面配体,其结构简式如图所示![]() 。每个吡啶分子中含有的σ键数目为___________。吡啶分子中所含的各元素的电负性由大到小的顺序是___________。
。每个吡啶分子中含有的σ键数目为___________。吡啶分子中所含的各元素的电负性由大到小的顺序是___________。
②二氯二吡啶合铂中存在的微粒间作用力有___________(填字母)。
a.范德华力 b.氢键 c.金属键 d.非极性键
③反式二氯二吡啶合铂分子是___________(填“极性分子”或“非极性分子”)。

(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如下图所示。
①“分子金属”可以导电,是因为___________能沿着其中的金属原子链流动。
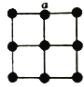
②“分子金属”中,铂原子是否以sp3的方式杂化?_________(填“是”或“否”),其理由是_______。
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为dg·cm-3,则晶胞参数a=______nm(列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验(夹持装置未画出),能达到实验目的的是
A. 实验甲:CuSO4溶液中会形成一条光亮的通路
B. 实验乙:试管中溶液变为红色
C. 实验丙:将湿润的有色布条放入盛有干燥氯气的瓶中,布条不褪色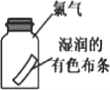
D. 实验丁:将灼烧至黑色的铜丝插入无水乙醇,铜丝变成紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,它们的相关信息如下表:
元素代号 | 相关信息 |
A | 最外层的电子数是次外层电子数的3倍 |
B | 海水中含量第一位的金属元素 |
C | L层得1个电子后成为稳定结构 |
D | 二价阴离子核外有18个电子 |
E | 失去一个电子后就成为一个质子 |
F | 单质为黄绿色气体,具有刺激性气味 |
请填写下列空格:
(1)A原子的电子式:_____。
(2)B离子的结构示意图:_______。
(3)C元素的名称:___,C原子中能量最高的电子位于第______层,与C离子质子数与电子数均相同的微粒可能是______(用微粒符号表示)。
(4)D的二价阴离子的电子式:___,D元素的某种同位素原子质量数为34,该原子核内的中子数为_____。
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R为五种短周期主族元素,Y、Z、W是原子序数递增的同周期相邻元素,且最外层电子数之和为15;X比Y核外少一个电子层;R的质子数是X、Y、Z、W四种元素质子数之和的![]() .下列说法正确的是( )
.下列说法正确的是( )
A. 简单离子半径:![]()
B. X与Y形成的二元化合物常温下一定为气态
C. W和R形成的化合物是离子化合物
D. Y与W、Z与W形成的二元化合物都是大气污染物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应m A(g)+n B(g) ![]() p C(g) △H,在密闭容器中进行,下图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线。由曲线分析,下列判断正确的是
p C(g) △H,在密闭容器中进行,下图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线。由曲线分析,下列判断正确的是

A. T1<T2,P1>P2,m+n>p,△H<0
B. T1>T2,P1<P2,m+n>p,△H>0
C. T1<T2,P1>P2,m+n<p,△H<0
D. T1>T2,P1<P2,m+n<p,△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,固定体积的密闭容器中发生反应M(g)+N(g)![]() 2W(g),能说明该反应一定达到平衡的是( )
2W(g),能说明该反应一定达到平衡的是( )
A.v(W)消耗=v(W)生成B.v正=v逆=0
C.容器内气体总质量不变D.n(M)∶n(N)∶n(W)=1∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】形成酸雨的原理之一可表示如下:

请回答下列问题:
(1)未污染的雨水的pH一般小于7大于5.6,这是由于溶解了___的缘故;酸雨的pH小于5.6,主要含有硫酸、___和一些有机酸等。
(2)图中三个反应不属于氧化还原反应的是___(填标号);写出反应②的化学方程式___。
(3)某研究性学习小组取来雨水做水样进行测定,随时间的推移雨水样品的pH值会变小,主要原因是为___(用化学方程式表示)。
(4)你认为减少酸雨产生的途径可采取的措施是____。(选填字母编号)
①少用煤做燃料 ②把工厂的烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
(5)从保护环境的角度出发,一些工厂采用“钙基固硫法”,即在含硫的煤中混入生石灰后燃烧,大部分SO2最终将转化为_____。
(6)汽车尾气中的CO,NO排放也是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个“催化转化器”,使CO与NO反应,生成两种无毒气体,其中之一是N2。写出NO与CO反应的化学方程式___,此反应的缺点是在一定程度上提高空气的酸度,其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铁粉与水蒸气在不同温度下反应,所得黑色固体产物的成分不同,某化学小组的同学为测定该固体产物的组成,称取168mg纯铁粉,按下列步骤进行实验:
①如图所示连接好装置检查气密性装入药品
②打开K,加热某装置,一段时间后,再加热另一装置;
③反应完成后,关闭K,停止加热,冷却后读取收集到的气体的体积

回答下列问题:
(1)实验中先点燃___________处的酒精灯,该操作在将D中的导管伸入量筒中准备收集气体之______ (填“前”或“后”)
(2)下列实验操作的目的是:
①将铁粉和石棉绒混合均匀___________;
②关闭K___________。
(3)判断铁粉与水蒸气反应已经完成的现象是___________。
(4)有同学认为用D装置测量气体的体积时,伸入量筒中的导管应适当加长,该同学的理由是___________。
(5)用改进后的正确装置进行实验,收集到气体的体积为67.2mL(已换算成标准状况),则固体产物的组成为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com