
【题目】用下列实验装置进行相应实验(夹持装置未画出),能达到实验目的的是
A. 实验甲:CuSO4溶液中会形成一条光亮的通路
B. 实验乙:试管中溶液变为红色
C. 实验丙:将湿润的有色布条放入盛有干燥氯气的瓶中,布条不褪色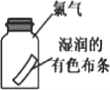
D. 实验丁:将灼烧至黑色的铜丝插入无水乙醇,铜丝变成紫红色
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】以海水为电解质的Mg-AgCl电池在军事上可用作电动鱼雷的电源,其电池反应离子方程式为:2AgCl+Mg=Mg2++2Ag+2Cl-。该电池工作时,下列说法正确的是

A. 正、负极的质量均减少 B. AgCl电极发生氧化反应
C. 电子由AgCl经外电路流向Mg D. 实现了电能向化学能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列实验。(a、b为弹餐夹,其他装置略去)
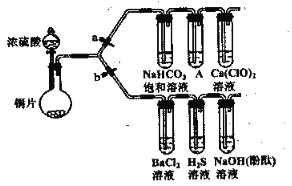
I验证SO2具有氧化性、还原性和酸性氧化物的通性。
(1) 连接仪器、检查装置气密性、加药品后,打开b (关闭a),然后滴入浓硫酸,加热。装有浓硫酸的仪器名称是___________,铜与浓硫酸反应的化学方程式是___________ 。
(2) 能验证SO2具有氧化性的实验现象是__________________________________________。
(3) 装有BaCl2溶液的试管中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀的化学式分别是___________,___________。写出其中SO2显示还原性并生成白色沉淀的总的离子方程式____________________________________________。
(4) 能验证SO2具有酸性氧化物的通性的实验现象是________________________________, 若通入过量的SO2,其化学方程式是____________________________________________。
II验证酸性的相对强弱:碳酸>次氯酸。(已知酸性:亚硫酸>碳酸)
(5) 打开a关闭b。装置A中的足量的试剂是___________。利用该装置能否判断碳酸的酸性比次氯酸强,理由是_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如下图所示(已知pKa=-lgKa),下列说法正确的是

A. H3AsO4溶液pKa2为4.5
B. NaH2AsO4溶液显碱性
C. 常温下,m点对应溶液中由水电离出的OH—浓度为10—11.5 mol/L
D. n点对应溶液中,离子浓度关系:c(HAsO42—)=c(H2AsO4—)>c( OH—) =c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种从铜电解工艺的阳极泥中提取Se和Te的流程如下:

下列叙述错误的是( )
A. 合理处理阳极泥有利于保护环境和资源再利用
B. 流出液是H2SO4溶液
C. 电解过程中阴极上析出单质Te
D. “焙砂”与碳酸钠充分混合后,可在瓷坩锅中焙烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)系统命名法命名下列物质:
 __________________________________;
__________________________________;
(2)书写下列物质的结构简式:
①2,6-二甲基-4-乙基辛烷:______________;②间三甲苯______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组用如下图所示装置制备、收集Cl2,并进行性质验证实验(夹持装置略去)。下列说法正确的是( )

A. 用![]() 和浓盐酸制备
和浓盐酸制备![]() 时,只选
时,只选![]()
B. ![]() 用于
用于![]() 收集时,a为进气口
收集时,a为进气口
C. ![]() 中加入NaBr溶液和
中加入NaBr溶液和![]() ,通入
,通入![]() 反应后振荡、静置,下层溶液呈橙红色
反应后振荡、静置,下层溶液呈橙红色
D. ![]() 中通入
中通入![]() 使品红溶液褪色后,取出溶液加热可恢复红色
使品红溶液褪色后,取出溶液加热可恢复红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于四种基本反应类型但属于氧化还原反应的是
A.2FeCl3+Cu=2FeCl2+CuCl2
B.CuSO4+H2S=CuS↓+H2SO4
C.Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
D.4Fe(OH)2+O2+2H2O=4Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤是重要的化工原料,用煤作燃料不仅浪费,而且因烟煤中含有硫的化合物(FeS2)燃烧时生成SO2气体造成环境污染。假设一个具有3万户人口的小型城市,平均每户燃煤5kg,这种煤含FeS25%,在燃烧时如有90%的S转化为SO2,并被排入大气中,试计算:
(1)该城市仅居民作燃料用煤一年(365天)向大气中排放SO2的总质量达多少吨?______
(2)假如这些SO2全部能回收,可生产98%的H2SO4多少吨?____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com