
����Ŀ��������(AlN)��һ���������ǽ������ϡ�ijAlN��Ʒ������Al2O3���ʣ�Ϊ�ⶨAlN�ĺ����������������ʵ�鷽��������֪��AlN+NaOH+ 2H2O==NaAlO2+ NH3��
������1��ȡһ��������Ʒ��������װ�òⶨ��Ʒ��AlN�Ĵ���(�г�װ������ȥ)��

��1����ͼCװ�������θ���ܵ������� ��
��2���������ʵ�鲽�裺��װ��ʵ��װ�ã����ȼ�������ԣ��ټ���ʵ��ҩƷ����������ʵ������� ,��Һ©������������NaOHŨ��Һ�������ٲ������塣��K1��ͨ�뵪��һ��ʱ�䣬�ⶨCװ�÷�Ӧǰ��������仯��ͨ�뵪����Ŀ���� ��
��3������װ�ô���ȱ�ݣ����²ⶨ���ƫ�ߣ�������Ľ���� ��
������2������ͼװ�òⶨm g��Ʒ��A1N�Ĵ���(���ּг�װ������ȥ)��

��4��Ϊ�ⶨ������������������װ���е�XҺ�������___________
A��CCl4 B��H2O C��NH4Cl��Һ D����
��5����m g��Ʒ��ȫ��Ӧ�����������������ΪV mL(��ת��Ϊ��״��)����AIN������������__________��
������3�������²���ⶨ��Ʒ��A1N�Ĵ��ȣ�

��6����������ɳ��������ӷ���ʽΪ________________
��7�����ڲ������δϴ�ӣ��ⶨ�����__________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
���𰸡���1�������� ��2���ر�K1����K2 ��װ���в����İ���ȫ������Cװ��
��3��Cװ�ó��ڴ�����һ������װ�� ��4��AD ��5��41V/22400m��100%
��6��CO2+ AlO2+ 2H2O=HCO3 + Al(OH)3 ��7��ƫ��
��������
�����������1������װ�ú����������÷�������������Ũ�����ܷ�����Ӧ�����壬������������ͼCװ�������θ���ܵ������Ƿ�������
��2����װ��ʵ��װ�ã���ԭ����֪�����Ʊ���Ҫ�ȼ��װ�������ԣ�����ʵ��ҩƷ����������ʵ������ǹر�K1����K2����Һ©������������NaOHŨ��Һ�������ٲ������塣��K1��ͨ�뵪��һ��ʱ�䣬�ⶨCװ�÷�Ӧǰ��������仯��ͨ�뵪����Ŀ������װ���в����İ���ȫ������Cװ�ã�ȷ�ⶨװ��C��������
��3����װ�ô�����ȱ���ǿ����е�ˮ�����Ͷ�����̼Ҳ���Խ���װ��C��ʹ�ⶨ���ƫ�ߣ���Ҫ��Cװ�ó��ڴ�����һ��ʢ��ʯ�ҵĸ���װ�á�
��4�����ݰ�����������ˮ�����ʷ�����A��CCl4�����ܽⰱ���������������Ȼ�̼��Һ�ķ����ⶨ���������A����ȷ��B.������������ˮ��������ˮ���ⶨ��B������C.������������ˮ����������NH4Cl��Һ�ķ����ⶨ���������C������D.���������ڱ������������ű���Һ���ⶨ�����������D����ȷ����ѡAD
��5����m g��Ʒ��ȫ��Ӧ�����������������ΪV mL����ת��Ϊ��״����
AlN+NaOH+H2O�TNaAlO2+NH3��
41 22.4L
X V��10-3L
X=41V��10-3/22.4 ��AlN����������=41V/22400m��100%��
��6����������ɵij�����������������ƫ��������Һ��ͨ�����������̼���巴Ӧ���ɣ���Ӧ�����ӷ���ʽΪCO2+ AlO2+ 2H2O=HCO3 + Al(OH)3 ��
��7�����ڲ������δϴ�ӣ�������ϴ�ӵõ��������������ⶨ�����ƫ�ߡ�


 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д� â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Թ��ȸʯ[��Ҫ�ɷ�Ϊ CuCO3��Cu(OH)2��CuSiO3��2H2O�� ��SiO2��FeCO3��Fe2O3������]Ϊԭ���Ʊ�CuCl2�Ĺ����������£�

��֪�� SOCl2��H2O![]() SO2����2HCl��
SO2����2HCl��
��1�� �������ʱ������ CuCO3��Cu(OH)2 ��Ӧ�Ļ�ѧ����ʽΪ ________________�� Ϊ����������ʱͭԪ�صĽ����ʣ����Բ�ȡ�Ĵ�ʩ�У����ʵ��������Ũ�ȣ����ʵ���߷�Ӧ�¶ȣ���______________��
��2�� ��������ʱ������Ӧ�����ӷ���ʽΪ__________________��
��3�� ������ 2������Ҫ�ɷ�Ϊ_______(�ѧʽ)������pH��ʱ��pH ���ܹ��ߣ���ԭ����___________��
��4�� ��������ˮ��ʱ�� ���� SOCl2��Ŀ����_____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ���������ڱ��е�λ�ã��û�ѧ����ش��������⣺
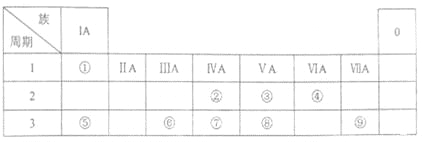
��1������ԭ�ӽṹʾ��ͼΪ ��
��2��������̬�⻯����ӵĽṹʽΪ ��������������ˮ����ķ���ʽ ��
��3������������ۺ������������ǿ������˳���� �����ѧʽ��
��4��������Ԫ�صĽ�����ǿ������ ��������������������С��������������
��5�������������γɵļ����Ӱ뾶���� ��������������������С��������������
��6������������Ԫ�ؿ��γɼȺ����Ӽ��ֺ����ۼ��Ļ����д�����ĵ���ʽ ��
��7������������������������Ӧˮ�����������ܷ�Ӧ��д���䷴Ӧ�����ӷ���ʽ�� �� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ����ʯī���缫�ĵ����У��׳���Ϊ500 mL��ijһ���ʵ���ɫ��Һ���ҳ���Ϊ500 mLϡ���ᣬ�պ�K1���Ͽ�K2���е�⣬�۲쵽A�缫�����к�ɫ�Ĺ�̬�������ɣ�B�缫����ɫ�������ɣ�����Һ�е�ԭ��������ȫ��������ֹͣ��⣬ȡ��A�缫��ϴ�ӡ�����������缫��������1.6 g����ش��������⣺

��1���������У��ҳ�C�缫������Ӧ�ĵ缫��ӦʽΪ______________________��
��2���׳ص��ʱ��Ӧ�����ӷ���ʽ__________________��
��3���׳ص�����Һ��pH��__________��Ҫʹ������Һ�ָ������ǰ��״̬���������________��������Ϊ________g��(������ǰ����Һ���������)
��4���������ٽ�K1�Ͽ����պ�K2��������ָ�뷢��ƫת����D�缫������Ӧ�ĵ缫��Ӧʽ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ӽ���Ĥ�������ӽ���Ĥ��ʯī�缫����ͼZ99��ʾ���ۡ����ȼҵ�е����ӽ�������ԭ�����ɵ��Na2SO4��Һ����NaOH��H2SO4��Һ��

����˵����ȷ����( )
A��������ӦʽΪ2H����2e��===H2��
B����A�ڳ�������H2SO4��Һ
C��a�������ӽ���Ĥ������H��ͨ��
D��Na2SO4��Һ��E�ڼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҩ�ǰѲ�ȫ�ݽ���������ע�䣬������ѹ���������������������á��л���M����ҩ�ǰѲݵijɷ�֮һ����ṹ����ͼ��ʾ��������������ȷ����( )

A��M�Ƿ����廯������ķ���ʽΪC9H6O4
B��1 mol M�������3 mol Br2������Ӧ
C��1 mol M������뺬��3 mol NaOH����Һ������Ӧ
D����һ�������£�M�ܷ���ȡ�����ӳɡ�ˮ�⡢�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������л�Ϊͬϵ�����
A��CH��CH��CH2��CH��CH=CH2
B��CH3��CH=CH2��CH3��CH2��CH=CH2
C��CH3��CH3��CH3��CH=CH2
D��CH2= CH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����õ�ⷨ�ɽ�����Fe��Zn��Ag��Pt�������Ĵ�ͭ�ᴿ������������ȷ����
A�����ʱ�Ծ�ͭ������
B�����ʱ��������������Ӧ
C����ͭ���ӵ�Դ��������缫��Ӧ��Cu=Cu2++2e-
D�������۵ײ����γɺ�����Ag��Pt�Ƚ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ɱ��ۻ�������ʱ�����и����з����仯���ǣ� ��
A.�����ڻ�ѧ�� B.���Ӽ���� C.���ӹ��� D.���Ӽ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com