
����Ŀ������������ѧ��Ӧ��ƽ�ⳣ����K1��K2��K3�����¶ȵĹ�ϵ�ֱ����±���ʾ��
��ѧ��Ӧ | ƽ�ⳣ�� | �¶� | |
973K | 1173K | ||
��Fe��s��+CO2��g�� | K1 | 1.47 | 2.15 |
��Fe��s��+H2O��g�� | K2 | 2.38 | 1.67 |
��CO��g��+H2O��g�� | K3 | �� | �� |
������˵����ȷ����
A����H1��0����H2��0
B����Ӧ�٢ڢ��ķ�Ӧ�������ϵ����H2����H1����H3
C����Ӧ�٢ڢ���ƽ�ⳣ�������ϵ��K1��K2��K3
D��Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ���´�ʩ
���𰸡�B
�����������������A����Ӧ���¶����ߣ�Kֵ������Ӧ���ȣ���H1��0����Ӧ���¶����ߣ�Kֵ��С����Ӧ���ȣ���H2��0����A����B�����ݸ�˹���ɿɵã�������������������H2����H1����H3����B��ȷ��C��K1��![]() ��K2��
��K2��![]() ��K3��
��K3��![]() ������K2��K1��K3����C����D������K2��K1��K3����֪��Ӧ����973Kʱ��Kֵ��1173Kʱ��Kֵ���¶����ߣ�Kֵ��С����Ӧ���ȣ�����Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ���´�ʩ����D����ѡB��
������K2��K1��K3����C����D������K2��K1��K3����֪��Ӧ����973Kʱ��Kֵ��1173Kʱ��Kֵ���¶����ߣ�Kֵ��С����Ӧ���ȣ�����Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ���´�ʩ����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�Ϊԭ��������������Ķ�����Ԫ��A~F�ĵ�һ��������������ݣ����еĽ���Ԫ����
������I��ev�� | A | B | C | D | E | F |
I1 | 5.2 | 7.6 | 6.0 | 11.3 | 13.6 | 14.5 |
I2 | 49.3 | 15.0 | 18.8 | 24.4 | 35.1 | 29.6 |
I3 | 71.6 | 80.1 | 28.4 | 47.9 | 54.9 | 47.4 |
I4 | 98.9 | 109.2 | 112.0 | 64.5 | 77.4 | 77.5 |
I5 | 138.3 | 141.3 | 153.7 | 392.1 | 113.9 | 97.9 |
A.A B CB.B C DC.C D ED.D E F
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽����ʯ��ƷA����������Ԫ�أ�����ɺ����ʣ���Ʋ��������ʵ�飺

��֪��ҺD��ֻ��һ�ֽ��������ӣ������۳�ַ�Ӧ�������������14 g��
��ش�
(1)��ƷA�Ļ�ѧʽΪ________________��
(2)д������c����ˮ��Ӧ�����ӷ���ʽ___________________��
(3)д����ƷA�����ᷢ��������ԭ��Ӧ�Ļ�ѧ����ʽ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ڱ���˵����ȷ���ǣ� ��
A.ͬһ����Ԫ��ԭ�ӵ�������������ͬ
B.ͬһ����Ԫ��ԭ�ӵĵ��Ӳ�����ͬ
C.�����ɼ�Ľ������ڵڢ�A��
D.����������8��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�д��ڵ���ƽ��CH3COOH![]() H++CH3COO��������������ȷ������ ��
H++CH3COO��������������ȷ������ ��
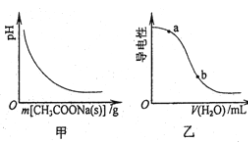
A��ͼ�ױ�ʾ��CH3COOH��Һ������CH3COONa�������ҺpH�ı仯
B��ͼ�ұ�ʾ��CH3COOH��Һ�м�ˮʱ��Һ�ĵ����Ա仯����CH3COOH��Һ��pH��a>b
C��������Һ������Ũ�ȵĹ�ϵ���㣺c��H+����c��OH����+c��CH3COO����
D��0.10mol��L��1��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��OH������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2Fe3++SO32��+H2O![]() 2Fe2++SO42��+2H+����ͼ��ʾ��һ�绯ѧʵ��װ�ã�ͼ��C��D��Ϊ���缫��UΪ���ţ�G�����������ƣ���ָ������ƫ���Դ������A����ΪFeCl3��Һ��B����ΪNa2SO3��Һ�����¹��ڸ�װ�õ�˵���������
2Fe2++SO42��+2H+����ͼ��ʾ��һ�绯ѧʵ��װ�ã�ͼ��C��D��Ϊ���缫��UΪ���ţ�G�����������ƣ���ָ������ƫ���Դ������A����ΪFeCl3��Һ��B����ΪNa2SO3��Һ�����¹��ڸ�װ�õ�˵���������

A��G��ָ��ָ��B��
B��U����������A���ƶ�
C��һ��ʱ���ѧ��Ӧ�ﵽƽ��״̬������������ͨ��
D��һ��ʱ���B����ҺpH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ZrO2�������մɲ��ϣ������Ӣɰ����Ҫ�ɷ�ΪZrSiO4��Ҳ�ɱ�ʾΪZrO2��SiO2����������Fe2O3��Al2O3��SiO2�����ʣ�ͨ�����·�����ȡ��

��֪����ZrO2�����ռӦ���ɿ�����ˮ��Na2ZrO3��Na2ZrO3���ᷴӦ����ZrO2+��
�����ֽ���������ʵ�������¿�ʼ��������ȫ������pH���±���
�������� | Fe3+ | Al3+ | ZrO2+ |
��ʼ����ʱpH | 1.9 | 3.3 | 6.2 |
������ȫʱpH | 3.2 | 5.2 | 8.0 |
��1������ʱZrSiO4������Ӧ�Ļ�ѧ����ʽΪ ������I�Ļ�ѧʽΪ ��
��2��Ϊʹ��ҺI���������ӳ�����ȫ�����ð�ˮ��pH=a����a�ķ�Χ�� �������Ӱ�ˮ��pH=bʱ����������Ӧ�����ӷ���ʽΪ ��
��3�������III������Һ�м���CaCO3��ĩ�����ȣ��õ��������塣�÷�Ӧ�����ӷ���ʽΪ ��
��4��Ϊ�õ�������ZrO2��Zr��OH��4��Ҫϴ�ӣ�����Zr��OH��4�Ƿ�ϴ�Ӹɾ��ķ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ��Ը�����(��Ҫ�ɷ�Ϊ�Ǹ�������FeCr2O4������Al2O3��SiO2������)Ϊ��Ҫԭ�������췯��(Na2Cr2O7)��ijʵ��С��ģ������������ͼ��ʾ��
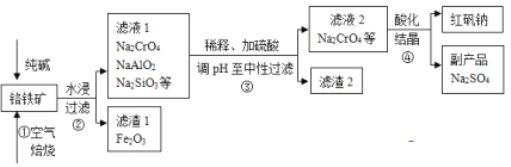
(1)������У�����ʱ���õ���������Ӧѡ��_________(������������������������ʯӢ����)��ѡ�øò��ʵ�ԭ����(��ϻ�ѧ����ʽ����)�� _____________________________________________��
(2)��ƽ���������Ҫ��Ӧ��
____FeCr2O4��___O2��___Na2CO3![]() ___Fe2O3��___Na2CrO4��___CO2 _____________
___Fe2O3��___Na2CrO4��___CO2 _____________
(3)�������У��ữʱ��CrO42�� (��ɫ)ת��ΪCr2O72��(��ɫ)��д��ƽ��ת�������ӷ���ʽ��____________________________________________________________���ú췯����Һ��������ʵ�飺
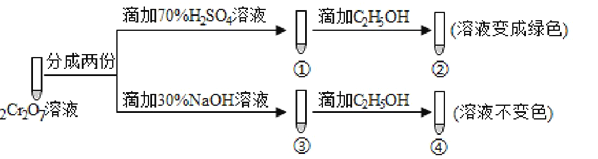
ʵ������У�������Һ��ɫ���������Һ��ƣ��ԱȢںܿ͢ɵó����ۣ�___________________��
(4)����������Ὣ��Һ��pH�������ԣ�������������Ҫ�ɷ���__________��____________��
(5)��ͼ��Na2Cr2O7��2H2O��Na2SO4���ܽ�����ߣ�������л�ù�̬����ƷNa2SO4��ʵ���������Ϊ____________��___________��

(6)ij�������õ�ⷨ����������ˮ�����������������������������ʢ�ź�����ˮ��ԭ��ʾ��ͼ���ϣ���������������ܽ⣬���ռ���H213.44L(��״����)ʱ�� ____________mol Cr2O72-����ԭ��һ��ʱ������Fe(OH)3��Cr(OH)3��������������Һ��c(Cr3+)=3.0��10��5mol��L��1����c(Fe3+)=_________��(��֪Ksp[Fe(OH)3]=4.0��10��38mol��L��1��Ksp[Cr(OH)3]=6.0��10��31mol��L��1)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��̬ԭ�ӵ�3d�ܼ�����һ�����ӣ�������ĵ��Ӳ��еĵ�����Ϊ�� ��
A.0B.2C.3D.8
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com