
【题目】氧元素形成的单质在环境、生命活动、生产、科研等方面有重要作用。
(1)氟利昂在紫外线的作用下能产生氯原子,氯原子对臭氧层有破坏作用。氯原子对臭氧层的破坏作用可用如下过程表示:Cl+O3![]() ClO+O2、O3
ClO+O2、O3![]() O2+O、ClO+O
O2+O、ClO+O![]() Cl+O2。这一过程总的化学方程式是______________________________。根据总反应的化学方程式,可知氯原子在反应中作________________________。
Cl+O2。这一过程总的化学方程式是______________________________。根据总反应的化学方程式,可知氯原子在反应中作________________________。
(2)意大利科学家使用普通氧分子和带正电的氧离子制出了新型的氧分子O4,它可能具有与S4相似的长方形结构。O4的摩尔质量为______;相同质量的O2、O3、O4的分子数之比为______,原子数之比为______;下列有关O4的说法不正确的是______(填序号)。
A.题述中生成O4的反应不属于化学变化
B.O4与O2、O3都是氧的同素异形体
C.O2可能具有很强的氧化性
【答案】2O3![]() 3O2 催化剂 64g/mol 6:4:3 1:1:1 A
3O2 催化剂 64g/mol 6:4:3 1:1:1 A
【解析】
(1)根据三个方程式,氯原子在反应前后质量和性质都没有改变,Cl作催化剂,反应条件为光照。
(2)O4由4个氧原子构成;相同质量的O2、O3、O4的分子数之比=![]() :
:![]() :
:![]() 。
。
(1)根据三个方程式,氯原子在反应前后质量和性质都没有改变,Cl作催化剂,反应条件为光照,三个方程式相加得总反应的化学方程式:2O3![]() 3O2。
3O2。
(2)O4由4个氧原子构成,其摩尔质量为16×4=64g/mol;相同质量的O2、O3、O4的分子数之比=![]() :
:![]() :
:![]() =6:4:3;原子个数之比=
=6:4:3;原子个数之比=![]() ×2:
×2:![]() ×3:
×3:![]() ×4=1:1:1;由O2制备O4,有化学键的断裂和形成,发生的是化学变化,O4与O2、O3都是由氧元素形成的不同性质的单质,属于同素异形体,均具有氧化性,答案为A。
×4=1:1:1;由O2制备O4,有化学键的断裂和形成,发生的是化学变化,O4与O2、O3都是由氧元素形成的不同性质的单质,属于同素异形体,均具有氧化性,答案为A。


科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,下图是扇形元素周期表的一部分,对照中学化学常见长式元素周期表,回答下列问题:
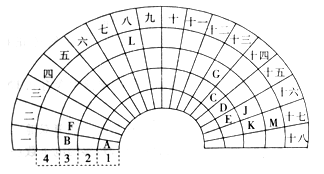
(1)元素C的最高价氧化物的电子式为____;元素G的离子结构示意图为____。
(2)元素L位于周期表的第_________族,1mol/L LM2溶液500mL与0.4 mol K单质恰好完全反应的离子方程式为_______________________________________。
(3)化合物X是由B、E、G三种元素组成,其水溶液呈_____性,原因是____________(用离子方程式表示)。
(4)D和G组成的化合物GD,被大量用于制造电子元件。工业上用G的氧化物、C单质和D单质在高温下制备GD,其中G的氧化物和C单质的物质的量之比为1:3,则该反应的化学方程式为___________。
(5)制取粗硅的过程中,SiO是反应中间产物,隔绝空气时SiO和NaOH溶液反应(产物之一是硅酸钠)的化学方程式______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物既是可导致酸雨的物质,也是造成空气污染的重要物质,加大对氮的氧化物的治理是环境保护重要举措。
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式: _____________________________,该反应中氧化剂是_________,还原剂是________________________________________。
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成对大气无污染的气体,该反应的化学方程式为___________________________________。
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH===2NaNO2+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
现有VL某NaOH溶液能完全吸收nmol NO2和mmol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为_________ mol·L-1。
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=_________。
③用含n和m的代数式表示所得溶液中NO3-和NO2-浓度的比值c(NO3-)∶c(NO2-)=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V 1 mL 0.1mol·L-1的Fe2(SO4)3溶液与2mL 0.1mol·L-1KI溶液混合,待充分反应后,下列方法可证明该反应具有一定限度的是( )
A.若V1<1,加入淀粉B.若V1≤1,加入KSCN溶液
C.若V1≥1,加入AgNO3溶液D.加入Ba(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示,下列说法错误的是( )
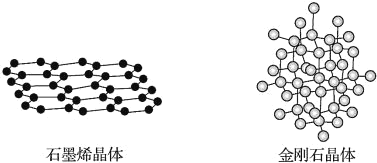
A.在石墨烯晶体中,每个C原子连接3个六元环
B.石墨烯晶体中的化学键全部是碳碳单键
C.在金刚石晶体中,C原子采用sp3杂化
D.在金刚石晶体中,六元环中最多有4个C原子在同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如右图所示。下列说法正确的是( )
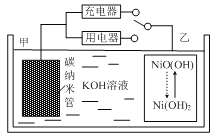
A.放电时,甲电极为正极,OH-移向乙电极
B.放电时,乙电极反应为Ni(OH)2+OH--e-=NiO(OH)+H2O
C.充电时,电池的甲电极与直流电源的正极相连
D.电池总反应为H2+2NiOOH![]() 2Ni(OH)2
2Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g·100 mL-1)。
Ⅰ.实验步骤
(1)配制待测白醋溶液,用____(填仪器名称)量取10.00 mL食用白醋,在____(填仪器名称)中用水稀释后转移到100 mL____(填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)量取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴____作指示剂。
(3)读取盛装0.1000 mol/L NaOH溶液的碱式滴定管的初始读数。
(4)滴定。判断滴定终点的现象是____,达到滴定终点,停止滴定,并记录NaOH溶液的最终读数,重复滴定3~4次。
(5)如图是某次滴定时的滴定管中的液面,其读数为____mL。
![]()
Ⅱ.实验记录
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(6)按正确数据处理,得出c(市售白醋)=____mol/L,市售白醋总酸量=____g·100 mL-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期表,完成下列问题。
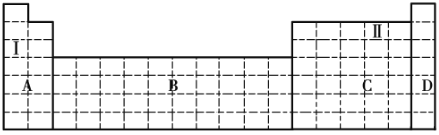
(1)在元素周期表中全部是金属元素的区域为____________(填序号)。
a.A b.B c.C d.D
(2)Ⅰ和Ⅱ元素形成的化合物的化学式为__________________。
(3)现有甲、乙两种短周期元素,室温下,甲元素的单质在冷的浓硫酸或空气中表面都会生成致密的氧化膜,乙元素原子核外第三层与第一层上的电子数相等。
①将甲、乙两元素的元素符号填写在上面元素周期表中对应的位置__________。
②甲、乙两元素中,金属性较强的是__________(填元素名称),可以验证该结论的实验是_______________(填序号)。
a.将在空气中放置已久的这两种元素的单质分别放入热水中
b.将这两种元素的单质粉末分别和相同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素。Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子总数与X、W原子的电子总数之比为5:4。下列说法正确的是( )
A.原子半径:W>Z>Y>X
B.Y的简单气态氢化物的热稳定性比Z的强
C.由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应
D.由X、Y、Z三种元素组成的化合物可以是酸、碱或盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com