
【题目】(1)某块光卤石(KCl·MgCl2·6H2O)中含5.3250 Cl-,则该光卤石的物质的量为_________mol
(2)0.15molH2SO4的质量是___________g,能和___________mol NaOH完全反应,该硫酸所含氢元素的质量与__________mol H2PO4或标准状况下__________L HCl中所含氢元素的质量相同。
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-离子,则ACl2的摩尔质量是_________;ACl2的化学式是____________。
(4) 0.3 mol的氧气和0.22 mol的臭氧(O3),它们的质量______________,它们所含的分子数__________,原子数__________,(以上三空填“相等”或“不相等”)它们的体积比(同温、同压)是__________。
(5)己知在标况下的四种气体①6.72LCH4 ②3.01×1023个HCl分子 ③13.6克H2S ④0.2molNH3用相应的序号填写下列空白
体积最大的是__________;质量最小的是__________;含氢原子数最多的是__________。
【答案】(1)0.05 (2)14.7、0.3、0.1、6.72 (3)95g/mol、MgCl2
(4)相等、不相等、相等、3∶2(5) ②④①
【解析】
试题分析:(1)KClMgCl26H2O~3Cl
1mol 3×35.5g
n 5.3250g
n=![]() =0.05mol;
=0.05mol;
(2)0.5mol H2SO4 的质量=0.5mol×98g/mol=49g;硫酸与NaOH按物质的量之比1:2反应,消耗NaOH的物质的量=2×0.5mol=1mol;每个H2SO4分子含有2个H原子,则n(H)=2n(H2SO4 )=2×0.5mol=1mol,含有氢元素质量相等,则H原子物质的量相等,则n(H3PO4)=1/3×1mol=1/3mol,n(HCl)=1mol,V(HCl)=1mol×22.4L/mol=22.4L;
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的物质的量为0.4mol/2=0.2mol,ACl2的摩尔质量是19g/0.2mol=95gmol-1,则A的相对原子质量为95-35.5×2=24,该二价金属氯化物的化学式为MgCl2;
(4)根据m=nM可知,0.3molO2与0.2molO3的质量都为9.6g,故两者的质量相等,根据N=nNA可知,0.3molO2与0.2molO3所含的分子数分别为0.3NA,0.2NA,则分子数不等,0.3mol的氧气和0.2mol的臭氧(O3),原子数都是0.6mol,根据V=nVm可知,同温同压的体积之比等于物质的量之比,所以体积之为3:2;
(5)①6.72L CH4的物质的量为![]() =0.3mol,质量为0.3mol×16g/mol=4.8g,含有H原子物质的量为0.3mol×4=1.2mol;②3.01×1023个HCl分子物质的量为
=0.3mol,质量为0.3mol×16g/mol=4.8g,含有H原子物质的量为0.3mol×4=1.2mol;②3.01×1023个HCl分子物质的量为![]() =0.5mol,质量为0.5mol×36.5g/mol=18.25g,含有H原子物质的量为0.5mol×1=0.5mol;③13.6克H2S 的物质的量为
=0.5mol,质量为0.5mol×36.5g/mol=18.25g,含有H原子物质的量为0.5mol×1=0.5mol;③13.6克H2S 的物质的量为![]() =0.4mol,含有H原子物质的量为0.4mol×2=0.8mol;④0.2molNH3的质量为0.2mol×17g/mol=3.4g,含有H原子物质的量为0.2mol×3=0.6mol;相同条件下,气体的体积之比等于物质的量之比,体积最大的是②,质量最小的是④,含氢原子数最多的是①。
=0.4mol,含有H原子物质的量为0.4mol×2=0.8mol;④0.2molNH3的质量为0.2mol×17g/mol=3.4g,含有H原子物质的量为0.2mol×3=0.6mol;相同条件下,气体的体积之比等于物质的量之比,体积最大的是②,质量最小的是④,含氢原子数最多的是①。


科目:高中化学 来源: 题型:
【题目】一定条件下,向一带活塞的密闭容器中充入2molSO2在一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,下列反应:2SO2(g)+O2(g)![]() 2SO3(g),达到平衡后改变下述条件,SO3气体平衡浓度不改变的是( )
2SO3(g),达到平衡后改变下述条件,SO3气体平衡浓度不改变的是( )
A.保持温度和容器体积不变,充入1molSO2(g)
B.保持温度和容器内压强不变,充入1molSO3(g)
C.保持温度和容器内压强不变,充入1molO2(g)
D.保持温度和容器内压强不变,充入1molAr(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,加“碘”食盐中较少使用碘化钾,因其口感苦涩且在贮藏和运输中易变化,目前代之加入是
A. I2 B. KIO C. NaIO D. KIO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)把NaHCO3和Na2CO3·10H2O混合物6.56g溶于水制成100ml溶液,测得溶液中c(Na+)=0.5mol/L。
向该溶液中加入盐酸至不再产生气体为止,将溶液蒸干后,所得固体质量为___________。
(2)将24.0g氢氧化钠固体放入水中,要使100个水分子中就含有一个Na+离子,所需水的质量为_________________。
(3)现有HNO3和NaNO3的混合溶液200mL,其中 HNO3和NaNO3的物质的量浓度均为1mol/L.若要使 HNO3和NaNO3 的物质的量浓度分别为2mol/L 和0.2mol/L,则须加入63%的浓硝酸(密度为1.2g/cm3)___________mL,再加入蒸馏水稀释至_______毫升才能实现。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O, 电池示意如图,下列说法正确的是( )

A.A处通氧气,B处通乙醇
B.电池工作时电子由a极沿导线经灯泡再到b极
C.电池正极的电极反应为:O2+2H2O+4e-=4OH-
D.若用这种电池作电源保护金属铁,则a电极连接石墨,b连接铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的三种钠盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
A. HX、HZ、HY B. HZ、HY、HX
C. HX、HY、HZ D. HY、HZ、HX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是1 L“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(g ·mol-1) |
蔗糖 | 50.00 | 342 |
硫酸钾 | 0.50 | 174 |
阿司匹林 | 0.35 | 180 |
高锰酸钾 | 0.50 | 158 |
硝酸银 | 0.04 | 170 |
⑴下列“鲜花保鲜剂”的成分中,属于非电解质的是 。
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
⑵“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为 mol.L-1。(只要求写表达式,不需要计算)
⑶配制上述1 L“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、 、 、 。(在横线上填写所缺仪器的名称)
⑷在溶液配制过程中,下列操作正确且对配制结果没有影响的是 。
A.将药品放入容量瓶中加蒸馏水溶解
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.60 g铁投入100 mL某浓度的盐酸中,铁和盐酸恰好完全反应。
求:(1)5.60 g铁的物质的量
(2)所用盐酸中HCl中的物质的量浓度
(3)反应中生成的H2在标准状况下的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减少环境污染,某工厂生产玻璃与处理窑炉气的工艺流程如下:
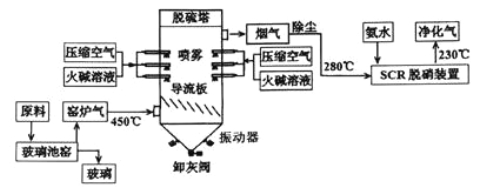
(1)生产普通玻璃、普通硅酸盐水泥和高炉炼铁都要用到的原料是________(填化学式),该物质在制玻璃过程中参与的化学方程式是_______________。
(2)生产玻璃中产生的窑炉气除SO2和氮氧化物外主要还有_________。
(3)窑炉气中的SO2一部分来源于原料中添加剂Na2SO4的热分解,该反应方程式为___________;
(4)在“脱硫塔”中喷洒火碱而不用石灰水的原因是___________;在进入“SCR脱硝装置”的烟气要先除尘的原因是_________________。
(5)烟气脱硝可采用氨水(NH3·H2O)脱除烟气的NO,其原理如图:

该脱硝原理中,NO最终转化为____________(填化学式)。当消耗1molNH3和0.25molO2时,除去的NO在标准状况下的体积为_____________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com