
【题目】下列对实验装置图、实验操作及结论描述正确的是

A.打开弹簧夹,由漏斗中加水至产生液面差,液面高度差不变时,说明装置气密性良好
B.打开弹簧夹一段时间后,红墨水倒吸入导气管中,说明铁钉发生了析氢腐蚀
C.滴入浓硫酸后一段时间,高锰酸钾溶液褪色,说明产生了还原性气体
D.加热片刻后高锰酸钾溶液褪色,说明石蜡油分解产生了乙烯
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】生活处处有化学。下列说法正确的是
A. 制饭勺、饭盒、高压锅等的不锈钢是合金
B. 做衣服的棉和麻均与淀粉互为同分异构体
C. 煎炸食物的花生油和牛油都是可皂化的饱和酯类
D. 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某短周期元素X,其原子的电子层数为n,最外层电子数为2n+1。下列有关元素X的说法错误的是
A. 元素X不可能是金属元素
B. 元素X的气态氢化物不一定是电解质
C. 元素X —定能形成化学式为KXO3的含氧酸钾盐
D. 工业上制取X的单质时一定采用氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2:约45%,Fe2O3:约40%,Al2O3:约10%,MgO:约5%.目前我国已经在技术上取得突破--用硫酸渣炼铁.Fe3+开始沉淀为氢氧化物的PH=1,沉淀完全时的PH为3.7.
I.某探究性学习小组的同学设计了不同的方案,用化学基本知识进行金属元素的提取实验。
方案一:
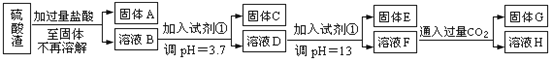
请回答:
(1)写出固体E的化学式:______________.试剂①是__________(填选项字母).
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(2)若要准确测定溶液的pH是否达到3.7,下列物品中可供使用的是__________(填选项字母).
A.石蕊试液 B.广泛pH试纸 C.pH计
(3)溶液H中溶质的化学式:______________
(4)要将固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为________________.
方案二:
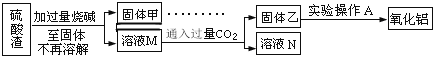
(5)此方案制得的氧化铝含有的主要杂质是_________________。
(6)写出由溶液M→固体乙这个过程中,主要化学反应的离子方程式:_______________;_______________。
(7)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:_______________。
(8)某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用1.000×10-2molL-1KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液10.00mL,则残留物中铁元素的质量分数是_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.25g·mL-1,质量分数为36.5%的浓盐酸配制成240mL 0.1mol/L的稀盐酸,请回答:
(1)浓盐酸的物质的量浓度为________mol/L
(2)配制240mL 0.1mol/L的稀盐酸,应选择_________mL的容量瓶,量取浓盐酸的体积为________ml。
(3)完成本实验必需用到的仪器有:量筒、玻璃棒、烧杯、________、容量瓶等
(4)定容时,加水超过了刻度线,应怎样操作:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列说法不正确的是
A.常温常压下,28gCO和N2混合气体中含有的原子总数为2![]()
B.标准状况下,11.2L的水中含有水分子0.5NA
C.2molOH-中电子数为20NA
D.0.1molFeCl3形成Fe(OH)3胶体,Fe(OH)3胶粒的数目小于0.1![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中两个化学反应属于同一反应类型的是( )
A. 由乙烯制 1,2-二溴乙烷;由乙烷制一氯乙烷
B. 由苯制溴苯;由乙醇与乙酸反应制乙酸乙酯
C. 乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色
D. 由苯制硝基苯;由苯制环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼和铝位于同一主族,它们可以形成许多组成和性质类似的化合物。一种用硼镁矿(Mg2B2O5·H2O)制取单质硼的工艺流程图如下:
回答下列问题:
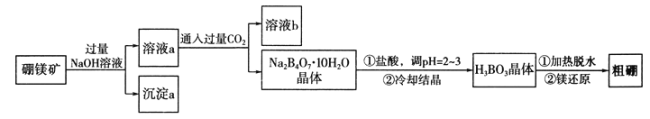
(1)Mg2B2O5·H2O中B的化合价为____________。
(2)溶液b中溶质的化学式为______________________。
(3)用pH试纸测溶液pH的操作方法是________________________。
(4)写出Na2B4O7·10H2O与盐酸反应的化学方程式:_____________________。
(5)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.0200 g粗硼制成的BI3完全分解,生成的I2用0.3000 mo1·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液15.00 mL。(已知:I2+2S2O32-=2I-+S4O62-)
①滴定操作中指示剂通常为______________。
②该粗硼样品的纯度为___________________。
③若滴定管在使用前未用Na2S2O3标准溶液润洗,测得样品的纯度将_________(填“偏高”、“偏低”或“无影响”)。
(6)请仿照上图形式设计从沉淀a中获得单质Mg的流程图(提示:在箭头上方或下方标出所用试剂或实验操作)。
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com