
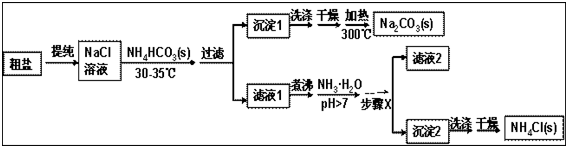
分析 根据题中流程可知,粗盐水提纯后得氯化钠溶液,经蒸发浓缩后,温度控制在30℃~35℃,防止碳酸氢按分解,加入碳酸氢铵,生成沉淀1为碳酸氢钠,滤液1主要为氯化铵,氯化铵溶液中加入氨水,可抑制铵根离子的水解,经过蒸发浓缩、冷却结晶、过滤可得沉淀2为氯化铵固体,经洗涤、干燥得纯净的氯化铵,滤液2中含有少量的氯化铵和碳酸氢钠,
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:①NaOH ②BaCl2③HCl ④Na2CO3,根据前面加入的物质是过量的,在后面加入的物质在除去溶液中原来的杂质外还要将前面加入的试剂杂质除去,据此判断;过滤中用到玻璃棒的作用是引流;
(2)样品中加入适量的氯化钡溶液可判断粗盐中SO42-是否已除尽;
(3)蒸发浓缩时溶液要加热,而NH4HCO3在36℃开始分解,据此答题;
(4)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水;
(5)氨水能抑制铵根离子的水解,同时能使NaHCO3转化为Na2CO3,并补充煮沸时损失的NH3,从氯化铵溶液得到氯化铵固体可以通过蒸发浓缩,冷却结晶,过滤的方法;
(6)由滴定用去的氢氧化钠的物质的量计算出盐酸的物质的量,根据方程式4NH4Cl+6HCHO→(CH2)6N4+4HCl+6H2O,计算出氯化铵的质量,进而计算出样品中氯化铵的质量分数.
解答 解:根据题中流程可知,粗盐水提纯后得氯化钠溶液,经蒸发浓缩后,温度控制在30℃~35℃,防止碳酸氢按分解,加入碳酸氢铵,生成沉淀1为碳酸氢钠,滤液1主要为氯化铵,氯化铵溶液中加入氨水,可抑制铵根离子的水解,经过蒸发浓缩、冷却结晶、过滤可得沉淀2为氯化铵固体,经洗涤、干燥得纯净的氯化铵,滤液2中含有少量的氯化铵和碳酸氢钠,
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:①NaOH ②BaCl2③HCl ④Na2CO3,根据前面加入的物质是过量的,在后面加入的物质在除去溶液中原来的杂质外还要将前面加入的试剂杂质除去,所以加入的顺序为NaOH、BaCl2、Na2CO3、HCl,故选B;过滤中用到玻璃棒的作用是引流,
故答案为:B;引流;
(2)样品中加入适量的氯化钡溶液可判断粗盐中SO42-是否已除尽,具体操作为取少量除杂后的样品于试管中,滴加适量氯化钡溶液,若无白色沉淀产生,则含SO42-已除尽,
故答案为:取少量除杂后的样品于试管中,滴加适量氯化钡溶液,若无白色沉淀产生,则含SO42-已除尽;
(3)蒸发浓缩时溶液要加热,而NH4HCO3在36℃开始分解,所以在加入固体NH4HCO3之前进行蒸发浓缩优于在加入NH4HCO3之后,原因是可避免NH4HCO3的分解,
故答案为:可避免NH4HCO3的分解;
(4)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,反应方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(5)氨水能抑制铵根离子的水解,同时能使NaHCO3转化为Na2CO3,并补充煮沸时损失的NH3,从氯化铵溶液得到氯化铵固体可以通过蒸发浓缩,冷却结晶,过滤的方法,
故答案为:抑制NH4+水解、使NaHCO3转化为Na2CO3、补充煮沸时损失的NH3;蒸发浓缩、冷却结晶、过滤;
(6)根据题意,滴定用去的氢氧化钠的物质的量为0.025L×0.1mol/L=0.0025mol,所以盐酸的物质的量为0.0025mol,根据方程式4NH4Cl+6HCHO→(CH2)6N4+4HCl+6H2O,可知1.5g该样品中氯化铵的质量为0.0025mol×$\frac{100}{10}$×53.5g/mol=1.3375g,所以样品中氯化铵的质量分数为$\frac{1.3375g}{1.5g}$×100%=89.2%,
故答案为:89.2%.
点评 本题考查侯氏制碱法、溶解度、物质的分离提纯、物质含量测定等,题目难度中等,侧重考查学生对流程的分析和基础知识的灵活的应用.


科目:高中化学 来源: 题型:选择题
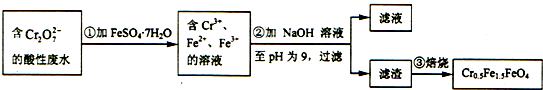
| A. | 根据第①步反应可知还原性:Cr3+大于Fe2+ | |
| B. | 第②步过滤得到的滤渣中主要成分为Cr(OH)3、Fe(OH)2,不含Fe(OH)3 | |
| C. | 欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需要加入27.8g FeSO4•7H2O | |
| D. | 第③步高温焙烧过程用到的主要实验仪器中属于硅酸盐质的有:酒精灯、蒸发皿、泥三角 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.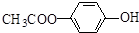 和
和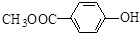 .
.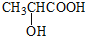 ) 的合成路线:
) 的合成路线: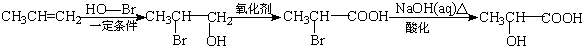 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
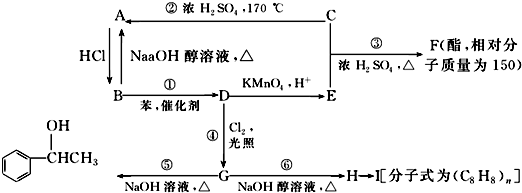
 .
. ;
; .
.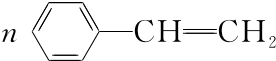 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$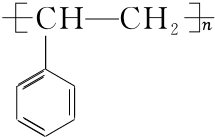 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含一种分子的物质是纯净物,只含一种元素的物质也是纯净物 | |
| B. | 医疗上的血液透析利用了胶体的性质 | |
| C. | NH3溶于水后所得的溶液可以导电,所以NH3为电解质 | |
| D. | 从海水中可以得到NaCl,电解NaCl溶液可制备Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
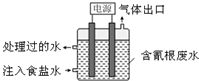 某些工业废水中常是含有氰根(CN-)的无机物,有一定的毒性,有的还是剧毒.图所示装置是工业上采用的电解法除去含CN-废水的装置.工作时控制溶液为碱性,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列叙述不正确的是( )
某些工业废水中常是含有氰根(CN-)的无机物,有一定的毒性,有的还是剧毒.图所示装置是工业上采用的电解法除去含CN-废水的装置.工作时控制溶液为碱性,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列叙述不正确的是( )| A. | 用石墨作阴极,铁作阳极 | |
| B. | 阴极的电极反应式为:2H2O+2e-=H2↑+2OH- | |
| C. | 阳极的电极反应式为:Cl-+2OH--2e-=ClO-+H2O | |
| D. | 除去CN-的反应:2CN-+5ClO-+H2O=N2↑+2CO2↑+5Cl-+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 所有的物质中都含有化学键 | |
| B. | 含有非极性键的化合物不一定是共价化合物 | |
| C. | 反应物总能量低于生成物总能量的反应一定是吸热反应 | |
| D. | 由非金属元素构成的化合物一定是共价化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com