
��ҵ����ƽ�VOSO4�е�K2SO4��SiO2���ʳ�ȥ�����յõ�V2O5���������£�
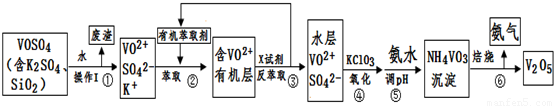
��ش��������⣺
��1����������÷����ijɷ��� ��д��ѧʽ��������I������ ��
��2������ڡ��۵ı仯���̿ɼ�Ϊ����ʽR��ʾVO2+��HA��ʾ�л���ȡ������
R2(SO4)n (ˮ��)+ 2nHA���л��㣩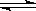 2RAn���л��㣩 + nH2SO4 (ˮ��)
2RAn���л��㣩 + nH2SO4 (ˮ��)
������ȡʱ��������������ԭ���� ������X�Լ�Ϊ ��
��3���ݵ����ӷ���ʽΪ ��
��4��25��ʱ��ȡ����������������õ��������ʺ���ҺpH֮���ϵ���±���
|
pH |
1.3 |
1.4 |
1.5 |
1.6 |
1.7 |
1.8 |
1.9 |
2.0 |
2.1 |
|
��������% |
88.1 |
94.8 |
96.5 |
98.0 |
98.8 |
98.8 |
96.4 |
93.1 |
89.3 |
����ϱ�����ʵ�������У����м��백ˮ��������Һ�����pHΪ ��
����������Ϊ93.1%ʱ������Fe(OH)3����������Һ��c(Fe3+)< ��
����֪��25��ʱ��Ksp[Fe(OH)3]=2.6��10-39��
��5���ù��������У�����ѭ�����õ������� �� ��
��1��SiO2 �����ˣ�2��������к����ᣬ��ʹƽ�������ƶ�����߷�����ȡ�ʣۻ����Ʊ����������RAn���л��㣩��Ũ�ȡ��ٷֺ����ȣݣ�H2SO4��3��NH3��H2O+VO3�� =NH4VO3��+OH��
��4��1.7��1.8����1.7��1.8����һ������2.6��10-3mol��L-1��5����������ˮ�����л���ȡ��
��������
�����������1���ڸ�����������ֻ�ж������費�ܽ���ˮ�����Թ��˵õ���������SiO2 ����2�������ڸ÷�Ӧ�ǿ��ܷ�Ӧ����Ӧ�������ᣬ���������к��ᣬ��С���Ũ�ȡ�������������ԭ������С�������Ũ�ȣ���ʹƽ��������Ӧ�����ƶ����Ӷ���߷�����ȡ�ʡ�������������ʹ������ȡ�ʽ��ͣ����Լ������ᣬ�������������Ũ�ȣ�ʹƽ�������ƶ����Ϳ��ԴﵽĿ�ġ���3�����ӷ���ʽΪNH3��H2O+VO3�� =NH4VO3��+OH����4�����ݱ������ݿɿ�������PHΪ1.7��1.8ʱ����������ߡ�����������Ϊ93.1%ʱPH=2.0��C(H+)=0.01mol/L,C(OH-)=(1��10-14)/0.01=1��10-12mol/L.Ksp[Fe(OH)3]=2.6��10-39��c(Fe3+)��C3(OH-)=2.6��10-3mol��L-1.������ͼ���Կ�����ˮ���л���ȡ������ѭ�����á�
���㣺������������Ի�ѧƽ���Ӱ�켰�ܶȻ������ļ����֪ʶ��


 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д� �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
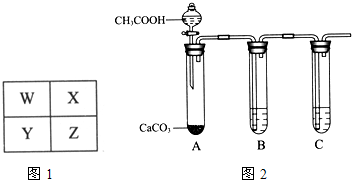 W��X��Y��ZΪ���ֶ���������Ԫ�أ���λ�ù�ϵ��ͼ1��
W��X��Y��ZΪ���ֶ���������Ԫ�أ���λ�ù�ϵ��ͼ1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ������ʡ����У������һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
��ҵ����ƽ�VOSO4�е�K2SO4��SiO2���ʳ�ȥ�����յõ�V2O5������������
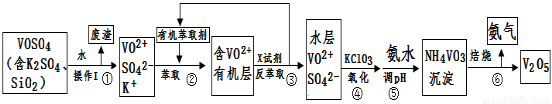
��ش��������⣺
��1�����������÷����ijɷ���??????????? ��д��ѧʽ��������I������?????? ��
��2�������������ı仯���̿ɼ�Ϊ����ʽR��ʾVO2+��HA��ʾ�л���ȡ������
R2(SO4)n (ˮ��)+ 2nHA���л��㣩 2RAn���л��㣩 + nH2SO4 (ˮ��)
2RAn���л��㣩 + nH2SO4 (ˮ��)
������ȡʱ��������������ԭ����???????????????????????????? ��
����X�Լ�Ϊ??????????????????? ��
��3���������ӷ���ʽΪ???????????????????????? ��
��4��25��ʱ��ȡ����������������õ��������ʺ���ҺpH֮���ϵ���±���
pH | 1��3 | 1��4 | 1��5 | 1��6 | 1��7 | 1��8 | 1��9 | 2��0 | 2��1 |
��������% | 88��1 | 94��8 | 96��5 | 98��0 | 98��8 | 98��8 | 96��4 | 93��1 | 89��3 |
�ϱ�����ʵ�������У����м��백ˮ��������Һ�����pHΪ?????????? ��
����������Ϊ93��1%ʱ������Fe(OH)3����������Һ��c(Fe3+)<????????????? ��
(��֪��25��ʱ��Ksp[Fe(OH)3]=2��6��10-39)
��5���ù��������У�����ѭ�����õ�������?????????????? ��??????? ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��ɽ��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��ҵ�ϣ�����ͭ��CuFeS2��ͨ��8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2��Ӧ��ȡͭ����������Ļ����
8Cu+4FeO+2Fe2O3+16SO2��Ӧ��ȡͭ����������Ļ����
��1��������Ӧ�У���ԭ��Ϊ ��
��2����ͭ��ұ��ͭ������¯������Fe2O3��FeO��SiO2��Al2O3�����Ʊ�Fe2O3������Ϊ��
����ϡ�����ȡ¯�������ˡ�
����Һ���������ټ������NaOH��Һ�����ˣ�������ϴ�ӡ�������յ�Fe2O3��
��������Ϣ�ش��������⣺
a��ͨ�������ڣ�¯���е�Al2O3����� ��д���ӣ���
b��ѡ���ṩ���Լ������ʵ����֤¯���к���FeO��
�ṩ���Լ���ϡ���� ϡ���� KSCN��Һ ����KMnO4��Һ NaOH��Һ ��ˮ
��ѡ�Լ�Ϊ ��
֤��¯���к���FeO��ʵ������Ϊ ��
��3��������¯���н��к������IJⶨ�������£�
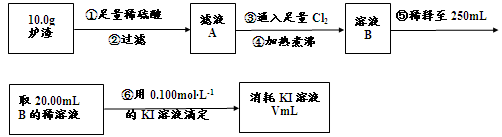
I������۷�����Ӧ�����ӷ���ʽΪ ��
II����������������� ��
III����������õ��IJ����������ձ�������������ͷ�ιܡ� ��
IV�����ζ�����������0.100mol��L−1KI��Һ20.00mL����¯�������İٷֺ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡ��ɽ�и�����ѧ������⣨�������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��ҵ����ƽ�VOSO4�е�K2SO4��SiO2���ʳ�ȥ�����յõ�V2O5���������£�
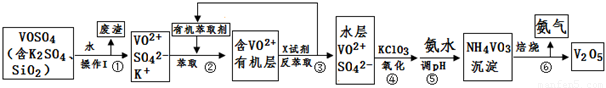
��ش��������⣺
��1����������÷����ijɷ��� ��д��ѧʽ��������I������ ��
��2������ڡ��۵ı仯���̿ɼ�Ϊ����ʽR��ʾVO2+��HA��ʾ�л���ȡ������
R2(SO4)n (ˮ��)+ 2nHA���л��㣩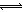 2RAn���л��㣩 + nH2SO4 (ˮ��)
2RAn���л��㣩 + nH2SO4 (ˮ��)
������ȡʱ��������������ԭ���� ��
����X�Լ�Ϊ ��
��3���ݵ����ӷ���ʽΪ ��
��4��25��ʱ��ȡ����������������õ��������ʺ���ҺpH֮���ϵ���±���
|
pH |
1.3 |
1.4 |
1.5 |
1.6 |
1.7 |
1.8 |
1.9 |
2.0 |
2.1 |
|
��������% |
88.1 |
94.8 |
96.5 |
98.0 |
98.8 |
98.8 |
96.4 |
93.1 |
89.3 |
����ϱ�����ʵ�������У����м��백ˮ��������Һ�����pHΪ ������������Ϊ93.1%ʱ������Fe(OH)3����������Һ��c(Fe3+)< ������֪��25��ʱ��Ksp[Fe(OH)3]=2.6��10��39��
��5���ù��������У�����ѭ�����õ������� �� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com