
����Ŀ��������Դ���ѵ�90%����������ѧ������
(1)��ҵ�����һ����Ҫ��Ӧ������CO��ԭH2O(g)����֪��
C(ʯī��s)��O2(g)===CO2(g)����H����394 kJ��mol��1
2C(ʯī��s)��O2(g)===2CO(g)����H����222 kJ��mol��1
H2(g)��![]() O2(g)===H2O(g)����H����242 kJ��mol��1
O2(g)===H2O(g)����H����242 kJ��mol��1
��CO��ԭH2O(g)���Ȼ�ѧ����ʽΪ__________________��
(2)���ܱ���Ϊ��߷�չDZ������ɫ��Դ��д����ʽ����ȼ�ϵ�ع���ʱ�ĸ����缫��Ӧʽ��______________________________________________________________��
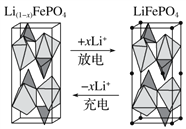
(3)һ����������Ӷ��ε�ء����������(LiFePO4)��ء���Ϊ�������ϵ���������ڳ䡢�ŵ�ʱ�ľֲ��Ŵ�ʾ��ͼ����ͼ��д���õ�س��ʱ�������缫��Ӧʽ��___________��
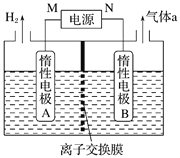
(4)LiOH���Ʊ�����ӵ���������ϵ���Ҫԭ�ϣ����ⷨ�Ʊ�װ������ͼ������aͨ�����KI��Һ�У�������Һ����������һ��ʱ�����ɫ����ȥ����M��Ϊ��Դ��_______(���������)����B�������ҺΪ_______(�ѧʽ)��Һ�������ӽ���Ĥ��_______(�����������)���ӽ���Ĥ��������ɫ��ȥ��ԭ��_________________________________��
���𰸡� CO(g)��H2O(g)===CO2(g) ��H2(g) ��H����41 kJ��mol��1 H2��2e����2OH��===2H2O LiFePO4��xe��===Li(1��x)FePO4��xLi�� �� LiCl �� ���������ɵ�I2��������Ϊ����̬�ĵ�Ļ�����
��������(1)��֪��25��ʱ����C(ʯī)+O2(g)�TCO2(g)��H3=-394kJ/mol����2C(ʯī)+O2(g)=2CO(g)��H2=-222kJ/mol����H2(g)+ ![]() O2(g)�TH2O(g)��H2=-242kJ/mol���ɸ�˹���ɣ���-��-�ڡ�
O2(g)�TH2O(g)��H2=-242kJ/mol���ɸ�˹���ɣ���-��-�ڡ�![]() �ã�CO(g)+H2O(g)�TCO2(g)+H2(g)���ʡ�H=��H3-��H2-��H1=-394kJ/mol-(-242kJ/mol)-(-111kJ/mol)=-41kJ/mol���ʴ�Ϊ��CO(g)+H2O(g)=CO2(g)+H2(g)��H=-41kJ/mol��
�ã�CO(g)+H2O(g)�TCO2(g)+H2(g)���ʡ�H=��H3-��H2-��H1=-394kJ/mol-(-242kJ/mol)-(-111kJ/mol)=-41kJ/mol���ʴ�Ϊ��CO(g)+H2O(g)=CO2(g)+H2(g)��H=-41kJ/mol��
(2)ȼ�ϵ�صĸ�������ȼ������ʧ���ӵ�������Ӧ�����ݵ�����Ǽ��Ի��������Ը����ϵĵ缫��Ӧʽ��H2-2e-+2OH-�T2H2O���ʴ�Ϊ��H2-2e-+2OH-�T2H2O��
(3)���ʱ����������ӦΪ�������缫��ӦʽΪ��LiFePO4-xe-�TLi(1-x)FePO4+xLi+���ʴ�Ϊ��LiFePO4-xe-�TLi(1-x)FePO4+xLi+��
(4)����Ʊ�LiOH�����缫�����Һ�ֱ�ΪLiOH��LiCl��Һ����ͼ��֪�����������������A�������ӷŵ磬��֪AΪ������M�Ǹ�������A���Ʊ�LiOH��Li+��A���������ӽ���Ĥ��B�ƶ������ӽ���Ĥ�������ӽ���Ĥ��B��ΪLiCl��Һ�������ӷŵ�����������Cl2��I2�����ɸ���̬�ĵ�Ļ����������ɫ��ȥ�ʴ�Ϊ������LiCl����������a(Cl2)��I2�����ɸ���̬�ĵ�Ļ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��3.01��1024��OH�������ʵ���Ϊ____������Ϊ___����ЩOH�����״����__L NH3�����ʵ�����ȣ������ЩOH������2L��Ba(OH)2��Һ�����Ba(OH)2�����ʵ���Ũ��Ϊ__��
��2��ͬ��ͬѹͬ����İ�����NH3�������⣨H2S�����������֮��Ϊ___������������֮��Ϊ__����ͬ�����İ�������������ķ�����֮��Ϊ______�ܶ�֮��Ϊ______��
��3�������8.96L ��CH4��CO������壬������Ϊ7.60g����ƽ��Ħ������Ϊ____________��CH4��CO���ʵ���֮��Ϊ________________��
��4����֪100mLAl2(SO4)3��Һ��Al3+ Ũ��Ϊ0.6mol/L����SO42-��Ũ��Ϊ______________��Al2(SO4)3�����ʵ���Ϊ_____________��������Al3+ ˮ�⣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᱡ����P��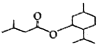 ����һ���������ಡ��ҩ�һ���Ʊ������ᱡ����P���������£�
����һ���������ಡ��ҩ�һ���Ʊ������ᱡ����P���������£�

��֪��
RCH=CH2 ![]() RCH2CHBr��R��ʾ������
RCH2CHBr��R��ʾ������
����������⣺
(1)A�Ļ�ѧ����Ϊ__________��
(2)�Լ�l�Ľṹ��ʽΪ__________��
(3)��E����F�Ļ�ѧ����ʽΪ__________���÷�Ӧ������__________��
(4)�Լ�2������__________�Լ��������ƻ�ѧʽ��
(5)��C��H����P�Ļ�ѧ����ʽΪ__________��
(6)H��ͬ���칹���У��ܷ���ˮ�ⷴӦ����״�����ﹲ��_________�֣������������칹�������к˴Ź������������ַ塢�ҷ�ֵ��Ϊ9:1��ͬ���칹��Ľṹ��ʽΪ__________��
(7)����ϩ��һ����Ҫ�Ļ���ԭ�ϣ��ο��Ʊ������ᱡ�����еķ���������Ա�����ϩΪ�л�ԭ�ϣ����Լ���ѡ�����Ʊ�����ϩ�ĺϳ���·��
�ϳ�·�߳��õı�ʾ����Ϊ��![]()
________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. ij������ʹƷ����Һ��ɫ�����������SO2
B. ��������ͭ��a��b����;����ȫת��Ϊ����ͭ��;��a��b���ĵ�����һ����:
;��a�� ![]()
C. ��ij��Һ�м���Ba(NO3)2��Һ��������ɫ����������ϡ����������ܽ⣬��ԭ��Һ�в�һ����SO![]()
D. ��ij��Һ�м���NaOH�����ȣ�������ʹʪ�����ɫʯ����ֽ�������壬��ԭ��Һ����NH![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��̽��SO2���廹ԭFe3����I2������ʹ�õ�ҩƷ��װ����ͼ��ʾ��
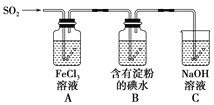
(1)Aװ���з�����Ӧ�����ӷ���ʽΪ_________________________________________��
(2)Bװ���з�����Ӧ�����ӷ���ʽΪ_________________________________________��
(3)����ʵ�鷽����������ʵ������ȡ����SO2����________��
A��Na2SO3��Һ��HNO3 B��Na2SO3������Ũ����
C���������ڴ�����ȼ�� D��ͭ����ŨH2SO4
(4)װ��C��������__________________________________________________��
(5)��Ҫ��A��������Һ��ȡ���壬������е�ʵ��������裺��������ȴ�ᾧ�����ˡ���Ȼ�������һϵ�в�����û���õ���������________(�����)��
A��������B��ʯ��������C��©������D���ձ� E������������F������
(6)������װ����ͨ�������SO2��Ϊ����֤A��SO2��Fe3��������������ԭ��Ӧ������ȡA�е���Һ���ֳ����ݣ������������ʵ�飺
�����٣�����һ����Һ�м�������KMnO4��Һ���Ϻ�ɫ��ȥ��
�����ڣ����ڶ�����Һ�м���KSCN��Һ������죬�ټ������Ƶ���ˮ����Һ��졣
�����ۣ�����������Һ�м�����ϡ�����ữ��BaCl2��������ɫ������
������������������________��ԭ����____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ���Ҳ����ķ�Һ�к���Fe3����Cu2����Ba2����Cl���������ӣ���������з����Է�Һ���д������Ի��ս������Ʊ��Ȼ������Ȼ������塣
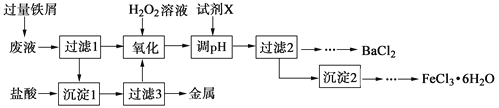
��1������1�к��еĽ��������� ��
��2������ʱ����H2O2��Һ������Ӧ�����ӷ���ʽΪ ��
��3�����������У�������Ϊ�Լ�X���� ������ĸ����
A��BaCl2 | B��BaCO3 | C��NaOH | D��Ba(OH)2 |
��4���������2ϴ���Ƿ���ȫ�ķ����� ��
��5���Ʊ��Ȼ�������������豣�������������Ŀ���� ��
��6���ɹ���2�õ�����Һ�Ʊ�BaCl2��ʵ���������Ϊ ����ȴ�ᾧ�� ��ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ����˵���в���ȷ���� ( )
A. ��ѧ����һ��������
B. ��ѧ������ʹԭ�����ϣ�Ҳ����ʹ��������
C. ��ѧ��Ӧ�����У���Ӧ������ڵĻ�ѧ�����ѣ���������еĻ�ѧ���γ�
D. �Ǽ��Լ����ǻ�ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧ��ӦA2(g)��B2(g)===2AB(g)�������仯��ͼ��ʾ���ж�������������ȷ����(����)
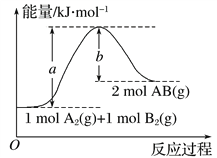
A. ����1 mol A��A��1 mol B��B�����ų�a kJ����
B. ÿ����2 mol AB(g)����b kJ����
C. �÷�Ӧ�з�Ӧ��������������������������
D. �÷�Ӧ�Ȧ�H��(a��b) kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��һ��������N2��H2��Ӧ����NH3����ش�
������Ӧ���������ΪE1���������������ΪE2����E1��E2����÷�ӦΪ________(����ȡ����ȡ�)��Ӧ��
����֪��1 mol H��H����1 mol N��H����1 mol N��N���ֱ���Ҫ��������436 kJ��391 kJ��946 kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ________________��
(2) N2H4��H2O2��Ͽ�������ƽ�������֪��16 gҺ̬N2H4������������Ӧ����N2(g)��H2O(l)���ų�310.6 kJ��������2H2O2(l)===O2(g)��2H2O(l)����H����196.4 kJ��mol��1����ӦN2H4(g)��O2(g)===N2(g)��2H2O(l)�Ħ�H��____________kJ��mol��1��N2H4��H2O2��Ӧ����N2(g)��H2O(l)���Ȼ�ѧ����ʽΪ_______________________________________��
(3)ʵ������50 mL 0.50 mol��L��1������50 mLijŨ�ȵ�NaOH��Һ����ͼ��ʾװ���з�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ���װ�����������ԵĴ�������һ����ȱ��һ�ֲ���������������������Ϊ____________��ʵ�����ṩ��0.50 mol��L��1��0.55 mol��L��1����Ũ�ȵ�NaOH��Һ��Ӧѡ��_____________mol��L��1��NaOH��Һ����ʵ�顣

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com