
【题目】异戊酸薄荷酯P(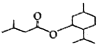 )是一种治疗心脏病的药物。一种制备异戊酸薄荷酯P的流程如下:
)是一种治疗心脏病的药物。一种制备异戊酸薄荷酯P的流程如下:

已知:
RCH=CH2 ![]() RCH2CHBr(R表示烃基)
RCH2CHBr(R表示烃基)
完成下列问题:
(1)A的化学名称为__________。
(2)试剂l的结构简式为__________。
(3)由E生成F的化学方程式为__________;该反应类型是__________。
(4)试剂2可以是__________试剂(填名称或化学式)
(5)由C和H生成P的化学方程式为__________。
(6)H的同分异构体中,能发生水解反应的链状化合物共有_________种(不考虑立体异构);其中核磁共振氢谱有两种峰、且峰值比为9:1的同分异构体的结构简式为__________。
(7)苯乙烯是一种重要的化工原料,参考制备异戊酸薄荷酯中的方法,设计以苯、乙烯为有机原料(无机试剂自选),制备苯乙烯的合成线路:
合成路线常用的表示方法为:![]()
________________________
【答案】 3-甲基苯酚(间-甲基苯酚) CH3CH=CH2 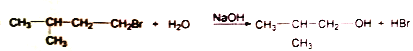 水解反应或取代反应 新制的银氨溶液或新制的氢氧化铜
水解反应或取代反应 新制的银氨溶液或新制的氢氧化铜 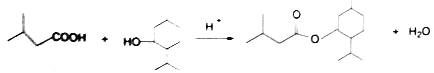 9
9 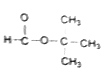
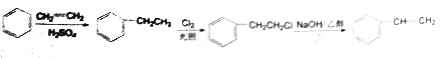
【解析】根据P的结构简式可知C与H发生酯化反应生成P,因此H的结构简式为(CH3)2CHCH2COOH,C的结构简式为![]() ;D与溴化氢发生加成反应生成E,E发生水解反应生成F,F是醇,F发生催化氧化生成G,G发生反应生成H,则G的结构简式为(CH3)2CHCH2CHO,F的结构简式为(CH3)2CHCH2CH2OH,E的结构简式为(CH3)2CHCH2CH2Br,D的结构简式为(CH3)2CHCH=CH2。根据C的结构简式可知A是间-甲基苯酚,依据A和B的分子式结合已知信息可知试剂1是丙烯,与A发生加成反应生成B,B中的苯环与氢气发生加成反应生成C,B的结构简式为
;D与溴化氢发生加成反应生成E,E发生水解反应生成F,F是醇,F发生催化氧化生成G,G发生反应生成H,则G的结构简式为(CH3)2CHCH2CHO,F的结构简式为(CH3)2CHCH2CH2OH,E的结构简式为(CH3)2CHCH2CH2Br,D的结构简式为(CH3)2CHCH=CH2。根据C的结构简式可知A是间-甲基苯酚,依据A和B的分子式结合已知信息可知试剂1是丙烯,与A发生加成反应生成B,B中的苯环与氢气发生加成反应生成C,B的结构简式为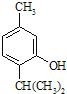 。
。
(1)A的结构简式为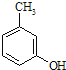 ,化学名称为 3-甲基苯酚。(2)试剂l是丙烯,结构简式为CH3CH=CH2。(3)由E生成F是卤代烃的水解反应,反应的化学方程式为(CH3)2CHCH2CH2Br+NaOH
,化学名称为 3-甲基苯酚。(2)试剂l是丙烯,结构简式为CH3CH=CH2。(3)由E生成F是卤代烃的水解反应,反应的化学方程式为(CH3)2CHCH2CH2Br+NaOH![]() (CH3)2CHCH2CH2OH+NaBr。(4)试剂2把醛基氧化为羧基,可以是新制的银氨溶液或新制的氢氧化铜;(5)由C和H生成P的化学方程式为
(CH3)2CHCH2CH2OH+NaBr。(4)试剂2把醛基氧化为羧基,可以是新制的银氨溶液或新制的氢氧化铜;(5)由C和H生成P的化学方程式为![]() +(CH3)2CHCH2COOH
+(CH3)2CHCH2COOH![]()
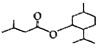 +H2O;(6)H的同分异构体中,能发生水解反应的链状化合物属于酯类,可以是甲酸和丁醇形成的酯类(4种),乙酸和丙醇形成的酯类(2种),丙酸和乙醇形成的酯类(1种),丁酸和甲醇形成的酯类(2种),共有9种(不考虑立体异构);其中核磁共振氢谱有两种峰、且峰值比为9:1的同分异构体的结构简式为HCOOC(CH3)3。(7)根据已知信息结合逆推法可知以苯、乙烯为有机原料(无机试剂自选)制备苯乙烯的合成线路图为
+H2O;(6)H的同分异构体中,能发生水解反应的链状化合物属于酯类,可以是甲酸和丁醇形成的酯类(4种),乙酸和丙醇形成的酯类(2种),丙酸和乙醇形成的酯类(1种),丁酸和甲醇形成的酯类(2种),共有9种(不考虑立体异构);其中核磁共振氢谱有两种峰、且峰值比为9:1的同分异构体的结构简式为HCOOC(CH3)3。(7)根据已知信息结合逆推法可知以苯、乙烯为有机原料(无机试剂自选)制备苯乙烯的合成线路图为![]()
![]()
![]()
![]()
![]()
![]()
![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列是几种原子的基态电子排布,电负性最大的原子是( )
A. 1s22s22p4 B. 1s22s22p63s23p3
C. 1s22s22p63s23p2 D. 1s22s22p63s23p64s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法中,不正确的是( )
A. 干冰可用作致冷剂 B. 在铁制容器表面刷铝粉可防止生锈
C. 氢氧化钠可用作医用胃酸中和剂 D. 过氧化钠可用作供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据元素周期表及元素周期律,下列推断中正确的是
A. 同一周期元素的原子,半径越小越容易失去电子
B. ⅠA族元素的金属性比ⅡA族元素的金属性强
C. 向氢硫酸溶液中滴入氯水有单质硫生成,可以验证硫元素的非金属性比氯元素弱
D. 主族元素的最高正化合价等于该元素原子的核外电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图为元素F、S、Cl在周期表中的位置,关于F、S、Cl的说法正确的是
A.非金属性:F > S > Cl B.原子半径:Cl > S > F
C.稳定性:HF > HCl > H2S D.酸性:HClO4 > H2SO4
He | ||
F | ||
S | Cl | |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
A. HCO3-、NH4+、H+、Cl- B. Al3+、OH-、Na+、Cl-
C. Na+、 H+ 、Fe2+、NO3- D. Mg2+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界能源消费的90%以上依靠化学技术。
(1)工业制氢的一个重要反应是利用CO还原H2O(g)。已知:
C(石墨,s)+O2(g)===CO2(g) ΔH=-394 kJ·mol-1
2C(石墨,s)+O2(g)===2CO(g) ΔH=-222 kJ·mol-1
H2(g)+![]() O2(g)===H2O(g) ΔH=-242 kJ·mol-1
O2(g)===H2O(g) ΔH=-242 kJ·mol-1
则CO还原H2O(g)的热化学方程式为__________________。
(2)氢能被视为最具发展潜力的绿色能源,写出碱式氢氧燃料电池工作时的负极电极反应式:______________________________________________________________。
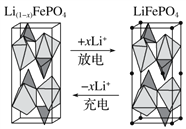
(3)一种新型锂离子二次电池——磷酸铁锂(LiFePO4)电池。作为正极材料的磷酸铁锂在充、放电时的局部放大示意图如下图,写出该电池充电时的阳极电极反应式:___________。
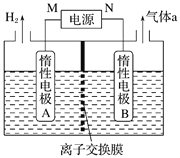
(4)LiOH是制备锂离子电池正极材料的重要原料,其电解法制备装置如下图。气体a通入淀粉KI溶液中,发现溶液变蓝,持续一段时间后,蓝色逐渐褪去。则M极为电源的_______(填“正”或“负”)极,B极区电解液为_______(填化学式)溶液,该离子交换膜是_______(填“阳”或“阴”)离子交换膜,解释蓝色褪去的原因_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g) == 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
(2)C(s)+ O2(g) == CO2(g) △H2=-393.5 kJmol-1
(3)H2(g) +![]() O2(g) == H2O(l) △H3=-285.8kJ·mol-1
O2(g) == H2O(l) △H3=-285.8kJ·mol-1
则反应2C(s)+2H2(g) +O2(g) == CH3COOH(l)的△H为( )
A.-488.3 kJ·mol-1 B.-244.15 kJ·mol-1 C.+488.3 kJ·mol-1 D.+244.15 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com