
【题目】已知反应: MnO2 +4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O。将一定质量的二氧化锰溶解在过量的浓盐酸中,反应一段时间后生成标准状况下氯气4.48 L (假设反应前后溶液体积不变)。试回答下列问题:
MnCl2 + Cl2↑+ 2H2O。将一定质量的二氧化锰溶解在过量的浓盐酸中,反应一段时间后生成标准状况下氯气4.48 L (假设反应前后溶液体积不变)。试回答下列问题:
(1)用单线桥法标明该反应中电子转移的方向和数目:______
MnO2 +4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(2)计算反应消耗的MnO2的质量______ ;
(3)计算被氧化的HCl物质的量______ 。
【答案】 ![]() (浓)
(浓)![]() MnCl2 + Cl2↑+ 2H2O 17.4 g 0.4 mol
MnCl2 + Cl2↑+ 2H2O 17.4 g 0.4 mol
【解析】(1). 在MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中,Mn元素的化合价从MnO2中的+4价降低到MnCl2中的+2价,得到2个电子,Cl元素的化合价从HCl中的-1价升高到Cl2中的0价,失去2个电子,则用单线桥法表示的式子为:
MnCl2+Cl2↑+2H2O中,Mn元素的化合价从MnO2中的+4价降低到MnCl2中的+2价,得到2个电子,Cl元素的化合价从HCl中的-1价升高到Cl2中的0价,失去2个电子,则用单线桥法表示的式子为:![]() (浓)
(浓)![]() MnCl2 + Cl2↑+ 2H2O。
MnCl2 + Cl2↑+ 2H2O。
(2). 生成标准状况下氯气4.48 L,则氯气的物质的量是:4.48L÷22.4L/mol=0.2mol,设反应消耗的MnO2的物质的量是xmol,则有:
MnO2+4HCl(浓)![]() MnCl2+ Cl2↑+ 2H2O
MnCl2+ Cl2↑+ 2H2O
1mol 1mol
xmol 0.2mol,得x = 0.2mol,则反应消耗的MnO2的质量是0.2mol×87g/mol = 17.4g,故答案是:17.4g。
(3). 设参加反应的HCl的物质的量是ymol,则有:
MnO2+4HCl(浓)![]() MnCl2+ Cl2↑+ 2H2O
MnCl2+ Cl2↑+ 2H2O
4mol 1mol
ymol 0.2mol,得y = 0.8mol,由反应方程式可知,被氧化的HCl是参加反应的HCl的一半,故被氧化的HCl的物质的量是0.8mol×![]() = 0.4mol,故答案是:0.4mol。
= 0.4mol,故答案是:0.4mol。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1。
CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1。
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
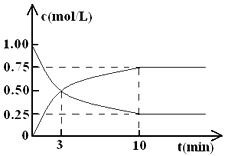
(1)从反应开始到平衡,氢气的平均反应速率v( H2 )= ________ ,CO2的转化率=________。
(2)该反应的平衡常数表达式k=__________ 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是_________________ (填编号)。
A.将H2O(g)从体系中分离B.充入He(g),使体系压强增大
C.升高温度 D.再充入lmolCO2和3molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法中正确的是( )
A. 元素排序的依据是元素的相对原子质量
B. 元素排序的依据是原子的核电荷数
C. 同一横行或同一纵行元素的性质相同
D. 具有稳定的形式,不可能再有任何新的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
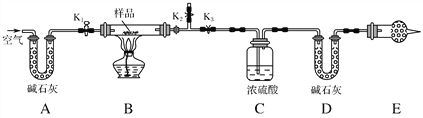
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是_________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为_________________________________________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是___________________。
②E处干燥管中盛放的药品是________,其作用是__________________ ________________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量________(填“偏大”、“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分有机物之间的转化关系以及转化过程相对分子质量变化关系如下:
物质转化关系:RCH2OH ![]() RCHO
RCHO![]() RCOOH
RCOOH
相对分子质量:M M2M+14
已知:物质A中只含有C.H、O三种元素,一定条件下能发生银镜反应,物质C的相对分子质量为104.A与其他物质之间的转化关系如图所示:
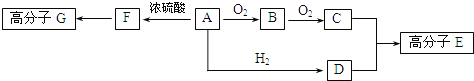
请回答下列问题:
(1)F中含有的官能团有________;G的结构简式___________。
(2)一定条件下B发生银镜反应的化学方程式__________。
(3)由C.D在一定条件下反应还能生成环状化合物,其化学反应方程式为_________。
(4)A的同分异构体很多,写出与A中所含官能团不同,但能与NaOH溶液反应的2种同分异构体的结构简式:_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com