
【题目】常温下用惰性电极电解200mLNaCl、CuSO4的混合溶液,所得气体的体积随时间变化如下图所示,根据图中信息回答下列问题:( 注:气体体积已换算成标准状况下的体积,且忽略气体在水中的溶解和溶液体积的变化.)
(1)曲线(选填“Ⅰ”或“Ⅱ”) 表示阳极产生气体的变化情况.
(2)NaCl的物质的量浓度为;CuSO4 的物质的量浓度 .
(3)t2时所得溶液的pH为 .
【答案】
(1)Ⅱ
(2)0.1mol/L;0.1mol/L
(3)1
【解析】解:刚开始时阴极Cu2+得电子,无气体放出,Cu2+反应完溶液中的H+放电,Ⅰ是H2 , 阳极先是溶液中的Cl﹣放电,反应完后溶液中的OH﹣放电,电解200mL一定浓度的NaCl与CuSO4混合溶液,阳极发生2Cl﹣﹣2e﹣=Cl2↑、4OH﹣﹣4e﹣=O2↑+2H2O,阴极发生Cu2++2e﹣=Cu、2H++2e﹣=H2↑,(1)通过以上分析知,I表示阴极生成的气体、II表示阳极生成的气体,所以答案是:Ⅱ;(2)由图可知,产生氯气为224mL,则由2Cl﹣﹣2e﹣=Cl2↑可知,n(NaCl)= ![]() ×2=0.02mol,所以c(NaCl)=
×2=0.02mol,所以c(NaCl)= ![]() =0.1mol/L,Ⅱ曲线中由t2时生成氧气为112mL,n(O2)=
=0.1mol/L,Ⅱ曲线中由t2时生成氧气为112mL,n(O2)= ![]() =0.005mol,则共转移电子为0.02mol+0.005mol×4=0.04mol,根据电子守恒及Cu2++2e﹣=Cu可知,n(CuSO4)=
=0.005mol,则共转移电子为0.02mol+0.005mol×4=0.04mol,根据电子守恒及Cu2++2e﹣=Cu可知,n(CuSO4)= ![]() =0.02mol,所以c(CuSO4)=
=0.02mol,所以c(CuSO4)= ![]() =0.1mol/L,所以答案是:0.1mol/L;0.1mol/L;(3)由t2时4OH﹣﹣4e﹣=O2↑+2H2O~4H+ , n(H+)=0.005mol×4=0.02mol,则溶液的c(H+)=
=0.1mol/L,所以答案是:0.1mol/L;0.1mol/L;(3)由t2时4OH﹣﹣4e﹣=O2↑+2H2O~4H+ , n(H+)=0.005mol×4=0.02mol,则溶液的c(H+)= ![]() =0.1mol/L,则溶液的pH=1,所以答案是:1.
=0.1mol/L,则溶液的pH=1,所以答案是:1.


科目:高中化学 来源: 题型:
【题目】I.A、B、C、D均为中学化学常见的纯净物,A是单质,它们之间有如下的反应关系;
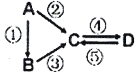
(1)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染,B与C在一定条件下反应生成的A是大气的主要成分,写出B-C的化学方程式:_______________。
(2)若D物质具有两性,②、③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体,写出A→C的离子方程式:______________________。
(3)若A是制作芯片常用材料,B为A单质的氧化物,C为水玻璃的主要成分.写出A→C的离子方程式:__________________________。
(4)若A是应用最广泛的金属.④反应用到A,②、⑤反应均用到同一种非金属单质,C的溶液用于蚀刻印刷铜电路板,写出C→D的离子方程式:__________________。
(5)若A为淡黄色固体,C、D是氧化物,且是是造成酸雨的主要物质,B与C可反应生成A。写出B完全燃烧的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将两个铂电极插入一定量饱和Na2SO4溶液中进行电解,通电一段时间后,在阳极上放出a mol气体,同时有w g Na2SO410H2O晶体析出.若温度不变,此时剩余溶液中溶质的质量分数为( )
A.![]() ×100%
×100%
B.![]() ×100%
×100%
C.![]() ×100%
×100%
D.![]() ×100%
×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度(×10﹣3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①可以判断该分解反应已经达到化学平衡的是(填字母).
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,计算25.0℃时的分解平衡常数为 .
(2)已知:NH2COONH4+2H2ONH4HCO3+NH3H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO﹣)随时间变化趋势如图所示.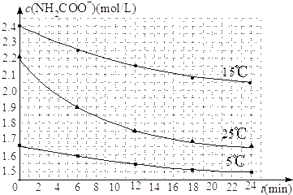
③计算25℃时,0~6min氨基甲酸铵水解反应的平均速率为 .
④根据图中信息,如何说明水解反应的平均速率随温度升高而增大: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学为了探究原电池工作的原理,进行了如下系列实验,请你一起参与实验并分析实验结果后回答有关问题: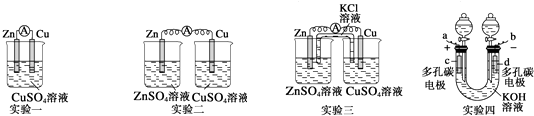
(1)实验一中铜片、锌片表面均有红色物质析出,电流计指针偏转,但较短时间内电流即明显减小.实验结束时测得锌片减少了3.94g,铜片增重了3.84g,则该原电池的工作效率是(指参加原电池反应的锌占反应总量的百分数).
(2)实验二中刚将铜、锌片插入溶液中时电流计指针有偏转,但立即就归零了.解释锌失去的电子能不能持续通过导线流向铜极给Cu2+ .
(3)实验三中盐桥中的K+流向溶液(填ZnSO4或CuSO4),如果Zn的消耗速率为1×10﹣3 mol/s,则K+的迁移速率为mol/s.
(4)实验四中,调节低压电源的电压到6V,并把其正、负极分别与上图装置中的两个碳电极相连接;接通电源,图示中的“+”连接到电源的正极上,“﹣”连接到电源的负极上,电解氢氧化钾溶液制取氢气、氧气,且制得的氢气与氧气的体积比为2:1,去掉电源,该装置就成为一只氢氧燃料电池,用带有一小灯泡的导线连接a、b,灯泡即可发亮.则下列说法错误的是 .
A.在电解KOH溶液制备H2和O2时,KOH的作用是增强溶液的导电性,一段时间后其浓度增大
B.当作为氢氧燃料电池时,c极发生氧化反应,d极发生还原反应
C.当作为氢氧燃料电池时,电解质溶液中的OH﹣向着d极移动
D.如将KOH溶液换成稀H2SO4 , 且作为氢氧燃料电池时,c极的电极反应为:O2+2H2O+4e﹣═4OH﹣ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小闵同学拥有下列实验仪器:

(1)写出仪器名称:c______。
(2)实验室用氯酸钾和二氧化锰制取氧气:
①上述仪器中不需要用到的是(填序号)_____。
②在用排水法收集氧气的过程中,判断集气瓶中氧气已集满的现象是______。
A.集气瓶中水位下降了;
B.在水槽中出现气泡;
C.将带火星的木条放在集气瓶口,木条复燃。
③要从反应后的剩余固体中回收二氧化锰,需要以下操作步骤:______、______、洗涤、烘干。
④小闵是否可以用向上排空气法收集氧气______(填写是或否)。
⑤小闵若在实验室利用12.25g氯酸钾与3gMnO2混合加热,列式计算最多可以得到多少物质的量的氧气____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,将装有N2和NO2混合气体的试管倒立在水中,经足够的时间后,试管内气体的体积缩小为原体积的3/5,则原混合气体中N2和NO2体积比是
A. 2/3 B. 3/2 C. 3/5 D. 5/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应一般均会伴随着能量变化,对H2在O2中燃烧的反应,正确的是( )
A.该反应为吸热反应
B.该反应为放热反应
C.断裂H﹣H键吸收能量
D.生成H﹣O键吸收能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com