
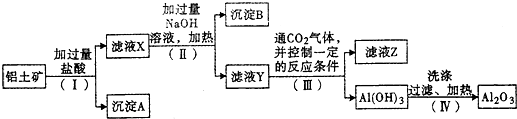
| ||
| ||


科目:高中化学 来源: 题型:
| A、用过滤的方法分离苯和苯酚 |
| B、用NaOH溶液除去乙酸乙酯中混有的乙酸等杂质 |
| C、制备氢氧化铁胶体时,将FeCl3饱和溶液逐滴滴入沸水中 |
| D、用湿润的红色石蕊试纸测量某溶液的酸碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该物质属于不饱和烃 |
| B、该分子碳、氮原子均满足8电子结构 |
| C、该分子所有原子处在一条直线上 |
| D、1mol该物质在一定条件下可与8molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KMnO4 |
| B、KClO3 |
| C、CaCl2 |
| D、Ca(ClO)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 25 | 325 | 700 | 1160 |
| 固体质量/g | 1.000 | 0.877 | 0.685 | 0.384 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com