
【题目】某化学兴趣小组为探究二氧化硫的性质,按如图所示装置进行实验。

请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是__________,反应的化学方程式为_______________。
(2)装置B中的现象是__________________,反应的离子方程式为_________________。
(3)装置C中的现象是____________________,该现象说明二氧化硫具有的性质是________________________。
(4)装置D的目的是探究二氧化硫与品红作用的可逆性,写出实验操作及现象_____________。
(5)尾气可采用__________溶液吸收。
【答案】蒸馏烧瓶 Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O 溶液由紫色变为无色 5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ 溶液中出现淡黄色浑浊 氧化性 品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复红色 氢氧化钠
【解析】
(1)根据装置构造判断其名称,硫酸和亚硫酸钠反应生成二氧化硫、水和硫酸钠,据此解答。
(2)根据二氧化硫能被酸性高锰酸钾溶液氧化分析;
(3)根据二氧化硫能把硫离子氧化为单质分析;
(4)根据生成的无色物质不稳定分析解答;
(5)根据二氧化硫是酸性氧化物分析。
(1)盛放亚硫酸钠的仪器为蒸馏烧瓶,其中发生反应的化学方程式为Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O;
(2)二氧化硫具有还原性,高锰酸钾与SO2发生氧化还原反应,因此现象是溶液由紫红色变为无色(或紫红色褪色),反应的离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
(3)C中Na2S与SO2发生氧化还原反应生成水和单质S,因此C中的实验现象是无色溶液中出现淡黄色浑浊;反应中SO2发生还原反应,说明SO2具有氧化性;
(4)品红与SO2反应后褪色,品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色即可证明SO2与品红作用的可逆性。
(5)二氧化硫有毒,属于大气污染物,二氧化硫是酸性氧化物,因此尾气可用NaOH溶液吸收,以防止污染环境。


科目:高中化学 来源: 题型:
【题目】关于化合物 ,下列叙述正确的是( )
,下列叙述正确的是( )
A. 分子间可形成氢键 B. 分子中既有极性键又有非极性键
C. 分子中有7个σ键和1个π键 D. 该分子在水中的溶解度小于2丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验说法不正确的是
A. 在两支试管中分别加1 mL无水乙醇和1.5 g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性
B. 向少量的火柴头浸泡液中滴加AgNO3、稀HNO3和NaNO2,检验火柴头中的氯元素
C. 在2mL紫色的COCl2溶液中加入浓盐酸,可使溶液显蓝色
D. 制备摩尔盐时,最后在蒸发皿中蒸发浓缩溶液,加热至液体表面出现晶膜为止,不能将溶液全部蒸干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对以下A至D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl―→H2O2+NaCl
B.Ag2O+H2O2―→Ag+O2+H2O
C.H2O2―→H2O+O2
D.H2O2+Cr2(SO4)3+KOH―→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是____________(填字母,下同),H2O2仅体现还原性的反应是____________,H2O2既体现氧化性又体现还原性的反应是__________,H2O2既不作氧化剂又不作还原剂的反应是____________。
(2)用单线桥法标出D反应中电子转移的方向和数目:________________________________________3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O反应中氧化剂是__________,被氧化的元素是______,还原产物是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡妥油(D)用作香料的原料,它可由A合成得到:
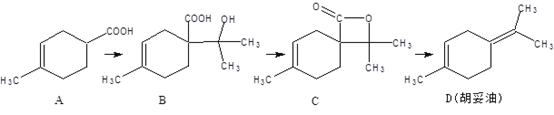
下列说法正确的是
A. 若有机物A是由异戊二烯)和丙烯酸加热得到的,则该反应的反应类型属于加成反应
B. 有机物B既能与O2催化氧化生成醛,又能跟NaHCO3溶液反应放出CO2气体
C. 有机物C的所有同分异构体中不可能有芳香族化合物存在
D. 有机物D分子中所有碳原子一定共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,某烃的密度是1.25g·L-1,一定体积的该烃完全燃烧生成4.48LCO2和3.6g水,该烃的分子式_________________。
(2)有机物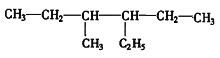 的正确命名为_______________________。
的正确命名为_______________________。
(3)某烃lmol与2molHCl完全加成,生成的氯代烷烃最多还可以与6mol氯气反应,则该烃的结构简式为_______________________。
(4)有下列五种烃:
① ②
②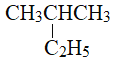 ③乙烷
③乙烷
④正戊烷 ⑤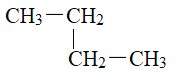 ⑥
⑥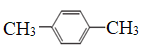
其中互为同分异构体的是__________________(填序号),②③④⑤四种物质按它们的沸点由低到高的顺序是_______________(填序号),等质量的①③⑥三种物质,完全燃烧时消耗O2的物质的量由少到多的顺序为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
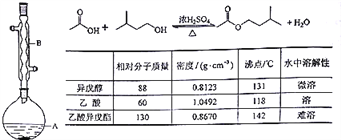
实验步骤:
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
(1)仪器B的名称是:________________________。
(2)在洗涤操作中,第一次水洗的主要目的是:___________________________; 第二次水洗的主要目的是:________________________________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后_______(填标号)。
A.直接将乙酸异戊酯从分液漏斗的上口倒出
B.直接将乙酸异戊酯从分液漏斗的下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:______________________。
(5)本实验的产率是___________(填标号)。
a. 30% b.40% c.60% d.90%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关“电离平衡”的叙述中正确的是( )
A. 电解质在溶液里达到电离平衡时,溶质电离出的离子浓度相等
B. 电离平衡时,由于分子和离子的浓度不断发生变化,所以说电离平衡是动态平衡
C. 电离平衡是相对的.暂时的,外界条件改变时,平衡就会发生移动
D. 电解质达到电离平衡后,分子的浓度和离子的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用25mL18.4mol/L的浓硫酸与铜共热一段时间后,冷却,过滤除去多余的铜,将滤液稀释到100 mL,所得溶液中SO42-浓度为3mol/L,则此时溶液中CuSO4的物质的量浓度为
A. 0.5mol/L B. 1.6 mol/L C. 1.8 mol/L D. 3mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com