
 ��֪A��B��C����ѧ��ѧ�ij������ʣ�������һ��������������ת����ϵ��
��֪A��B��C����ѧ��ѧ�ij������ʣ�������һ��������������ת����ϵ��
| ||
| �� |
| ||
| �� |
| Cu |
| �� |
| ˮԡ |
| �� |
| Cu |
| �� |
| ˮԡ |
| �� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��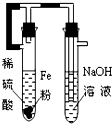 ��ȡFe��OH��2���� |
B�� ���װ�õ������� |
C�� ����HBr |
D�� �����Ԫ�صĴ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | c��һԪ�ᣩ | c��NaOH��/mol/L | �����Һ��pH |
| �� | c��HX��=0.1mol/L | 0.1 | pH=x |
| �� | c��HY��=0.1mol/L | 0.1 | pH=7 |
| �� | c��HZ��=0.1mol/L | 0.1 | pH=9 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| O2 |
| O2 |
| HO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1.8g��ˮ��D2O���к�NA������ |
| B����״���£�2.24L Cl2�����ϡNaOH��Һ��Ӧ��ת�Ƶĵ�������Ϊ0.2NA |
| C�������£�21.0g��ϩ�Ͷ�ϩ�Ļ�������к��е�̼ԭ����ĿΪ1.5NA |
| D��������ͭ�뺬2mol H2SO4��Ũ�����ַ�Ӧ��������NA��SO2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ӵ�����ڶ��ε�أ���Ŀǰ�ֻ����ʼDZ����Ե��ִ������Ʒ��Ӧ����㷺�ĵ�� |
| B��ͭпԭ��ع���ʱ�����������·��п�缫����ͭ�缫������ͭ�缫���������Һ���ص�п�缫 |
| C���״�ȼ�ϵ�ؿɰѻ�ѧ��ת��Ϊ���� |
| D��п�̸ɵ�ظ��ݵ���ʵ����ʷ�Ϊ���Լ��������࣬��������п�缫Ϊ����������п�������Ĺ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A����20.16 L |
| B������20.16 L |
| C������20.16 L��40.32 L֮�� |
| D������40.32 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol Cl2������Fe��Ӧ��ת�Ƶĵ�����Ϊ3NA |
| B��������ΪNA��CO��C2H4����������ԼΪ22.4L������Ϊ28g |
| C��46g NO2��N2O4������庬��ԭ����Ϊ3NA |
| D�������£�0.1mol/L��NH4NO3��Һ�е�ԭ����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com