
【题目】下列物质中,不能用两种单质直接化合制得的是( )
A.CuSB.Fe3O4C.FeCl3D.Al2O3
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.煤的干馏是将煤在空气中加强热使之分解的过程
B.溴的四氯化碳溶液可用来鉴别裂化汽油和直馏汽油
C.石油裂解的主要目的是为了得到更多的汽油
D.煤的气化是将其通过物理变化转化为气态的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定物质的量的SO2与NaOH溶液反应,所得溶液中含Na2SO3和NaHSO3,若两者物质的量之比为3﹕5,则参加反应的SO2与NaOH的物质的量之比为
A. 3﹕5 B. 1﹕2 C. 18﹕8 D. 8﹕11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述不正确的是
A. 用氯化钠腌制食品,可延长食品的保存时间
B. 用硫酸亚铁补铁时,不可同时服用维生素C
C. 用铝箔制成的食品包装“锡纸”,可以包裹食品在烤箱中加热
D. 用纤维素和淀粉为原料制成可降解塑料,有利于减少白色污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物在磁性材料、电池材料、超硬材料及催化剂等领域有广泛应用.
(1)CoxNi(1-x)Fe2O4可用作H2O2分解的催化剂
①已知CoxNi(1-x)Fe2O4中Co、Ni化合价均为+2,则该化合物这铁元素的化合价为_______
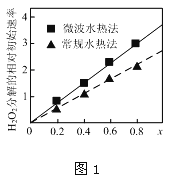
②如图1表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线.由图中信息可知:_______法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效果更好的是__________
③CoxNi(1-x)Fe2O4能与氢碘酸发生氧化还原反应,所得溶液这含有三种金属离子,写出反应的离子方程式____________
(2)草酸钴是制备钴的氧化物的重要原料。下图2为二水合草酸钴(CoC2O4·2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。

① 通过计算确定C点剩余固体的化学式为________
② 取一定质量二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比为______________。
(3)以硫化钴(Co3S4)为原料冶炼钴的原理为在空气中焙烧矿石得到两种氧化物,反应中只有一种元素被氧化,然后利用铝热反应可得到钴。写出焙烧时的化学方程式:________;写出铝热反应的引发操作_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的工业制法中,错误的是( )
A. 制钠:以海水为原料制得NaCl,再电解熔融NaCl得钠
B. 制铁:以焦炭和铁矿石为原料,用CO还原铁矿石得铁
C. 制硅:用焦炭还原二氧化硅得硅
D. 制铝:电解液态氯化铝得铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是
A. 等量固态硫燃烧比气态硫燃烧放热多
B. 已知2H2(g)+O2(g)![]() 2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为 241.8 kJ·mol-1
2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为 241.8 kJ·mol-1
C. 已知2C(s)+2O2(g)![]() 2CO2(g) ΔH=a 2C(s)+O2(g)
2CO2(g) ΔH=a 2C(s)+O2(g)![]() 2CO(g) ΔH=b,则a>b
2CO(g) ΔH=b,则a>b
D. 已知 NaOH(aq)+HCl(aq)![]() NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则含 40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ 的热量
NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则含 40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ 的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是

①分子式为C12H20O2
②能使酸性KMnO4溶液褪色,但不能使溴水褪色
③能发生的反应类型有:加成、取代、氧化、加聚
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1 mol该有机物水解时只能消耗1 mol NaOH
⑥1 mol该有机物在一定条件下和H2反应,共消耗H2为3 mol
A. ①②③ B. ①②⑤ C. ②④⑥ D. ②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2。装置如图(有些夹持装置省略)所示。已知SO2Cl2的熔点为- 54.1℃,沸点为69.1℃,在潮湿空气中遇水能发生剧烈的水解反应,并产生白雾。

(1)仪器组装完毕后,检验戊装置气密性的方法是___________________,表明装置气密性良好。
(2)仪器C的作用是吸收逸出的有毒气体Cl2、SO2,防止污染环境和__________________。
(3)试剂X、Y的组合最好是__________________(填字母)。
a.18.4 mol/L H2SO4+Cu b.4 mol/L HNO3 +Na2SO3 c.60% H2SO4+K2SO3
(4)戊是贮气装置,则E中的试剂是______;若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是:________________。
(5)反应结束后,将丙中的混合物分离开的实验操作是______。若反应中消耗的氯气的体积为896 ml。(已转化为标准状况,SO2足量),最后得到纯净的磺酰氯3.3 g,则磺酰氯的产率为 ______(保留三位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com