
����Ŀ��������(SO2Cl2)��һ����Ҫ���л��ϳ��Լ���ʵ���ҿ�����SO2��Cl2��Ӧ��ȡ������SO2Cl2��װ����ͼ����Щ�г�װ��ʡ�ԣ���ʾ����֪SO2Cl2���۵�Ϊ- 54.1�棬�е�Ϊ69.1�棬�ڳ�ʪ��������ˮ�ܷ������ҵ�ˮ�ⷴӦ��������������

��1��������װ��Ϻ�����װ�������Եķ�����___________________������װ�����������á�
��2������C�������������ݳ����ж�����Cl2��SO2����ֹ��Ⱦ������__________________��
��3���Լ�X��Y����������__________________������ĸ����
a.18.4 mol/L H2SO4+Cu b.4 mol/L HNO3 +Na2SO3 c.60% H2SO4+K2SO3
��4����������װ�ã���E�е��Լ���______����ȱ��װ���ҺͶ�����ʪ�������Ͷ�������֮�䷢����Ӧ�Ļ�ѧ����ʽ�ǣ�________________��
��5����Ӧ���������еĻ������뿪��ʵ�������______������Ӧ�����ĵ����������Ϊ896 ml������ת��Ϊ��״����SO2�����������õ������Ļ�����3.3 g��������ȵIJ���Ϊ ______��������λ��Ч���֣���
���𰸡� �ر�c��d�����Һ©���ڼ�ˮ����d��һ��ʱ����Һ©���ڵ�Һ�岻���µ� ��ֹ�����е�ˮ����������ϵ���»�����ˮ�� c ����ʳ��ˮ SO2+Cl2+2H2O=H2SO4+2HCl ���� 61.1%
���������ɣ�4������������װ�ÿ�֪��װ���Ʊ����������������������ڱ��з�Ӧ����SO2Cl2�����л���̿������������ã�SO2Cl2��ˮ�������ҵ�ˮ�ⷴӦ����Ϊ�����������E��ʢ����Һ���������ų�װ���������������DZ���ʳ��ˮ�����������ܽ�ȣ�������������SO2Cl2�е�͡��ӷ���BΪ�����ܣ�ʹ�ӷ��IJ���SO2Cl2������������ʯ������Ϊ��Ӧ�Ķ���������������ֹ��Ⱦ�����������տ����е�ˮ��������ֹ����C�е��»�����ˮ�⣬��
��1����װ���к��з�Һ©�����������װ�������Եķ����ǹر�c��d�����Һ©���ڼ�ˮ����d��һ��ʱ����Һ©���ڵ�Һ�岻���µΣ�����װ����������������2�����ڻ���һ����Cl2��SO2ͨ���������ݳ�����C��Ӧʹ�ü����Լ�������SO2Cl2��ˮ��ˮ�⣬�ʼ�ʯ������������������SO2����ֹ�����е�ˮ����������ϵ���»�����ˮ������3�������Ʊ�SO2��װ�ã�ͭ��Ũ���ᷴӦ��Ҫ���ȣ�����������SO2������ѡ��c.60% H2SO4+K2SO3���Ʊ�SO2����4������ˮ�����ڱ���ʳ��ˮ����E�е��Լ��DZ���ʳ��ˮ��������ˮ���ڵ������¿ɽ�SO2���������ᣬ��������ԭΪHCl����Ӧ�ķ���ʽΪSO2+Cl2+2H2O��H2SO4+2HCl����5������е㲻ͬ��Һ�����������ķ��������Ա��л������뿪��ʵ���������������״���£�896mlCl2Ϊ0.04mol���������Ͽɵõ�0.04molSO2Cl2����Ϊ0.04mol��135g/mol��5.4g������SO2Cl2�IJ�Ϊ3.3g/5.4g��100%��61.1%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����������ֵ���ֱ�ӻ����Ƶõ��ǣ� ��
A.CuSB.Fe3O4C.FeCl3D.Al2O3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. ���ʯ��ʯī��Ϊ̼��ͬ�������壬����ȼ��ʱ����������������һ����̼�������ȼ�����ɶ�����̼����Ӧ�зų���������ͼ��ʾ��
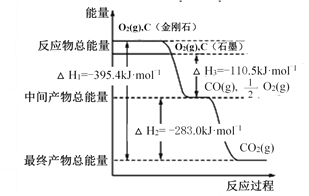
��1���������Ľ��ʯ��ʯī��ȫȼ�գ�___________(�������ʯ���� ��ʯī��)�ų����������࣬д����ʾʯīȼ���ȵ��Ȼ�ѧ����ʽ��______________________________________��
��2����ͨ��״���£�__________________(�������ʯ������ʯī��)���ȶ���д��ʯīת��Ϊ���ʯ���Ȼ�ѧ����ʽ��__________��
��3��12 gʯī��һ����������ȼ�գ��������� 36 g���ù����зų�������Ϊ_______ ��
II. ij��Ӧ��������Ӧ A��B��C ���ɣ����ķ�Ӧ����������ͼ��ʾ(E1��E2��E3��E4 ��ʾ���)���ش��������⡣

��1��A��B �����е� ��H______________(����������������)0��
��2���������_____________________(������������������)�ı䷴Ӧ���ʱ䡣
��3��������Ӧ�� ��H��_____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H-H������Ϊ436kJ/mol��H-N������Ϊ391kJ/mol,���ݻ�ѧ����ʽ: N2(g)+3H2(g)=2NH3(g) ��H=-92kJ/mol,��N��N��������
A. 946kJ/mol B. 473kJ/mol C. 211kJ/mol D. 346kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ϊ��ѹ��������Ϊ�������������������зֱ����2molSO2��1molO2����ʱ�����������ȡ������¶Ȳ��䷢����Ӧ��2SO2(g)+O2(g)![]() 2SO3(g)����H<0��һ��ʱ���ﵽƽ�⣬Ϊʹ�������е�SO2��ƽ�������е����������ȣ����д�ʩ�п��е���
2SO3(g)����H<0��һ��ʱ���ﵽƽ�⣬Ϊʹ�������е�SO2��ƽ�������е����������ȣ����д�ʩ�п��е���
A. ���������г���һ�����ĵ���
B. ��������г���һ������SO2����
C. �������������¶�
D. �����������ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�����ڱ���һ���֣��ش������й����⣺ 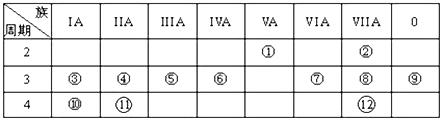
��1��������ԭ�ӽṹʾ��ͼ�� �� д���ٵ���̬�⻯����ӵĵ���ʽ ��
��2��Ԫ�آܡ��⡢�����������ˮ����ļ�����ǿ��Ϊ��Ԫ�آڡ��ߡ�����⻯���ȶ�����ǿ������˳��Ϊ�����û�ѧʽ��գ���
��3���������γɵĻ�����R2O2��������ѧ������Ϊ ��
��4����ٺ͢����ڵ�һ��Ԫ��A�����ж��ֲ�ͬ��̬�ĵ��ʣ�����һ�ֳ�����ԭ��صĵ缫����һ����ȼ�ϵ�أ����������������缫����KOH��Һ�У�Ȼ����X��ͨ��A�������̬�⻯���Y��ͨ��O2 �� ��д���缫��Ӧʽ�� �������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥ MgCl2 ���������е� Fe3+�����ڼ��Ƚ���������¼���һ���Լ������˺��ټ����������ᣬ�����Լ���
A.NH3��H2OB.MgOC.Na2CO3D.NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֻ�ı�һ��Ӱ�����أ�ƽ�ⳣ��K�뻯ѧƽ���ƶ��Ĺ�ϵ������������
A. Kֵ���䣬ƽ������ƶ� B. Kֵ�仯��ƽ��һ���ƶ�
C. ƽ���ƶ���Kֵ���ܲ��� D. ƽ���ƶ���Kֵһ���仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��������ʼ���ˮ�У�����������Һ��ˮ����� c(H+)��10-7 mol��L-1 ����
A.NaOHB.NH4ClC.HClD.Na2SO4
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com