
【题目】现有常温下甲、乙、丙三种溶液,甲为0.1mol·L-1的NaOH溶液,乙为0.1mol·L-1的HCl溶液,丙为0.1mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=___。
(2)丙溶液中存在的电离平衡为___(用电离平衡方程式表示)。
(3)常温下,用水稀释0.1mol·L-1的CH3COOH溶液,下列各量随水量的增加而增大的是___(填序号)。
①n(H+) ②c(H+) ③![]() ④c(OH-)
④c(OH-)
(4)甲、乙、丙三种溶液中由水电离出的c(OH-)最大的是___。
(5)某同学用甲溶液分别滴定20.00mL乙溶液和20.00mL丙溶液,得到如图所示的两条滴定曲线,则a=___。
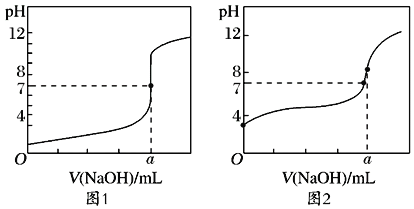
(6)图___(填1或2)表示NaOH溶液滴定CH3COOH溶液的过程。
(7)图2中a点对应的溶液pH=8,原因是___(用离子方程式表示)。
【答案】13 CH3COOH![]() CH3COO-+H+,H2O
CH3COO-+H+,H2O![]() OH-+H+ ①④ 丙 20.00 2 CH3COO-+H2O
OH-+H+ ①④ 丙 20.00 2 CH3COO-+H2O![]() OH-+CH3COOH
OH-+CH3COOH
【解析】
(1) 氢氧化钠是强碱,所以溶液中氢离子浓度是1 x10-13mol/L,则溶液的pH=13;
(2)醋酸和水都是弱电解质,存在电离平衡,所以电离方程式分别是CH3COOH![]() CH3COO-+H+,H2O
CH3COO-+H+,H2O![]() OH-+H+;
OH-+H+;
(3) 常温下,用水稀释0.1mol·L-1的CH3COOH溶液,促进反应CH3COOH![]() CH3COO-+H+向右移动,所以n(H+)变大,但是体积增大的程度大于氢离子增加的程度,所以c(H+)变小,但是,常温下Kw不变,根据Kw= c(H+)· c(OH-)不变,所以c(OH-)变大;温度不变,
CH3COO-+H+向右移动,所以n(H+)变大,但是体积增大的程度大于氢离子增加的程度,所以c(H+)变小,但是,常温下Kw不变,根据Kw= c(H+)· c(OH-)不变,所以c(OH-)变大;温度不变,
Ka= 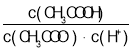 不变,而c(H+)变小,所以
不变,而c(H+)变小,所以![]() 变小;
变小;
(4)酸或碱都是抑制水的电离平衡的,且溶液中氢离子或OH-浓度越大,对水的电离的抑制程度越大。所以根据酸碱的浓度可知,甲、乙、两三种溶液中由水电离出的c(OH-)的大小关系为丙>甲=乙;
(5)盐酸和氢氧化钠恰好反应时,溶液显中性,所以根据酸碱的浓度以及盐酸的体积可知,消耗氢氧化钠溶液的体积是20.00ml,即a = 20.00ml;
(6) 图2中V(NaOH)=0时,pH大于1,可知0.1mol/L该溶液的pH大于1,所以图2应该表示甲溶液(NaOH溶液)滴定丙溶液(CH3COOH溶液)的曲线;
(7) 图2中a点对应的溶液pH=8,是因为此时刚好生成醋酸钠,醋酸根水解:CH3COO-+H2O![]() OH-+CH3COOH。
OH-+CH3COOH。


 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】下列变化属于①放热反应 ②吸热反应
A:分解反应 B:化合反应C:置换反应
(1)氯酸钾分解制氧气,既是_______(填①或②)又是______。(填A或B或C,下同)
(2)生石灰跟水反应生成熟石灰,既是_______又是______。
(3)锌粒与稀硫酸的反应,既是_______又是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】垃圾分类正在全国逐渐推广,垃圾资源化是可持续、绿色发展的重要途径。由金属废料(主要含铁、铜和它们的氧化物)制得碱式碳酸铜和摩尔盐[(NH4)2SO4·FeSO4·xH2O]的工艺流程如下图所示:
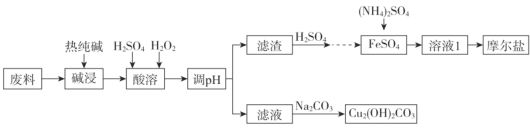
已知:Ksp[Fe(OH)3]=1×10-38 ,Ksp[Cu(OH)2]= 2.2×10-21,一般认为某离子浓度小于或等于10-5mol/L时,该离子转化或去除完全。
请回答下列问题:
(1)热纯碱的作用是_______________,H2O2的电子式为___________。
(2)调pH步骤可选用的试剂为______________。
A.CuO B.Cu(OH)2 C.Fe2O3 D.Fe(OH)3
(3)若所得溶液中c(Cu2+)=0.22 mol·L-1,则需要调节的pH范围是_______________。
(4)溶液1经过加热、蒸发至溶液中出现晶体时,自然冷却即可得到晶体,然后抽滤,用酒精洗涤晶体,酒精洗涤的目的是____________________________________。
(5)写出该流程中生成碱式碳酸铜的离子方程式________________________________。
(6)取3.92g摩尔盐产品,在隔绝空气的条件下加热至135°C时完全失去结晶水,此时固体质量为2.84g,则该摩尔盐结晶水个数x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用,某博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
主要成分的化学式 | |||
|
|
|
|
铁器在具有![]() 、_____等环境中容易被腐蚀。
、_____等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.![]() 转化为
转化为![]() 。
。
Ⅱ.![]() 在自然环境中形成
在自然环境中形成![]() ,该物质中铁元素的化合价为_______。
,该物质中铁元素的化合价为_______。
Ⅲ.![]() 和
和![]() 反应形成致密的
反应形成致密的![]() 保护层,
保护层,![]() 的作用是_______。
的作用是_______。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
Ⅳ.![]() 保护层被氧化为
保护层被氧化为![]() ,如此往复腐蚀,___
,如此往复腐蚀,___![]() +___
+___![]() +___
+___![]()
![]() ____
____![]() (将反应补充完整)
(将反应补充完整)
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成![]() 保护层,法如下: 将铁器浸没在盛有
保护层,法如下: 将铁器浸没在盛有![]() 溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用
溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用![]() 溶液洗涤至无Cl-。
溶液洗涤至无Cl-。
①检测洗涤液中 Cl-的方法是_____。
②脱氯反应:![]() 。离子反应的本质是离子浓度的减小,比较
。离子反应的本质是离子浓度的减小,比较![]() 与
与![]() 溶解度的大小:__________较大。[填
溶解度的大小:__________较大。[填![]() 与
与![]() ]
]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4[UO2(CO3)3]等。回答下列问题:
(1)UF4用Mg或Ca还原可得金属铀。金属铀的一种堆积方式为体心立方堆积,该堆积方式的空间利用率为__________________;基态钙原子核外电子排布式为_________________;熔点:MgO(2852℃)高于CaO(2614℃),其原因是_____________________________。
(2)![]() 。NH4HF2中所含作用力有____________(填字母)。
。NH4HF2中所含作用力有____________(填字母)。
a. 氢键 b. 配位键 c. 共价键 d. 离子键 e. 金属键
(3)已知: ![]() .
.
①NH4+ 的空间构型为___________,与NH4+ 互为等电子体的分子或离子有_____(写两种)
②CO32- 中碳原子杂化轨道类型为______________________。
③分解产物中属于非极性分子的是_____________________(填字母)。
a. NH3 b. CO2 c. N2 d. H2O
(4)UO2 的晶胞结构及晶胞参数如下图所示:
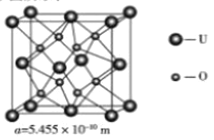
①晶胞中U的配位数为_________________。
②UO2 的密度为__________g·cm-3(列出计算式即可,用NA表示阿伏伽德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是( )
A. 2H+(aq) +![]() (aq)+
(aq)+![]() (aq)+2OH
(aq)+2OH![]() (aq)=BaSO4(s)+2H
(aq)=BaSO4(s)+2H![]() O(l);
O(l);![]() H=
H=![]() 57.3 kJ/mol
57.3 kJ/mol
B. KOH(aq)+![]() H
H![]() SO4(aq)=
SO4(aq)=![]() K
K![]() SO4(aq)+H
SO4(aq)+H![]() O(l);
O(l);![]() H=
H=![]() 57.3kJ/mol
57.3kJ/mol
C. C8H18(l)+![]() O
O![]() (g)=8CO
(g)=8CO![]() (g)+ 9H
(g)+ 9H![]() O;
O;![]() H=
H=![]() 5518 kJ/mol
5518 kJ/mol
D. 2C8H18(g)+25O![]() (g)=16CO
(g)=16CO![]() (g)+18H
(g)+18H![]() O(l);
O(l);![]() H=
H=![]() 5518 kJ/mol
5518 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请回答有关问题
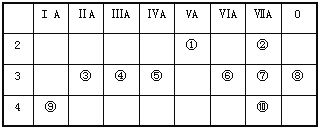
(1)⑤和⑧的元素符号是_______和_______。
(2)表中最活泼的金属元素是___________,非金属性最强的元素是___________(填写元素符号)。
(3)表中能形成两性氢氧化物的元素是___________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:__________________;__________________。
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
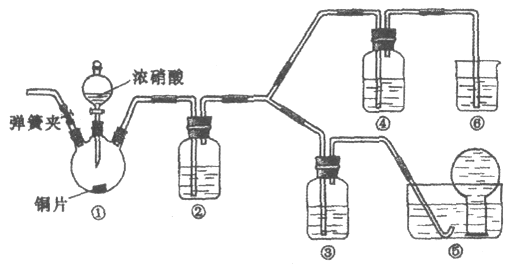
可选药品:浓硝酸、3 mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应2NO2+2 NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中。装置③、④、⑥中盛放的药品依次是_____。
(2)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后_______。
(3)装置①中发生反应的化学方程式是______。
(4)装置②的作用是_____,发生反应的化学方程式是______。
(5)该小组得出的结论所依据的实验现象是______。
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确,这些方案中可行的是______。(选填字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 molX气体跟a molY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)![]() b Z(g)。反应达到平衡后,测得X的转化率为25%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b的数值可能是( )
b Z(g)。反应达到平衡后,测得X的转化率为25%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b的数值可能是( )
A.a=2,b=1 B. a=1,b=2 C.a=2,b=2 D. a=3,b=2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com