
【题目】某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂.下列叙述正确的是( ) 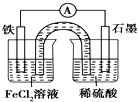
A.原电池工作一段时间后,FeCl2溶液中c(Cl﹣)增大
B.此电池工作原理与硅太阳能电池工作原理相同
C.Fe为正极,石墨上发生的反应为2H++2e﹣═H2↑
D.该装置中的盐桥完全可用金属导线代替
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如下图。回答下列问题:
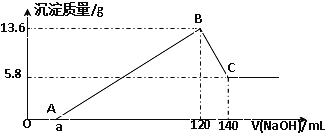
(1)写出OA段和BC段反应的离子方程式:
OA:________________________________ ; BC:_____________________________;
(2)原Mg-Al合金的质量是_____________。
(3)原HCl溶液的物质的量浓度是________________。
(4)所加NaOH溶液的物质的量浓度是____________。
(5)a的值是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,回答下列问题. 
(1)该反应是反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率(填“增大”“减小”“不变”),原因是;
(3)反应体系中加入催化剂对反应热是否有影响? , 原因是;
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 , E2(填“增大”“减小、”“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关自然资源的开发利用的说法不正确的是( )
A. 证明海带中存在碘元素的实验中,需将干海带洗净后置于坩埚中灼烧
B. 以Cu2S为原料可采用火法炼铜冶炼出金属Cu
C. 海水晒盐后的母液中,直接加入CCl4可萃取Br2单质
D. 资料表明,蓝铜矿的主要成分为2CuCO3·Cu(OH)2,当它与焦炭一起高温加热时,可以生成铜、二氧化碳和水。该反应的化学方程式为:2[2CuCO3·Cu(OH)2]+3C![]() 6Cu+7CO2↑+2H2O
6Cu+7CO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶质的质量分数和物质的量浓度的计算结果错误的是( )
A. 密度为0.91g/cm3的氨水,质量分数为25%。该氨水用等体积的水稀释后,所得溶液中溶质的质量分数等于12.5%
B. 有K2SO4和Al2(SO4)3的混合溶液,已如其中Al3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,则此溶液中K+的物质的量浓度为0.2mol/L
C. 将5mol/L的Mg(NO3)2溶液amL稀释至bmL,稀释后溶液中NO3-的物质的量浓变为![]() mol/L
mol/L
D. 将标准状况下,将VLA气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶液的物质的量浓度为![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种物质在酸性溶液中的还原性强弱顺序如下:SO2>I->Fe2+>H2O2。据此判断下列反应不能发生的是
A. 2Fe3++SO2+2H2O=2Fe2++SO![]() +4H+
+4H+
B. H2O2+H2SO4=SO2↑+O2↑+2H2O
C. SO2+I2+2H2O=H2SO4+2HI
D. 2Fe3++2I-=2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中所示物质或概念间的从属关系符合如图的是
X | Y | Z | |
A | 钠元素 | 主族元素 | 短周期元素 |
B | 电解质 | 化合物 | 纯净物 |
C | 氢氧化铁 | 胶体 | 分散系 |
D | 置换反应 | 氧化还原反应 | 放热反应 |
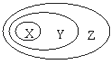
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol 890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
A.C(s)+ ![]() O2(g)=CO(g)△H=﹣393.5 kJ/mol
O2(g)=CO(g)△H=﹣393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(l)△H=+571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3 kJ/mol
D.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H=﹣2800 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com