
【题目】用化学知识填空:
(1)丙烷通过脱氢反应可得丙烯。
已知:①C3H8(g)===CH4(g)+C2H2(g)+H2(g) ΔH1=+156.6 kJ·mol-1
②C3H6(g)===CH4(g)+C2H2(g) ΔH2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)===C3H6(g)+H2(g)的ΔH=__________kJ·mol-1。
(2)0.5mol甲烷燃烧时,生成液态水和二氧化碳,同时放出445kJ的热量,写出甲烷的燃烧热的热化学方程式_________________________________________________
(3)请写出NH4Cl溶液中各离子浓度的大小关系式:___________________________________
(4)常温下,Na2CO3溶液呈碱性,原因是_____________________ (用离子方程式表示)。
(5)①醋酸在水溶液中的电离方程式为______________________。
②下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是_________(填字母序号)。
a. 滴加少量浓盐酸 b. 微热溶液 c. 加水稀释 d. 加入少量醋酸钠晶体
【答案】 +124.2 kJ·mol-1 CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1 c(Cl-)>c(NH![]() )>c(H+)>c(OH-) CO32-+H2O
)>c(H+)>c(OH-) CO32-+H2O![]() HCO3-+OH- CH3COOH
HCO3-+OH- CH3COOH![]() CH3COO-+H+ bc
CH3COO-+H+ bc
【解析】(1)本题考查热化学反应方程式的计算,①-②得出△H=△H1-△H2=(156.6-32.4)kJ·mol-1=+124.2kJ·mol-1;(2)本题考查热化学反应方程式的书写,根据燃烧热的定义,1mol甲烷燃烧产生的热量为1×445/0.5kJ=890kJ,即甲烷燃烧热的热化学反应方程式为:CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1;(3)本题考查离子浓度大小比较,NH4Cl溶液中存在:NH4++H2O ![]() NH3·H2O+H+,NH4+水解程度微弱,因此离子浓度大小顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-);(4)本题考查盐类水解应用,Na2CO3溶液中CO32-发生水解,其水解反应方程式为CO32-+H2O
NH3·H2O+H+,NH4+水解程度微弱,因此离子浓度大小顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-);(4)本题考查盐类水解应用,Na2CO3溶液中CO32-发生水解,其水解反应方程式为CO32-+H2O![]() HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O![]() H2CO3+OH-,使溶液中c(OH-)>c(H+),溶液显碱性;(5)考查弱电解质的电离以及影响弱电解质电离的因素,①CH3COOH属于弱电解质,醋酸部分电离,其电离方程式为CH3COOH
H2CO3+OH-,使溶液中c(OH-)>c(H+),溶液显碱性;(5)考查弱电解质的电离以及影响弱电解质电离的因素,①CH3COOH属于弱电解质,醋酸部分电离,其电离方程式为CH3COOH![]() CH3COO-+H+;②a、滴加少量浓盐酸,c(H+)增大,抑制CH3COOH的电离,故a错误;b、弱电解质的电离是吸热过程,升高温度,促进电离,即CH3COOH的电离程度增大,故b正确;c、加水稀释,促进电离,即CH3COOH的电离程度增大,故c正确;d、加入醋酸钠晶体,CH3COOH的电离程度降低,故d错误。
CH3COO-+H+;②a、滴加少量浓盐酸,c(H+)增大,抑制CH3COOH的电离,故a错误;b、弱电解质的电离是吸热过程,升高温度,促进电离,即CH3COOH的电离程度增大,故b正确;c、加水稀释,促进电离,即CH3COOH的电离程度增大,故c正确;d、加入醋酸钠晶体,CH3COOH的电离程度降低,故d错误。


科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A | B | C | D |
|
|
|
|
钢铁表面水膜的酸性很弱或呈中性,发生吸氧腐蚀 | 钢铁表面水膜的酸性较强,发生析氢腐蚀 | 将锌板换成铜板对钢闸门保护效果更好 | 钢闸门作为阴极而受到保护 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾长石(K2Al2Si6O16)通常也称正长石,主要用于生产玻璃、陶瓷制品,还可用于制取钾肥。某学习小组以钾长石为主要原料,从中提取氧化铝、碳酸钾等物质,工艺流程如下:
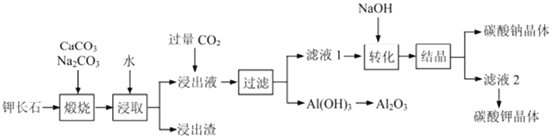
回答以下问题:
(1) 请以氧化物组成的形式表示钾长石的化学式为_____________
(2) 钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的KAlO2 和NaAlO2,写出Al2O3 转化为NaAlO2 的化学方程式_____________________。
(3) 已知“浸取”时应保持溶液呈碱性,分析其原因为____________(用离子方程式解释),若要提高浸取的速率,可采取的措施有_______________(回答一条)。
(4) 滤液1的主要成分是_________(填写化学式)
(5) 此工艺中可以循环利用的主要物质是________、___________和水。
(6) 以石墨为电极,通过电解Al2O3 可制得金属铝。电解池中接电源负极的一极的电极反应式是_______。长时间电解后,需要更换新的石墨电极的是___极(填“阴”或“阳”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把①pH相同的氨水和氢氧化钠溶液②物质的量浓度相同的醋酸和盐酸,分别加水稀释相同倍数后,pH较大的是
A. ①中氢氧化钠溶液较大,②中盐酸较大
B. ①中氨水较大,②中盐酸较大
C. ①中氨水较大,②中醋酸较大
D. ①中氢氧化钠溶液较大,②中醋酸较大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中错误的是
A. 电解池的阳极上发生氧化反应,阴极上发生还原反应
B. 原电池跟电解池连接后,电子从电池负极流向电解池阳极
C. 电镀时,电镀池里的阳极材料发生氧化反应
D. 电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示3套实验装置,分别回答下列问题。
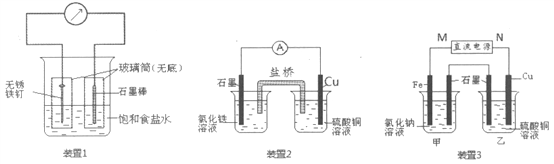
(1)装置1为铁的吸氧腐蚀实验,一段时间后,玻璃筒内的石墨电极上的电极反应式为_________。
(2)装置2中的石墨是_______极,该电极反应式为___________。
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为________极;甲烧杯中铁电极的电极反应为_________________。
②乙烧杯中电解的总方程式为_______________。
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氮化镓(GaN)、砷化镓(GaAs)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点,如砷化镓灯泡寿命是普通灯泡的100倍,而耗能即为10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。请回答下列问题:
(1)镓为元素周期表第31号元素,基态镓原子的电子排布式为__________________,核外电子占据最高能层符号为________。
(2)氮化镓与金刚石具有相似的晶体结构,氮化镓中氮原子与镓原子之间以_______键相结合,氮化镓属于_______晶体。
(3)下列说法正确的是________
A.第一电离能:As < Ga B.砷和镓都属于p区元素
C.电负性:As < Ga D.半导体GaP、SiC与砷化镓为等电子体
(4)① 砷化镓是将(CH3)3Ga和AsH3用MOCVD(金属有机物化学气相淀积)方法制备得到的,该反应在700℃进行,反应的方程式为:______________________________。
②反应物AsH3分子的几何构型为_________,(CH3)3Ga中镓原子杂化方式为___。
(5)实验测得AsH3沸点比NH3低,其原因是:___________________________。
(6)下图是氮化镓的晶胞模型,氮化镓为立方晶胞,氮化镓的密度为d g/cm3。列式计算氮化镓晶胞边长a的表达式:a=______cm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等温等压下,关于等质量D2、T2两种气体的下列叙述中不正确的是()
A. 密度之比2:3 B. 质子数之比3:2 C. 中子数之比3:4 D. 体积之比2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列8种有机物:①CH2=CH2;②![]() ;③
;③![]() ;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦
;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦![]() ;⑧CH3CH2OH。根据官能团的不同,有机物可分为( )
;⑧CH3CH2OH。根据官能团的不同,有机物可分为( )
A. 4类 B. 5类 C. 6类 D. 7类
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com