
【题目】以氮化镓(GaN)、砷化镓(GaAs)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点,如砷化镓灯泡寿命是普通灯泡的100倍,而耗能即为10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。请回答下列问题:
(1)镓为元素周期表第31号元素,基态镓原子的电子排布式为__________________,核外电子占据最高能层符号为________。
(2)氮化镓与金刚石具有相似的晶体结构,氮化镓中氮原子与镓原子之间以_______键相结合,氮化镓属于_______晶体。
(3)下列说法正确的是________
A.第一电离能:As < Ga B.砷和镓都属于p区元素
C.电负性:As < Ga D.半导体GaP、SiC与砷化镓为等电子体
(4)① 砷化镓是将(CH3)3Ga和AsH3用MOCVD(金属有机物化学气相淀积)方法制备得到的,该反应在700℃进行,反应的方程式为:______________________________。
②反应物AsH3分子的几何构型为_________,(CH3)3Ga中镓原子杂化方式为___。
(5)实验测得AsH3沸点比NH3低,其原因是:___________________________。
(6)下图是氮化镓的晶胞模型,氮化镓为立方晶胞,氮化镓的密度为d g/cm3。列式计算氮化镓晶胞边长a的表达式:a=______cm。

【答案】 1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1 N 共价 原子 BD (CH3)3Ga+AsH3![]() GaAs+3CH4 三角锥形或型 sp2 NH3分子间能形成氢键,而As电负性小,半径大,分子间不能形成氢键。
GaAs+3CH4 三角锥形或型 sp2 NH3分子间能形成氢键,而As电负性小,半径大,分子间不能形成氢键。 ![]()
【解析】(1)镓为元素周期表第31号元素,基态镓原子的电子排布式为1s22s22p63s23p63d104s24p1,核外电子占据最高能层符号为N,故答案为:1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1;N;
(2)金刚石是原子晶体,氮化镓与金刚石具有相似的晶体结构,氮化镓中氮原子与镓原子之间以共价键相结合,氮化镓也属于原子晶体,故答案为:共价;原子;
(3)A.同周期元素从左到右第一电离能逐渐增大,则第一电离能:As>Ga,故A错误;B.砷和镓的价层电子都为sp电子,位于周期表p区,故B正确;C.同周期元素从左到右电负性逐渐增大,则电负性:As>Ga,故C错误;D.GaP的价层电子为3+5=8,SiC的价层电子为4+4=8,GaAs价层电子数为3+5=8,则为等电子体,故D正确;故答案为:BD;
(4)①反应为(CH3)3Ga和AsH3,生成为GaAs,根据质量守恒可知还应有和CH4,反应的化学方程式为:(CH3)3Ga+AsH3![]() GaAs+3CH4,故答案为:(CH3)3Ga+AsH3
GaAs+3CH4,故答案为:(CH3)3Ga+AsH3![]() GaAs+3CH4;
GaAs+3CH4;
②AsH3中含有3个δ键和1个孤电子对,为三角锥形,(CH3)3Ga中Ga形成3个δ键,没有孤电子对,为sp2杂化,故答案为:三角锥;sp2;
(5)N原子半径较小,电负性较大,对应的NH3分子间能形成氢键,沸点较高,而As电负性小,半径大,分子间不能形成氢键,沸点较低,故答案为:NH3分子间能形成氢键,而As电负性小,半径大,分子间不能形成氢键;
(6)GaN晶胞中,Ga位于顶点和体心,所以含有Ga数为:8×![]() +1=2,N原子位于棱和体心,所以N数为:4×
+1=2,N原子位于棱和体心,所以N数为:4×![]() +1=2,GaN晶胞中含有两个GaN,晶胞边长为
+1=2,GaN晶胞中含有两个GaN,晶胞边长为![]() =
=![]() =
=![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】滴加新制氯水后,下列各组离子可能大量存在的是( )
A.Fe3+、Cl﹣、NO3﹣
B.Na+、HCO3﹣、SO42﹣
C.Ag+、NH4+、NO3﹣
D.Na+、SO32﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() 2C(g)+3D(g)在四种不同情况下的反应速率如下,其中表示
2C(g)+3D(g)在四种不同情况下的反应速率如下,其中表示
反应速率最快的是
A. v(A)=0.20mol·L-1·min-1 B. v(B)=0.30 mol·L-1·min-1
C. v(C)=0.40 mol·L-1·min-1 D. v(D)=0.50 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学知识填空:
(1)丙烷通过脱氢反应可得丙烯。
已知:①C3H8(g)===CH4(g)+C2H2(g)+H2(g) ΔH1=+156.6 kJ·mol-1
②C3H6(g)===CH4(g)+C2H2(g) ΔH2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)===C3H6(g)+H2(g)的ΔH=__________kJ·mol-1。
(2)0.5mol甲烷燃烧时,生成液态水和二氧化碳,同时放出445kJ的热量,写出甲烷的燃烧热的热化学方程式_________________________________________________
(3)请写出NH4Cl溶液中各离子浓度的大小关系式:___________________________________
(4)常温下,Na2CO3溶液呈碱性,原因是_____________________ (用离子方程式表示)。
(5)①醋酸在水溶液中的电离方程式为______________________。
②下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是_________(填字母序号)。
a. 滴加少量浓盐酸 b. 微热溶液 c. 加水稀释 d. 加入少量醋酸钠晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北魏贾思勰《齐民要术·作酢法》这样描述苦酒:“乌梅苦酒法:乌梅去核,一升许肉,以五升苦酒渍数日,曝干,捣作屑。欲食,辄投水中,即成醋尔。”下列有关苦酒主要成分的说法正确的是( )
A. 苦酒的主要溶质是非电解质 B. 苦酒的主要溶质是弱电解质
C. 苦酒的主要溶质是强电解质 D. 苦酒的溶液中只存在分子,不存在离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关,下列有关说法错误的是
A. 大量燃烧化石燃料是造成雾霾天气的原因之一
B. 从海水中提取物质都必须通过化学反应才能实现
C. 燃料脱硫和减少汽车尾气排放都能减少酸雨的产生
D. 用食醋可以除去热水壶内壁的水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用pH=m的盐酸滴定20mLpH=n的MOH溶液,且m+n=14,混合溶液的pH与盐酸体积(V)的关系如图所示。下列说法正确的是
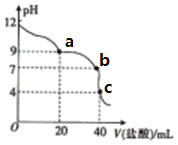
A. Kb(MOH)的数量级为10-11
B. 由c点可算得m=14/3
C. b点溶液呈中性,此时c(Cl-)=c(M+)
D. a点:c(Cl-)>c(M+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填写下列空格
①9gH2O含H原子的物质的量为_____________mol;
②标准状况下,体积为11.2 L 的CO2所含原子的总数是_______________
③等质量的O2和O3所含原子个数比为________
④8.4g NaHCO3 正好与20mL盐酸完全反应。此盐酸的物质的量浓度是__________,产生的CO2在标准状况下的体积是_____________ L
⑤ 用单线桥法表示反应:2KMnO4+16HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O转移电子的方向和数目____________________________________________________。
⑥写出离子反应方程式CO2 + 2OH-= CO32-+ H2O所对应的一个化学方程式:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com