
����Ŀ����.�Ӻ�ˮ�õ��Ĵ�ʳ��ˮ�г���Ca2����Mg2����SO42-����Ҫ�����ᴿ�����к�����CaCl2��MgSO4�Ĵ�ʳ��ˮ���ڳ�ȥ���������ɳ֮��Ҫ��4���Լ������ᡢ��Na2CO3����NaOH����BaCl2����ȥʳ��ˮ��Ca2����Mg2����SO42-���ᴿ�IJ�������ͼ����Լ��������ͼ��
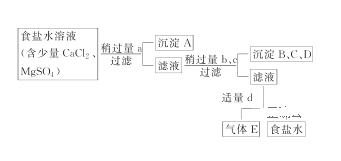
ͼ��a��b��c��d�ֱ��ʾ����4���Լ��е�һ�֣��Իش�
(1)����A��������________��
(2)�Լ�d��________���ж��Լ�d�Ѿ������ķ�����___________________��
��������d����Һ�з�����Ӧ�����ӷ���ʽΪ___________________________��
(3)�����������������˳�����A��B��C��Dʱ�����õ�________(�����)�������۵�������________��
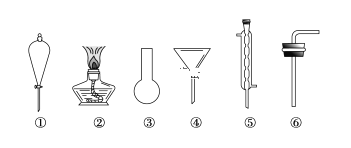
��.��ˮ�������ɺ�ˮ��õ�ˮ�ij��÷���֮һ����ʵ���������һ������װ�ÿ϶���Ҫ���������е�һ���֣�����ȷ����________(�����)��
��.�������������ʾ����������Եõ���ˮ�����ӵ�ˮ����ȡ�⣬��Ҫ���������е�________(�����)������������Ϊ________����õ�ˮ�м������Ȼ�̼����ȡ�ⵥ�ʵ�ʵ�����Ϊ________��
���𰸡����ᱵ��������þ ���� ��Һ�в��ٲ������� OH����H��=H2O��CO32-��2H��=CO2����H2O �� Բ����ƿ �ڢۢݢ� �� ��Һ©�� ��ȡ��Һ
��������
��.��������ӻ��뱵�������ɳ���������þ���ӻ������������Ӻ�̼����������ɳ����������ӻ���̼����������ɳ����������Թ�����a����һ�ֳ�����aΪ�Ȼ������õ��ij���AΪ���ᱵ����Һ�м��Թ������������ƣ���þ��������������þ�����������Թ���̼���ƣ������ӡ��������ı���������̼��ơ�̼�ᱵ�������ʳ���B��C��D�ֱ�Ϊ������þ��̼��ơ�̼�ᱵ��������������������Գ�ȥ������̼���ƺ��������ƣ�
(1)���ݼ�����Լ�ȷ�����ɳ���A��4���Լ��������Na2CO3����NaOH����BaCl2����ȥʳ��ˮ��Ca2+��Mg2+��SO42-�������Լ���˳���Ǣܢۢڢ٣�
(2)����������Ժ�̼�������֮��ķ�Ӧ�������ش�
(3)���ݹ���ʵ���õ��������Լ���������������װ����Ҫ�������У��ƾ��ơ�������ƿ���������������ܡ�ţ�ǹܡ���ƿ�������ش�
��.��������װ����Ҫ���������ش�
��.��ȡ��Һ����ʹ�õ������Ƿ�Һ©����
��.þ���������������ӳ���������������������ƿ��Խ�þ���ӳ���������������ñ����ӳ���������������Ȼ������Խ���������ӳ����������ȳ�þ���ӣ������ȳ���������Ӷ��У���������̼������ӳ������������Ӽ���̼����ת��Ϊ���������Ǽ����̼����Ҫ���ڼ�����Ȼ���֮������̼���ƻ��ȥ��Ӧʣ����Ȼ��������Ӷ������ˣ��ٽ��й��ˣ�����ټ��������ȥ��Ӧʣ������������Ӻ�̼������ӣ�
(1)4���Լ��������Na2CO3����NaOH����BaCl2����ȥʳ��ˮ��Ca2+��Mg2+��SO42-�������Լ���˳���Ǣܢۢڢ٣��Ȼ������Խ���������ӳ�������Ӧ�Ļ�ѧ����ʽΪ��MgSO4+BaCl2�TBaSO4��+MgCl2������AΪ��BaSO4��
(2)�Լ�d�����ᣬĿ���dz�ȥ��Һ�к��еĹ���OH-��CO32-��������Ժ�̼�������֮�䷴Ӧ����ˮ�Լ�������̼�������ٲ���������̼ʱ��֤�������Ѿ��������漰�����ӷ�Ӧ����ʽΪOH����H��=H2O��CO32-��2H��=CO2����H2O��
(3)����ʵ���õ���������©�������������ձ��ȣ�����ʵ��װ�ã����˳�����A��B��C��Dʱ�����õ�©������װ�âܣ�װ�â�ΪԲ����ƿ��
��.����װ����Ҫ�������У��ƾ��ơ�������ƿ���������������ܡ�ţ�ǹܡ���ƿ���ʴ�Ϊ�ڢۢݢޣ�
��.�ӵ�ˮ����ȡ�⣬���Բ�ȡ��ȡ��Һ������ʹ�õ���ȡ�������Ȼ�̼��ʹ�õ������Ǣ٣�������Ϊ��Һ©����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��E��F�����ܱ������У���һ�������·�����Ӧ��E(s)+4F(g)![]() G(g)����֪�÷�Ӧ��ƽ�ⳣ��ֵ���±���ʾ������˵����ȷ����
G(g)����֪�÷�Ӧ��ƽ�ⳣ��ֵ���±���ʾ������˵����ȷ����
�¶ȡ� | 25 | 80 | 230 |
ƽ�ⳣ��ֵ | 5��104 | 2 | 1.9�� 10��5 |
A.������Ӧ��������Ӧ
B.25��ʱ����ӦG(g)![]() E(s)+4F(g)��ƽ�ⳣ��ֵ��0.5
E(s)+4F(g)��ƽ�ⳣ��ֵ��0.5
C.��80��ʱ�����ijʱ�̣�F��GŨ�Ⱦ�Ϊ0.5 mol��L��1�����ʱv(��)��v(��)
D.���º����£����������ٳ�������G(g)������ƽ��ʱ��G������ٷֺ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ�ס��ҡ�����λͬѧ��ȡ����������ʵ����̡�
��ʵ��Ŀ�ģ���ȡ����������
��ʵ��ԭ�����ס��ҡ�����λͬѧ����ȡ�Ҵ���������Ũ�����Ϲ��ȵķ�����ȡ����������
1.��װ����ƣ��ס��ҡ�����λͬѧ�ֱ��������������ʵ��װ��:
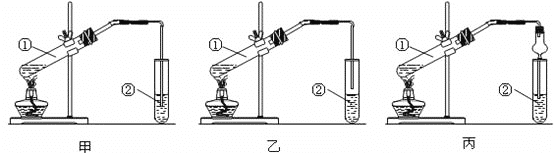
��Ӽס�����λͬѧ��Ƶ�װ����ѡ��һ����Ϊʵ������ȡ����������װ�ã���Ӧѡ���װ����____(����������������)����ͬѧװ���е����θ���ܣ��������������⣬��һ��Ҫ������______��
2.��ʵ�鲽�裩
(1)��ѡ���װ����װ���������Թ����ȼ���amLCH3CH218OH���ܶ�Ϊ��g/cm-3�������ı�����(CH3COOH)��������������2mLŨH2SO4;
(2)���Թ̶ܹ�������̨��;
(3)���Թܢ��м��������ı���Na2CO3��Һ;
(4)�þƾ��ƶ��Թܢټ���;
(5)���۲쵽�Թܢ�������������ʱ��Ϊ��Ӧ������ɡ�
���������ۣ�
a.������(1)װ��ʵ��װ�ã�����ҩƷǰ��Ӧ______��
b.��(5)�У����۲쵽�Թܢ�����______����ʱ��Ϊ��Ӧ������ɡ�
c.�����Թܢ��еĻ������Եõ���Ʒ������δ��Ӧ��������Ҵ���ʵ�������������:
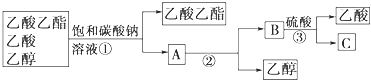
������ʵ����������У����漰�Ģ٢ڢ����η�������ֱ��ǣ�______��
d.��֪�����봼��������Ӧ�У���Ӧ��ԭ������ʧȥ�ǻ�����ʧȥ��ԭ�ӽ�ϳ�ˮ����д���Թܢ�����������������Ӧ�Ļ�ѧ����ʽ(ע����Ӧ����)_____________��
���õ���������������bg����ʵ�������������IJ��ʣ�______����a��b������ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С����ʵ����̽�����������(NH2COONH4)�ֽⷴӦƽ�ⳣ����ˮ�ⷴӦ���ʵIJⶨ��
(1)��һ���������İ�������粒����������Ƶ��ܱ����������(��������������䣬��������������Բ���)���ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4(s)![]() 2NH3(g)��CO2(g)��ʵ���õIJ�ͬ�¶��µ�ƽ�����������±���
2NH3(g)��CO2(g)��ʵ���õIJ�ͬ�¶��µ�ƽ�����������±���
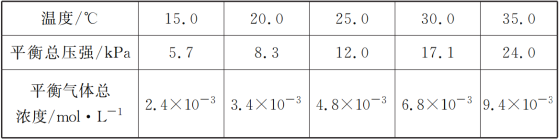
�ٿ����жϸ÷ֽⷴӦ�Ѿ��ﵽƽ�����___________
A. 2v(NH3)��v(CO2)
B. �ܱ���������ѹǿ����
C. �ܱ������л��������ܶȲ���
D. �ܱ������а����������������
�ڸ��ݱ������ݣ���ʽ����25.0 ��ʱ��������淋ķֽ�ƽ�ⳣ������ʽΪ________��ƽ�ⳣ��Ϊ________��
��ȡһ�����İ�������粒������һ�����������ܱ���������У���25.0 ���´ﵽ�ֽ�ƽ�⡣���ں�����ѹ�������������������粒��������_______ (����������������������������)��
�ܰ�������立ֽⷴӦ���ʱ���H________0(����������������������)���ر���S______0(����������������������)��
(2)��֪��NH2COONH4��2H2O![]() NH4HCO3��NH3��H2O��
NH4HCO3��NH3��H2O��
���о�С��ֱ������ݲ�ͬ��ʼŨ�ȵİ����������Һ�ⶨ��ˮ�ⷴӦ���ʣ��õ�c(NH2COO-)��ʱ��ı仯������ͼ��ʾ��
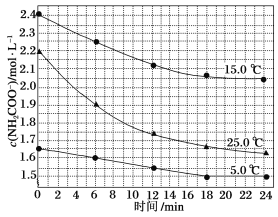
�ݼ���25.0 ��ʱ��0��6 min���������ˮ�ⷴӦ��ƽ�����ʣ�_______
����ͼ����Ϣ�����˵����ˮ�ⷴӦ�������¶����߶�����25.0 ��ʱ��Ӧ�����ʼŨ�Ƚ�С����0��6 min��ƽ����Ӧ����(���ߵ�б��)�Ա�15.0 ��ʱ��________(������������С��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£���N2O��CO2��ɵĻ��������ܶ���C2H4��N2��H2��ɵĻ�������ܶȵ� 2������C2H4��N2��H2��ɵĻ��������H2����������Ϊ
A. 3/13 B. 10/13 C. ����3/13����10/13 D. 3/143
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ�����KClO3��50mLŨ���ᷴӦ��ȡCl2����Ӧԭ�����£�
KClO3+HCl��KCl+Cl2��+H2O
(1)��ƽ������ѧ����ʽ����˫���ű������ת�Ʒ�������Ŀ__________________��
(2)Ũ������������Ӧ�б��ֳ�����������__����ѡ���ţ�
A��ֻ�������� B��ֻ�л�ԭ�� C����ԭ�Ժ����� D�������Ժ�����
(3)������0.1mol Cl2����ת�Ƶ��ӵ����ʵ���Ϊ_______��������λС����
(4)����Ӧ��HCl��������ֻ��50%������������Ȼ�ԭ����Ȼ�ԭ�����7.1gʱ��Ũ��������ʵ���Ũ��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��ģ�ҵ��Ư�ۣ��������ͼ��ʵ��װ�á��ش��������⣺

��1����װ��������a��������____________________��
��2��д��װ�â��з�Ӧ����ʽ�����˫����____________________��
��3��װ�â��б���ʳ��ˮ��������__________________________��
��4��װ�â���ȡƯ�۵Ļ�ѧ����ʽ��_____________��
��5��Ư�۵�Ư��ԭ����___________________________���û�ѧ����ʽ��ʾ����
��6����ѧʵ���г���ʪ��ĵ��۵⻯����ֽ�����Ƿ���Cl2������д����������з����ķ�Ӧ����ʽ ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п����صĸ���Ϊп������Ϊ���������������KOH����ط�ӦΪZn��Ag2O��H2O=Zn(OH)2��2Ag����п�����Ϊ��Դ�������������Һұ��������װ����ͼ��ʾ��
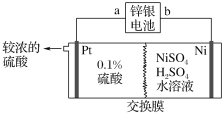
����˵����ȷ���ǣ� ��
A.װ����ʹ�������ӽ���Ĥ
B.п�����a����ӦʽΪAg2O��H2O��2e��=2Ag��2OH��
C.���������ϡ���ᣬ����õ��Ƚ�Ũ������
D.��п������ܽ�13gп�������������������Ϊ5.9g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ž��з���Ԫ��������150���ꡣ�±���Ԫ�����ڱ���һ���֣�W��X��Y��ZΪ����������Ԫ�أ�W��X������ϼ�֮��Ϊ8������˵���������

A. ԭ�Ӱ뾶��W<X
B. ���³�ѹ�£�Y����Ϊ��̬
C. ��̬�⻯�����ȶ��ԣ�Z<W
D. X������������ˮ������ǿ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com