
分析 向该溶液中加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子,在酸性溶液中AlO2-、CO32-离子因发生反应生成弱电解质而不能存在,而后才有沉淀.能够生成沉淀的是Fe3+离子、Fe2+离子或Al3+离子中的一种或几种,结合溶液的电中性和Fe2+离子的还原性以及NO3-离子的氧化性做进一步的推断.
解答 解:向该溶液中加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子;
在酸性溶液中AlO2-、CO32-离子分别与H+离子反应生成Al(OH)3沉淀、CO2气体而不能存在;
根据溶液的电中性可知一定含有阴离子,则一定含有NO3-;
而后才有沉淀.能够生成沉淀的是Fe3+离子、Fe2+离子或Al3+离子中的一种或几种,但在酸性条件下Fe2+离子与NO3-离子发生氧化还原反应而不能共存,则一定不含Fe2+离子;
综上所述,溶液中一定含有H+离子、NO3-离子,一定没有AlO2-、CO32-、Fe2+离子,Fe3+离子、Al3+离子至少有一种,
故答案为:AlO2-、CO32-、Fe2+.
点评 本题考查常见离子的检验,注意从反应的现象推断离子的存在性,把握物质的性质和离子的检验方法是做本题的关键,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
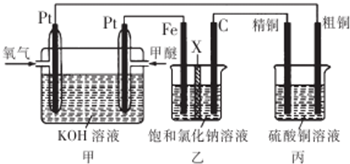
| A. | 通入氧气的一极为正极,发生的电极反应为O2-4e -+2H2O═4OH- | |
| B. | 乙装置中铁电极为阴极,电极反应式为Fe-2e -═Fe2+ | |
| C. | 反应一段时间后,乙装置中生成的氢氧化钠在铁极区 | |
| D. | 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
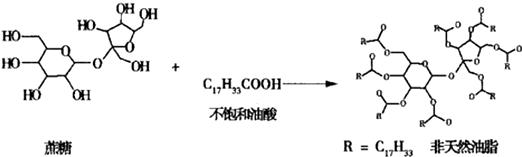
| A. | 该非天然油脂与氢氧化钠溶液共热,产物可与溴的四氯化碳溶液反应 | |
| B. | 天然油脂、蔗糖、非天然油脂都能发生水解反应 | |
| C. | 蔗糖、葡萄糖分别与银氨溶液水浴加热反应,有相同的实验现象 | |
| D. | 植物油、非天然油脂都可以与H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{a}^{b}$R | B. | ${\;}_{a}^{a+b}$R | C. | ${\;}_{a-m}^{a+b-m}$R | D. | ${\;}_{a+m}^{a+b+m}$R |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 通CO的一极是电池的负极 | |
| B. | 负极发生的电极反应是:O2+2CO2+4e-═2CO32- | |
| C. | 正极发生的电极反应是:CO+CO32--2e-═2CO2 | |
| D. | 正极发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com