
分析 (1)发生反应有:2Na2O2+2H2O=4NaOH+O2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)生成的气体为氧气与氢气,过氧化钠与Al都反应,令过氧化钠与Al的物质的量分别为x mol、y mol,根据二者质量之和及生成气体的体积之和列方程,据此计算解答;
(3)结合方程式计算判断NaOH是否完全反应、生成偏铝酸钠的物质的量,确定NaOH物质的量,再根据c=$\frac{n}{V}$计算.
解答 解:(1)发生反应有:2Na2O2+2H2O=4NaOH+O2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)发生反应有:2Na2O2+2H2O=4NaOH+O2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,生成的气体为氧气与氢气,
令过氧化钠与Al的物质的量分别为x mol、y mol,过氧化钠与Al都反应,则:
2Na2O2+2H2O=4NaOH+O2↑,
xmol 2xmol 0.5xmol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
ymol ymol ymol 1.5ymol
所以$\left\{\begin{array}{l}{78x+27y=18.3}\\{0.5x+1.5y=\frac{5.6}{22.4}}\end{array}\right.$
解得:x=0.2,y=0.1,
故生成氧气与氢气的体积之比为0.5×0.2mol:1.5×0.1mol=2:3,
故答案为:氧气、氢气;2:3;
(3)由方程式可知,过氧化钠反应生成氢氧化钠为2×0.2mol=0.4mol,Al反应消耗的NaOH为0.1mol、生成的偏铝酸钠为0.1mol,故溶液中氢氧化钠为0.4mol-0.1mol=0.3mol,
溶液中氢氧化钠的物质的量浓度=$\frac{0.3mol}{0.1L}$=3mol/L,
偏铝酸钠的物质的量浓度=$\frac{0.1mol}{0.1L}$=1mol/L,
答:溶液中氢氧化钠的物质的量浓度为3mol/L,偏铝酸钠的物质的量浓度为1mol/L.
点评 本题考查混合物的有关计算,难度中等,注意题目中物质全部反应,注意题目涉及过量计算,充分利用方程式计算.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是显影技术中的中间体.回答下列问题:
)是显影技术中的中间体.回答下列问题: .
.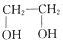 )可合成环酯,该反应的化学方程式为
)可合成环酯,该反应的化学方程式为 +
+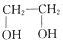 $→_{△}^{浓H_{2}SO_{4}}$2H2O+
$→_{△}^{浓H_{2}SO_{4}}$2H2O+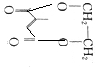 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
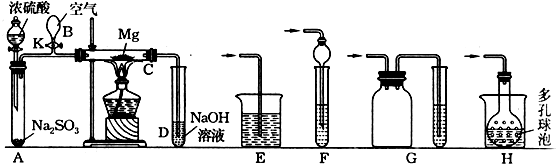
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸雨是指pH<7的酸性降水 | |
| B. | 淡水的密度小于海水的密度 | |
| C. | 蒸馏法是海水淡化的方法之一 | |
| D. | 融化的雪水中矿物质含量比深井水中的少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、HCO3-、SO42-、Cl- | B. | CO32-、Cl-、K+、Na+ | ||
| C. | Na+、SO42-、CO32-、Cl- | D. | SO42-、Fe3+、Na+、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com