
| A.铁、铜都有剩余,溶液中只有Fe2+ |
| B.铁、铜都不剩余,溶液中可能有Fe3+、一定有Fe2+和Cu2+ |
| C.铁有剩余、铜没剩余,溶液中只有Fe2+、Cu2+ |
| D.铁没剩余、铜有剩余,溶液中一定没有Fe3+ |
 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源:不详 题型:单选题
| A.镁和铁 | B.镁和铝 | C.铁和锌 | D.钠和镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
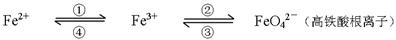
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2 :3 | B.3 :2 | C.1 :2 | D.2 :1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A | B | C | D |
| 将二氧化硫通入到一定量氯水中 | 将氨水滴入到一定量氯化铝溶液中 | 常温下将铜粉加入到一定量浓硝酸中 | 常温下将铁粉加入到一定量浓硝酸中 |
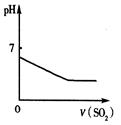 | 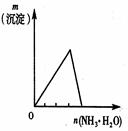 |  | 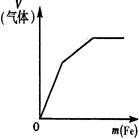 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②④⑤ | B.①③⑥ | C.①②⑥ | D.①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.线段BD表示Fe3+物质的量的变化 |
| B.原混合溶液中FeBr2的物质的量为6mol |
| C.当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com