
【题目】已知:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ·mol-1。在恒容密闭容器内,投入2mol N2和6mol H2发生反应,当反应达到平衡状态时,下列说法不正确的是
2NH3(g) △H=-92.4 kJ·mol-1。在恒容密闭容器内,投入2mol N2和6mol H2发生反应,当反应达到平衡状态时,下列说法不正确的是
A. 当其他条件不变的情况下,升高温度,原有的平衡被破坏,逆反应速率增大,正反应速率减小
B. 一定存在2v(H2)正=3 v(N2)逆
C. 反应过程中可能放出92.4 kJ的热量
D. 容器内混合气体的平均相对分子质量不再发生变化时,说明反应达到平衡状态
【答案】A
【解析】
A.升高温度时,正逆反应速率均增大,由于正反应为放热反应,则正反应增大的程度大于逆反应;
B.达到平衡状态时,v(N2)正= v(N2)逆,则2v(H2)正=3 v(N2)逆成立;
C.若达到平衡状态时,氮气的转换率为50%时,则放出92.4 kJ的热量;
D.若反应达到平衡状态时,则气体的物质的量不再改变,则M=m/n不变;
A.升高温度时,正逆反应速率均增大,由于正反应为放热反应,则正反应增大的程度大于逆反应,A错误;
B.达到平衡状态时,v(N2)正= v(N2)逆,则2v(H2)正=3 v(N2)逆成立,B正确;
C.若达到平衡状态时,氮气的转换率为50%时,则放出92.4 kJ的热量,C正确;
D.若反应达到平衡状态时,则气体的物质的量不再改变,则M=m/n不变,D正确;
答案为A


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是( )
A. 电子通过外电路从b极流向a极
B. b极上的电极反应式为:O2+2H2O+4e-===4OH-
C. 每转移0.1 mol电子,消耗标准状况下1.12 L的H2
D. H+由b极通过固体酸电解质传递到a极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5 mL 0.005 mol/L FeCl3溶液和5 mL 0.015 mol/L KSCN溶液混合,达到平衡后呈红色。再将混合液分为5份,分别进行如下实验:
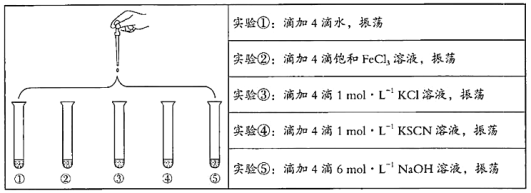
下列说法不正确的是
A. 对比实验①和②,为了证明增加反应物浓度,平衡发生正向移动
B. 对比实验①和③,为了证明增加反应物浓度,平衡发生逆向移动
C. 对比实验①和④,为了证明增加反应物浓度,平衡发生正向移动
D. 对比实验①和⑤,为了证明减少反应物浓度,平衡发生逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0,下列分析中不正确的是( )
CO2(g)+H2(g) ΔH<0,下列分析中不正确的是( )

A. 图Ⅰ研究的是t0时升高温度对反应速率的影响
B. 图Ⅱ研究的是t0时增大压强(缩小容积)或使用催化剂对反应速率的影响
C. 图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂
D. 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释相关的离子方程式错误的是
A. H2S溶于水:H2S+H2O![]() HS-+H3O+
HS-+H3O+
B. 向Na2S2O3溶液中加入稀硫酸:S2O3-+2H+=S↓+SO2↑+H2O
C. NH4Cl溶液呈酸性:NH4++H2O=NH3·H2O+H+
D. K2Cr2O7溶于水:Cr2O7-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往1.0 mol·L-1KI溶液中加入固体I2,发生反应:I2(aq)+I-(aq)![]() I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是
I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是

A. 该反应的△H>0
B. a、c两点对应的I-反应速率相等
C. b点时0~10s I-的平均反应速率为0.04mol·L-1·s-1
D. d点时该反应在对应温度下处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: ①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol;
②Na2O2(s)+CO2(g)=Na2CO3(s)+![]() O2(g) ΔH=-226 kJ/mol
O2(g) ΔH=-226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为 283 kJ
B.反应①正反应活化能与逆反应活化能之差为+566 kJ/mol
C.反应 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D. CO(g)与 Na2O2(s)反应放出 509 kJ 热量时,电子转移数为 6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸有许多重要的性质,工业上可以通过硫铁矿(主要成分是FeS2)制取。
(1)硫原子核外电子占有______种能量不同的轨道。H2SO4属于______晶体。
(2)非金属性:S____O(选填“>”、“<”或“=”)。试用一个实验事实说明___________________。
(3)接触法制硫酸工业中,其主要反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)![]() 2SO3(g)+190kJ该反应的平衡常数表达式是K=_____________,该反应450℃时的平衡常数______500℃时的平衡常数(选填“大于”、“小于”或“等于”)。
2SO3(g)+190kJ该反应的平衡常数表达式是K=_____________,该反应450℃时的平衡常数______500℃时的平衡常数(选填“大于”、“小于”或“等于”)。
(4)在一个固定容积为10L的密闭容器中充入0.40mol SO2和0.20 O2,半分钟后达到平衡,测得容器中含SO3 0.36mol,则v(SO2)=____mol·![]() ·min
·min![]() ;若继续通入0.40mol SO2和0.20mol O2,则平衡______移动(选填“向正反应方向”、“向逆反应反向”或“不”)。
;若继续通入0.40mol SO2和0.20mol O2,则平衡______移动(选填“向正反应方向”、“向逆反应反向”或“不”)。
(5)该热化学方程式的意义是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是________________________,还可使用___________代替硝酸。
(2)沉淀A的主要成分是_________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________________________________。
(3)加氨水过程中加热的目的是___________________________________________。
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4- +H+ +H2C2O4 →Mn2+ +CO2 +H2O。实验中称取0.400 g水泥样品,滴定时消耗了0.0500 mol·L-1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com