
����Ŀ���ȼ��⾫�Ƶı���ʳ��ˮ�����õ���Ʒ����ȡƯ�۵ȡ�
��1����������к���SO42��������ʱ�������Լ���ȥSO42�������Լ�����ѡ��______��
A��Ba��OH��2 �� B��Ba��NO3��2 �� C��BaCl2
��2����ⱥ��ʳ��ˮ�����Ļ�ѧ����ʽ_________________��
��3����������������������Һ��ȡ��84������Һ�Ļ�ѧ����ʽ____________��
��4��Ư���ڿ����о��ú����ʵĻ�ѧ����ʽ_____________��
���𰸡� B 2NaCl + 2H2O![]() 2NaOH+H2��+Cl2�� Cl2+2NaOH=NaCl+NaClO+H2O Ca(ClO)2+CO2+H2O=CaCO3+2HClO
2NaOH+H2��+Cl2�� Cl2+2NaOH=NaCl+NaClO+H2O Ca(ClO)2+CO2+H2O=CaCO3+2HClO
��������������Ҫ�������ӷ�Ӧ��
��1����������к���SO42��������ʱ�������Լ���ȥSO42�����Լ�Ba��NO3��2������������NO3-�����Ը��Լ�����ѡ��B��
��2����ⱥ��ʳ��ˮ������Ӧ�Ļ�ѧ����ʽΪ2NaCl + 2H2O![]() 2NaOH+H2��+Cl2����
2NaOH+H2��+Cl2����
��3����������������������Һ��ȡ��84������Һ����Ư�����ƣ���Ӧ�Ļ�ѧ����ʽΪCl2+2NaOH=NaCl+NaClO+H2O��
��4��Ư���ڿ����о��ú����ʵĻ�ѧ����ʽΪCa(ClO)2+CO2+H2O=CaCO3+2HClO��


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��һ������ɱ��Ч�ʸߡ�������ȾС��ˮ��������ʵ���ҿ�ͨ�����·�Ӧ�Ƶ�
��һ������ɱ��Ч�ʸߡ�������ȾС��ˮ��������ʵ���ҿ�ͨ�����·�Ӧ�Ƶ�![]() :
:![]()
![]()
![]() ,����˵������ȷ����( )
,����˵������ȷ����( )
A. ![]() �ڷ�Ӧ���ǻ�ԭ��
�ڷ�Ӧ���ǻ�ԭ��
B. ![]() �μӷ�Ӧ,�ڱ�״�����ܵõ�22.4L����
�μӷ�Ӧ,�ڱ�״�����ܵõ�22.4L����
C. �ڷ�Ӧ��![]() �Ȳ���������Ҳ���ǻ�ԭ��
�Ȳ���������Ҳ���ǻ�ԭ��
D. ![]() �μӷ�Ӧ��
�μӷ�Ӧ��![]() ����ת��
����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��

��I������������ʵ���Ũ����________��
��II��ij��ѧ��ȤС������������ʵ�ʵ��̽��ʱ����Ҫ240mL1.84mol/L��ϡ���ᡣ�ɹ�ѡ��������ɣ��������� ����ƿ ���ձ� ����ͷ�ι� ����Ͳ ������ƿ ��������ƽ ��ҩ�� ��մ��������⣺
(1) ���������У�������ϡ����ʱ�ò�������________ (����ţ�
(2) �����㣬��:Ũ��������Ϊ_____________�����У�
��10mL ��50mL ��100mL���ֹ�����Ͳ����ѡ�õ���Ͳ��______ (����ţ�
�������������ϡ�͵�ʵ������У�___________________��
��3��������ϡ��������У�����������ȷ�����������ƫ�ߵ��У�_________ (����ţ�
��ϴ����ȡŨ�������Ͳ������ϴ��Һת�Ƶ�����ƿ��
������ƿ��1moll/Lϡ������ϴ
��ת��ǰ������ƿ�к�����������ˮ
����.ȡŨ����ʱ���Ӷ��̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����ù���NaOH����0.5 mol/L��NaOH��Һ500 mL�����ձ���100 ml��Ͳ������ƿ��ҩ�עݲ�������������ƽ����ƿ
��1������ʱ������ʹ�õ�������_____________(�����)����ȱ�ٵ�������__________________��
��2�������Ƶ�ת�ƹ�����ijѧ��������ͼ��������ָ�����еĴ���______________��____________��
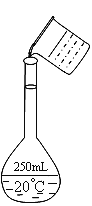
��3������ʱ��һ��ɷ�Ϊ���¼�������ٳ����ڼ�����ܽ��ҡ�Ȣ�ת�Ƣ�ϴ�Ӣ߶��ݢ���ȴ������ȷ�IJ���˳��Ϊ_________________��
��4�����в�����ʹ���Ƶ���ҺŨ��ƫ�͵���___________(����ĸ)
A.û�н�ϴ��Һת�Ƶ�����ƿ B.ת�ƹ�������������Һ����
C.����ƿϴ����δ���� D.����ʱ���ӿ̶���
E.����NaOH�������Na2O����
��5��������ƿʹ�÷����У����в�������ȷ����(�����) ___________
A.ʹ������ƿǰ������Ƿ�©ˮ
B.����ƿ������ˮϴ�������ü�Һ��ϴ
C.���������ƹ���ֱ�ӷ�����ƽ���̵���ֽ�ϣ�ȷ�����������ձ����ܽ������ע������ƿ��
D.���ݺ�����ƿ������ʳָ��סƿ��������һֻ�ֵ���ָ��סƿ�ף�������ƿ��תҡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2������һ�������¿������þ��Ӧ���ɱ���һ�������¿����γ�CO2���壬�������仯��������Ҫ�˷������÷ֱ���
A.�������������� B.�����������Ӽ�������
C.���Ӽ��������������� D.���Ӽ������������Ӽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݣ��ݴ�����˵����ȷ���� ( )

A. ����������ʵ���Ũ��Ϊ9.2mol/L
B. 1molCu�����������ᷴӦ����2g����
C. ����200mL4.6mol/L��ϡ������ȡ������50mL
D. ���������������ˮ��Ϻ�������Һ��Ũ�ȴ���9.2mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѪҺ�еĸ�����ƽ�����ٴ�ҽѧ�о�����Ҫ�����塣ij�о�С��Ϊ�ⶨѪҺ��Ʒ��Ca2���ĺ��������е�ʵ�����£�
����ȡ5.0 mLѪҺ��Ʒ�����������Ƴ�100 mL��Һ��
����ȡ10.0 mL��Һ���������(NH4)2C2O4��Һ��ʹCa2����ȫת����CaC2O4������
�۹��˲�ϴ�����õ�CaC2O4�������ù���ϡ�����ܽ⣬����H2C2O4��CaSO4ϡ��Һ��
�ܼ���0.001 mol��L��1������KMnO4��Һ��ʹH2C2O4��ȫ������ͬʱ����ʹ����ʯ��ˮ����ǵ���ɫ��ζ���壬��������KMnO4��Һ�����Ϊ2.00 mL��
��1����������õ��IJ��������в��������ձ�����Ͳ��________________________��
��2��������з�����Ӧ�����ӷ���ʽΪ_______________________________________��
��3��������з�����Ӧ�����ӷ���ʽΪ__________________________�����������뻹ԭ��������ʵ���֮��Ϊ___________________��
��4��Ѫ����Ca2���ĺ���Ϊ________g��mL��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪a��b��c�����л�������Ľṹ���£�![]() ��a����
��a����![]() ��b����
��b����![]() ��c�������й�˵������ȷ���ǣ� ��
��c�������й�˵������ȷ���ǣ� ��
A. a��b��c�ķ���ʽ��ΪC8H8 B. a��b��c��һ�ȴ�������Ϊ5��
C. a��b��c������H2�����ӳɷ�Ӧ D. a��b����ʹ����KMnO4��Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������춡������![]() )��һ�ֺϳ����ϣ�����һ�ֺϳ�·����ͼ:
)��һ�ֺϳ����ϣ�����һ�ֺϳ�·����ͼ:

��֪��R-CH=CH2![]() R-CH2CH2OH����ش��������⣺
R-CH2CH2OH����ش��������⣺
��1��A�Ļ�ѧ������______________��B�к��еĹ�����������________________��
��2����һ�������£�A��ˮ��ӦҲ��������B������һ��������÷�Ӧ�ķ�Ӧ����Ϊ___________��������һ��������Ľṹ��ʽΪ_____________________________��
��3��C�ɱ����Ƶ�Cu(OH)2����Һ������Ҳ���Ա�������������������д��C��������Һ��Ӧ�Ļ�ѧ����ʽ��_____________________________��
��4��D�ĺ˴Ź���������ʾΪ6��壬�ҷ����֮��Ϊ1��1��1��1��2��2����D�Ľṹ��ʽΪ_______________��D��ͬ���칹���ж��֣����б�����������������״��ȡ������������Na��Ӧ��ͬ���칹����_______�֣����������칹����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com