
【题目】在体积为V L的密闭容器中通入a mol CO和b mol O2 , 点燃充分反应后容器内碳原子数和氧原子数之比为( )
A.a:b
B.a:2b
C.a:(a+2b)
D.a:2(a+b)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质与水蒸气反应,生成一种黑色固体Y。请回答下列问题:
(1)X与A的稳定氧化物反应的化学方程式:__________。
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因__________。
(3)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为__________。将所得沉淀过滤、洗涤、灼烧,可得到__________g固体。
(4)为探究黑色固体Y的成分,两探究小组分别用黑色固体Y进行以下实验。
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色固体粉末加入稀盐酸 | 溶解,无气泡 | 溶解,无气泡 |
2 | 取步骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是__________。
②甲组步骤1中反应的离子方程式为__________。
③乙组步骤4中,溶液变红的原因为__________;溶液褪色可能的原因是__________;验证方法为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学家们合成了如下图所示的一系列的星烷,如三星烷、四星烷、五星烷等。下列说法正确的是
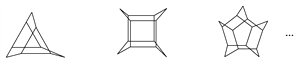
A. 它们的一氯代物均只有三种
B. 它们之间互为同系物
C. 三星烷与乙苯互为同分异构体
D. 六星烷的化学式为C18H24
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下式表示一种有机物的结构,关于它的性质的叙述中不正确的是

A. 它有酸性,能与Na2CO3溶液反应
B. 它可以水解,水解产物只有一种
C. 1mol该有机物最多能和8mol NaOH反应
D. 1mol该有机物最多能和8mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利尿酸在奥运会上被禁用,其结构简式如下图所示。下列叙述正确的是( )

A. 利尿酸衍生物利尿酸甲酯的分子式是C14H14Cl2O4
B. 利尿酸分子内处于同一平面的原子不超过10个
C. 1 mol利尿酸能与7 mol H2发生加成反应
D. 利尿酸能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合利用CO2、CO对构建低碳社会有重要意义。
(1) H2 和CO合成甲醇反应为:CO(g)+2H2(g)![]() CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为_______;10min内用H2表示的化学反应速率为_______;若要加快CH3OH的生成速率并提高CO的转化率,可采取的措施有_______(填一种合理的措施)。
CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为_______;10min内用H2表示的化学反应速率为_______;若要加快CH3OH的生成速率并提高CO的转化率,可采取的措施有_______(填一种合理的措施)。

(2) 二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g) +3H2(g) ![]() CH3OH(g) +H2O(g)+Q。
CH3OH(g) +H2O(g)+Q。
①该反应的平衡常数表达式为K=________。②在恒容密闭容器中使CO2和H2(物质的量之比为1∶3)发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如下图所示,则Q_________0(填“大于”或“小于”)
(3) 如下图所示,利用缺铁氧化物[如Fe0.9O]可实现CO2的综合利用。请说明该转化的2个优点_____________。若用1 mol缺铁氧化物[Fe0.9O]与足量CO2完全反应可生成________mol C(碳)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述中,错误的是
A.胶体的本质特征是其分散质粒子直径为1-100nm
B.胶体是胶状的纯净化合物
C.利用丁达尔效应可区分溶液和胶体
D.将饱和FeCl3溶液滴入沸水中,再煮沸可形成红褐色的胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com