
ЁОЬтФПЁПЛЏбЇЗДгІN2+3H22NH3ЕФФмСПБфЛЏШчЭМЫљЪОЃЌИУЗДгІЕФШШЛЏбЇЗНГЬЪНЪЧЃЈЁЁЁЁЃЉ 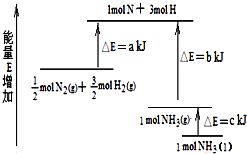
A.N2ЃЈgЃЉ+3H2ЃЈgЃЉ2NH3ЃЈlЃЉЁїH=2ЃЈaЉbЉcЃЉkJ/mol
B.N2ЃЈgЃЉ+3H2ЃЈgЃЉ2NH3ЃЈgЃЉЁїH=2ЃЈbЉaЃЉkJ/mol
C.0.5N2ЃЈgЃЉ+1.5H2ЃЈgЃЉNH3ЃЈlЃЉЁїH=ЃЈb+cЉaЃЉkJ/mol
D.0.5N2ЃЈgЃЉ+1.5H2ЃЈgЃЉNH3ЃЈgЃЉЁїH=ЃЈa+bЃЉkJ/mol
ЁОД№АИЁПA
ЁОНтЮіЁПНтЃКгЩЭМПЩвдПДГіЃЌЁїEЮЊЗДгІЕФЛюЛЏФмЃЌЗДгІШШЕШгкЗДгІЮяЕФЛюЛЏФмМѕЩњГЩЮяЕФЛюЛЏФмЃЌЫљвд ![]() N2ЃЈgЃЉ+
N2ЃЈgЃЉ+ ![]() H2ЃЈgЃЉ=NH3ЃЈgЃЉЁїH=ЃЈaЉbЃЉkJ/molЃЌМДN2ЃЈgЃЉ+3H2ЃЈgЃЉ2NH3ЃЈgЃЉЁїH=Љ2ЃЈbЉaЃЉ kJ/molЃЌЖј1molЕФNH3ЃЈgЃЉзЊЛЏЮЊ1molЕФNH3ЃЈlЃЉЗХГіЕФШШСПЮЊckJЃЌИљОнИЧЫЙЖЈТЩгаЃК
H2ЃЈgЃЉ=NH3ЃЈgЃЉЁїH=ЃЈaЉbЃЉkJ/molЃЌМДN2ЃЈgЃЉ+3H2ЃЈgЃЉ2NH3ЃЈgЃЉЁїH=Љ2ЃЈbЉaЃЉ kJ/molЃЌЖј1molЕФNH3ЃЈgЃЉзЊЛЏЮЊ1molЕФNH3ЃЈlЃЉЗХГіЕФШШСПЮЊckJЃЌИљОнИЧЫЙЖЈТЩгаЃК ![]() N2ЃЈgЃЉ+
N2ЃЈgЃЉ+ ![]() H2ЃЈgЃЉ=NH3ЃЈlЃЉЁїH=ЃЈaЉbЉcЃЉkJ/molЃЌМДЃКN2ЃЈgЃЉ+3H2ЃЈgЃЉ2NH3ЃЈ1ЃЉЁїH=2ЃЈaЉbЉcЃЉkJmolЉ1ЃЌЙЪAе§ШЗЃЛ
H2ЃЈgЃЉ=NH3ЃЈlЃЉЁїH=ЃЈaЉbЉcЃЉkJ/molЃЌМДЃКN2ЃЈgЃЉ+3H2ЃЈgЃЉ2NH3ЃЈ1ЃЉЁїH=2ЃЈaЉbЉcЃЉkJmolЉ1ЃЌЙЪAе§ШЗЃЛ
ЙЪбЁAЃЎ


 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаРызгдкЫЎШмвКжаФмДѓСПЙВДцЕФЪЧЃЈ ЃЉ
A.Na+ЁЂClЉЁЂHCO3ЉЁЂCa2+
B.OHЉЁЂNa+ЁЂMg2+ЁЂHCO3Љ
C.Na+ЁЂClЉЁЂH+ЁЂAg+
D.Na+ЁЂSiO32ЉЁЂH+ЁЂClЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЊСЫГ§ШЅДжбЮжаЕФCa2+ЁЂMg2+ЁЂSO42-МАФрЩГЃЌПЩНЋДжбЮШмгкЫЎЃЌШЛКѓНјааЯТСаЮхЯюВйзїЃКЂйЙ§ТЫЃЌЂкМг Й§СПNaOHШмвКЃЌЂлМгЪЪСПбЮЫсЃЌЂмМгЙ§СПNa2CO3ШмвКЃЌЂнМгЙ§СПBaCl2ШмвКЁЃе§ШЗЕФВйзїЫГађЪЧЃЈ ЃЉ
A.ЂкЂйЂмЂнЂлB.ЂмЂкЂнЂйЂлC.ЂкЂнЂмЂйЂлD.ЂнЂкЂйЂмЂл
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЬМЛЏбЇЪЧжИвдЗжзгжажЛКЌвЛИіЬМдзгЕФЛЏКЯЮя(ШчвЛбѕЛЏЬМЁЂЖўбѕЛЏЬМЁЂМзЭщЁЂМзДМЕШ)ЮЊдСЯЃЌгУЛЏЙЄЕФЗНЗЈжЦдьВњЦЗЕФЛЏбЇЬхЯЕЕФзмГЦЁЃЮвЙњФмдДБШНЯЗсИЛЃЌУКЕФЬНУїДЂСП6000вкЖжЃЌОгЪРНчЕкШ§ЮЛЃЌвђДЫЃЌЗЂеЙвЛЬМЛЏбЇгазХгХдНЕФЬѕМўКЭЙтУїЕФЧАЭОЁЃЧыЛиД№ЯТСагаЙиЮЪЬтЁЃ
(1)вбжЊдквЛЖЈЮТЖШЯТгаШчЯТЗДгІ:
I.C(s)+CO2(g)![]() 2CO(g)H1=akJ/mol
2CO(g)H1=akJ/mol
II.CO(g)+H2O(g)![]() H2(g)+CO2(g)ЁїH2=bkJ/mol
H2(g)+CO2(g)ЁїH2=bkJ/mol
III.C(s)+H2O(g)![]() CO(g)+H2(g)ЁїH3________ЁЃ
CO(g)+H2(g)ЁїH3________ЁЃ
(2)дквЛКуШнЕФУмБеШнЦїжаЃЌМгШыlmolCO(g)ЁЂ2molH2O(g)ЃЌЗЂЩњЗДгІCO(g)+H2O(g)![]() H2(g)+CO2(g) ЁїH ЃЌCOЕФЦНКтзЊЛЏТЪЫцЮТЖШЕФБфЛЏШчЭМЫљЪОЃК
H2(g)+CO2(g) ЁїH ЃЌCOЕФЦНКтзЊЛЏТЪЫцЮТЖШЕФБфЛЏШчЭМЫљЪОЃК

ЂйИУЗДгІЕФЁїH__0(ЬюЁА<ЁБЛђЁА>ЁБЁЃ)
ЂкдкФГЮТЖШЯТЃЌФмХаЖЯИУЗДгІЪЧЗёДяЕНЛЏбЇЦНКтзДЬЌЕФвРОнЪЧ________ЁЃ
a.ЛьКЯЦјЬхжаc(CO)ВЛБф b.c(CO)=c(CO2)
c.Іде§(H2O)=ІдФц(H2) d.ЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПВЛБф
ЂлAЕуЪБH2O(g)ЕФзЊЛЏТЪЮЊ__________ЁЃ
ЂмдкЬхЛ§ВЛБфЪБЃЌвЊдіДѓИУЗДгІЕФе§ЗДгІЫйТЪПЩВЩШЁЕФДыЪЉЪЧ_______(аДСНЬѕ)ЁЃ
ЂнAЕуЪБИУЗДгІЕФЦНКтГЃЪ§ЮЊ________(БЃСєЕНаЁЪ§ЕуКѓСНЮЛ)ЁЃ
ЂоШєдкИУШнЦїжаГфШы2molCOКЭ3molЫЎеєЦјНјааЗДгІЃЌДяЕНЦНКтЪБЫЎеєЦјЕФЬхЛ§ЗжЪ§гыH2ЕФЬхЛ§ЗжЪ§ЯрЕШЃЌдђЦНКтКѓCOЕФЬхЛ§ЗжЪ§ЮЊ_______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙ§ГЬВЛЩцМАЛЏбЇБфЛЏЕФЪЧ
A.КЃЫЎЩЙбЮB.ЙтКЯзїгУ
C.ИжЬњЩњатD.ОЦОЋШМЩе
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНќФъПЦбЇМвЬсГіЁАТЬЩЋздгЩЁБЙЙЯыЁЃАбКЌгаДѓСПCO2ЕФПеЦјДЕШыK2CO3ШмвКжаЃЌдйАбCO2ДгШмвКжаЬсШЁГіРДЃЌВЂЪЙжЎгыH2ЗДгІЩњГЩПЩдйЩњФмдДМзДМЁЃЦфЙЄвеСїГЬШчЯТЭМЫљЪОЃК
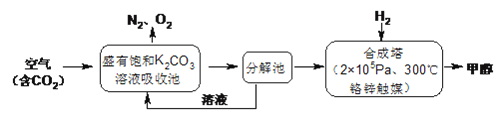
ЛиД№ЯТСаЮЪЬтЃК
(1)НјШыЗжНтГижажївЊЮяжЪЪЧ______ЃЛдкКЯГЩЫўжаЃЌШєзуСПЕФH2гыCO2ЗДгІЃЌЯћКФ4.4gCO2ЃЌЩњГЩЦјЬЌЕФH2OКЭCH3OHЃЌПЩЗХГі5370JЕФШШСПЃЌаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН________ЁЃ
(2)ИУЙЄведкФФаЉЗНУцЬхЯжСЫЁАТЬЩЋздгЩЁБЙЙЯыжаЕФЁАТЬЩЋЁБЃК Ђй_______ЃЛЂк_______ЁЃ
(3)вЛЖЈЬѕМўЯТЃЌЭљ2LКуШнУмБеШнЦїжаГфШы1.0molCO2КЭ3.0mol H2ЃЌдкВЛЭЌДпЛЏМСзїгУЯТЃЌЯрЭЌЪБМфФкCO2ЕФзЊЛЏТЪЫцЮТЖШБфЛЏШчЭМЫљЪОЃК
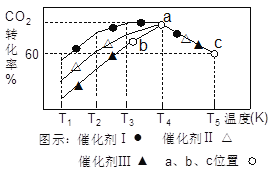
ЂйДпЛЏМСаЇЙћзюМбЕФЪЧ_______ЃЈЬюЁАДпЛЏМСIЁБЃЎЁАДпЛЏМСЂђЁБЃЌЁАДпЛЏМСЂѓЁБЃЉЁЃbЕуvЃЈе§ЃЉ______vЃЈФцЃЉЃЈЬюЁА>ЁБЃЌЁА<ЁБЃЌЁА=ЁБЃЉЁЃ
ЂкДЫЗДгІдкaЕуЪБвбДяЦНКтзДЬЌЃЌaЕуЕФзЊЛЏТЪБШcЕуИпЕФдвђЪЧ_________ЁЃcЕуЪБИУЗДгІЕФЦНКтГЃЪ§K=___________(БЃСєвЛЮЛаЁЪ§)ЁЃ
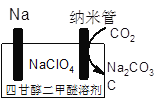
(4)ПЦбЇМвЛЙбаОПСЫРћгУЮТЪвЦјЬхжЦдьГфЕчЕчГиЃЌЯТЭМЮЊе§дкбаОПЕФNaЁЊCO2ПЩГфЕчЕчГиЪОвтЭМЃЌИУзАжУЗХЕчЪБЕФзмЗДгІЗНГЬЪНЮЊ_________ЁЃ
(5)МКжЊ25ЁцЪБH2CO3ЕФЕчРыЦНКтГЃЪ§ЮЊЃКKal =4.4ЁС10Ѓ7ЁЂKa2 =4.7ЁСl0ЃllЃЌдђЗДгІЃКHCO3Ѓ+H2O![]() H2CO3+ OHЃЕФЦНКтГЃЪ§K=________ЁЃ
H2CO3+ OHЃЕФЦНКтГЃЪ§K=________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ 
A.ЭМЂйжаЁїH1=ЁїH2+ЁїH3
B.ЭМЂкПЩгУгкжЄУїЪЕбщжаЩњГЩСЫввЯЉ
C.ЭМЂлБэЪОДзЫсШмвКЕЮЖЈNaOHКЭАБЫЎЛьКЯШмвКЕФЕчЕМТЪБфЛЏЧњЯп
D.ЭМЂмПЩБэЪОгЩCOЃЈgЃЉЩњГЩCO2ЃЈgЃЉЕФЙ§ГЬжавЊЗХГі566kJ ШШСП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУвЛЪјЙтееЩфФГвКЬхЪБЃЌВњЩњвЛЬѕЙтССЕФЭЈТЗЁЃИУвКЬхЪЧ
A.CuSO4ШмвКB.ЯЁбЮЫс
C.NaOHШмвКD.Fe(OH)3НКЬх
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕчНтдРэдкЛЏбЇЙЄвЕжагазХЙуЗКЕФгІгУЁЃЯжНЋЩшМЦЕФдЕчГиЭЈЙ§ЕМЯпгыЯТЭМжаЕчНтГиЯрСЌЃЌЦфжаaЮЊЕчНтвКЃЌXКЭYЪЧСНПщЕчАхАхЃЌдђЃК

(1)ШєXКЭYОљЮЊЖшадЕчМЋЃЌaЮЊБЅКЭNaClШмвКЃЌдђЕчНтЪБМьбщYЕчМЋЗДгІВњЮяЕФЗНЗЈЪЧ________________________ЁЃ
(2)ШєXЁЂYЗжБ№ЮЊЪЏФЋКЭЬњЃЌaШдЮЊБЅКЭЕФNaClШмвКЃЌдђЕчНтЙ§ГЬжаЩњГЩЕФАзЩЋЙЬЬхЮяжЪЕФЕчНтзмЗДгІЗНГЬЪНЮЊЃК________________ЃЌНЋЦфТЖжУдкПеЦјжаПЩЙлВьЕНЕФЯжЯѓЮЊ______ЁЃ
(3)ШєXКЭYОљЮЊЧщадЕчАхЃЌaЮЊвЛЖЈХЈЖШЕФСђЫсЭШмвКЃЌЭЈЕчвЛЖЮЪБМфКѓЃЌЯђЫљЕУШмвКжаМгШы0.1molCu(OH)2ЃЌЧЁКУЛжИДЕчНтЧАЕФХЈЖШЃЌдђЕчНтЙ§ГЬжазЊвЦЕФЕчзгЕФЮяжЪЕФСПЮЊ______ЁЃ
(4)ФГЭЌбЇЮЊСЫЪЙЗДгІ2HCl+2Ag=2AgC1+H2ЁќФмдкЩЯЪізАжУжаНјааЃЌдђЕчНтвКМАЕчМЋЗжБ№ЮЊЃК___________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com