
根据下表中的数据,结合学过的化学知识,判断下列说法正确的是
| 物质 | NaCl | MgCl2 | AlCl3 | SiCl4 |
| 沸点/℃ | 1465 | 1412 | 181(升华) | 57.6 |
科目:高中化学 来源: 题型:填空题
Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于 晶体,俗名叫 ;
(2)R的氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是 ;
(3)X的常见氢化物的空间构型是 ,它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是 ;
(4)Q分别与Y、Z形成的共价化合物的化学式是 和 ,Q与Y形成的分子的电子式是 ,属于 分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有下列几种物质:①Ne、②NH4Cl、③NaOH、④Cl2、⑤CO2、⑥H2O、⑦Na2O2。
(1)上述物质中,属于共价化合物的是 (填序号,下同),既存在离子键又存在极性键的是 。
(2)②号物质的电子式为 、用电子式表示⑥号物质的形成过程: 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
宇航员在升空、返回或遇到紧急情况时,必须穿上10公斤重的舱内航天服,神舟系列宇航员所穿舱内航天服是我国科学家近年来研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅(SiC)、陶瓷和碳纤维复合而成,下列相关叙述错误是( )
A.它耐高温 B.它没有固定熔点
C.它是由多种材料组成的复合材料 D.它是一种新型有机材料
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某研究所合成了一种球形分子,它的分子式为C60Si60,其结构中包含有C60和Si60结构。下列对该分子的叙述中正确的是
| A.分子中Si60被包裹在C60里面 | B.形成的晶体属于分子晶体 |
| C.其摩尔质量为2400 | D.熔点高、硬度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中错误的是
| A.当中心原子的配位数为6时,配合单元常呈八面体空间结构 |
| B.SO3为平面正三角形结构 |
| C.已知[Cu(NH3)2]2+的中心原子采用sp杂化,则它们的空间构型为直线型 |
| D.配位数为4的配合物均为正四面体结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关晶体的叙述中,错误的是
| A.离子晶体在熔化时,离子键被破坏,而分子晶体熔化时化学键不被破坏 |
| B.白磷晶体中,结构粒子之间通过共价键结合 |
| C.石英晶体是直接由硅原子和氧原子通过共价键所形成的空间网状结构的晶体 |
| D.构成分子晶体的结构粒子中不一定存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是( )。
| A.Na+(g)+Cl-(g)=NaCl(s) ΔH |
B.Na(s)+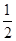 Cl2(g)=NaCl(s) ΔH1 Cl2(g)=NaCl(s) ΔH1 |
| C.Na(s)=Na(g) ΔH2 |
| D.Na(g)-e-=Na+(g) ΔH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com