
有下列几种物质:①Ne、②NH4Cl、③NaOH、④Cl2、⑤CO2、⑥H2O、⑦Na2O2。
(1)上述物质中,属于共价化合物的是 (填序号,下同),既存在离子键又存在极性键的是 。
(2)②号物质的电子式为 、用电子式表示⑥号物质的形成过程: 。
(10分)(1)⑤⑥;②③
(2)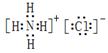 ;
;
解析试题分析:(1)全部由共价键形成的化合物是共价化合物,所以属于共价化合物的是CO2和H2O,答案选⑤⑥;一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。如果是同一种非金属形成的共价键则是非极性键,如果是不同种非金属形成的共价键,则是极性键,所以既存在离子键又存在极性键的是氯化铵和氢氧化钠,答案选②③。
(2)氯化铵是离子化合物,电子式是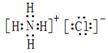 。水是由极性键形成的共价化合物,其形成过程可表示为
。水是由极性键形成的共价化合物,其形成过程可表示为 。
。
考点:考查化学键、共价化合物、电子式等
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。明确化学键的含义以及化学键与化合物关系是答题的关键,有利于培养学生的逻辑思维能力和规范答题能力。


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:单选题
下列关于化学键的说法正确的是
| A.构成单质分子的微粒一定含有共价键 |
| B.全部由非金属元素组成的化合物不一定是共价化合物 |
| C.非极性键只存在于双原子单质分子中 |
| D.不同元素组成的多原子分子里的化学键一定都是极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知N、P同属元素周期表的第ⅤA族元素,N在第二周期,P在第三周期,NH3分子呈三角锥形,N原子位于锥顶,三个H原子位于锥底,N—H键间的夹角是107.3°。
(1)PH3分子与NH3分子的构型关系是____________(填“相同”、“相似”或“不相似”)______________(填“有”或“无”)P—H键,PH3分子是______________(填“极性”或“非极性”)分子。
(2)NH3与PH3相比,热稳定性更强的是____________,原因是_____________。
(3)NH3和PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是________________。
| A.键的极性N—H比P—H强 |
| B.分子的极性NH3比PH3强 |
| C.相对分子质量PH3比NH3大 |
| D.NH3分子之间存在特殊的分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)在下列物质①NH3、②BF3、③HCl、④SO3,属于非极性分子的是(填番号)________________。
(2)试比较含氧酸的酸性强弱(填“>”、“<”或“=”): HClO3________HClO4。
(3)根据价层电子对互斥理论判断:H2O的VSEPR构型为 。
(4)沸点比较:邻羟基苯甲醛 对羟基苯甲醛(填“>”、“<”或“=”),原因是__________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)氨气易溶于水生成氨水,氨水电离生成铵根离子,铵根离子中氮原子采取________杂化,NH4+中H—N—H键角比NH3中H—N—H键角大,原因是__________________。
(2)Cu3N形成的晶体结构如图所示,N3-的配位数是________________。
(3)常温常压下,给水施加一个弱电场便可形成冰,称之为“热冰”,热冰中微粒间存在的作用力有________,其大小顺序是__________。
(4)NaF和NaCl属于同一主族的钠盐,但NaF的莫氏硬度比NaCl大,原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
在下列各组气体中,试分析判断哪种气体更易液化?
①Cl2、N2;②SiH4、CH4;③SO2、CO2;④邻二甲苯、对二甲苯;⑤甲烷、乙烷;⑥丁烷、异丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据下表中的数据,结合学过的化学知识,判断下列说法正确的是
| 物质 | NaCl | MgCl2 | AlCl3 | SiCl4 |
| 沸点/℃ | 1465 | 1412 | 181(升华) | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在下列四种有关性质的叙述中,可能属于金属晶体的是( )
| A.由分子间作用力结合而成,熔点低 |
| B.固体或熔融后易导电,熔点在1000℃左右 |
| C.由共价键结合成网状结构,熔点高 |
| D.固体不导电,但溶于水或熔融后能导电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com