
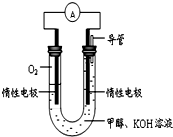
 某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.| 9.8g |
| 98g/mol |
| 9.8g |
| 98g/mol |
| 0.1mol |
| 0.5L |


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
| M |
| M |
| 选项 | X | Y | Z | M |
| A | C | CO | CO2 | O2 |
| B | Fe | FeCl2 | FeCl3 | Cl2 |
| C | AlCl3 | Al(OH)3 | NaAlO2 | NaOH |
| D | NH3 | NO | NO2 | O2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2 |
| B、NO2 |
| C、NO |
| D、N2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 食物 | 泡菜 | 葡萄 | 番茄 | 苹果 | 牛奶 | 玉米粥 |
| pH | 3.4 | 4.2 | 4.4 | 3.1 | 6.5 | 7.8 |
| A、牛奶和玉米粥均属于碱性食物 |
| B、胃酸过多的人应少食泡菜 |
| C、番茄的酸性比苹果强 |
| D、用湿润的pH试纸蘸取葡萄汁测其pH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2mol/L?S |
| B、0.4mol/L?S |
| C、0.6mol/L?S |
| D、0.8mol/L?S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用100mL的容量瓶准确量取100mL液体 |
| B、分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 |
| C、用托盘天平称量NaCl固体时,NaCl放在称量纸上,称量NaOH固体时,NaOH放在小烧杯里 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳和水反应吸收热量131.3kJ |
| B、1mol C(s)和1mol H2O(g)反应生成一氧化碳和氢气,并吸收131.3kJ的热量 |
| C、1mol C跟1mol H2O反应吸收131.3kJ的热量 |
| D、固体碳和气态水各1mol反应,放出131.3kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2- |
| B、NH4+ |
| C、CO32- |
| D、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1 |
| B、0.2 mol?L-1 |
| C、0.05 mol?L-1 |
| D、0.025 mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com