
常温常压下,O3为淡蓝色有特殊臭味的气体,工业上常用O3作为造纸、纺织等行业的漂白和脱色剂,也可用作饮用水的消毒和杀菌剂,但O3浓度超标时会因其强氧化性而对人体产生毒副作用。自然条件下打雷时空气中会有部分O2转化为O3。
实验室现提供以下装置和药品,请你完成O3的制备及性质验证实验。
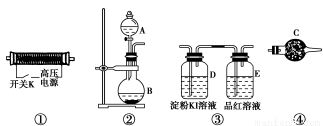
请回答以下问题:
(1)以上装置的连接顺序为______接______接________接________。
(2)A中应装入的试剂为________(写化学式);B中发生反应的化学方程式为____________________________________________________。
(3)检验整个装置的气密性的具体操作是__________________________。
(4)实验开始时,取下分液漏斗的塞子,断开电源开关K,再旋开分液漏斗的活塞,持续通入气体一段时间,其目的是________、________。然后合上电源开关K,试预测下列装置中可能观察到的现象及对应的结论。
D装置中:___________________________________________________;
E装置中:____________________________________________________。
(5)请指出该实验装置中的不妥之处并改进:_________________________。
(1)② ④ ① ③
(2)H2O2 2H2O2催化剂,2H2O+O2↑(或H2O 2Na2O2+2H2O=4NaOH+O2↑,注意对应)
(3)关闭分液漏斗的活塞,用热毛巾捂住烧瓶B,观察D、E的导管口是否有气泡冒出,松手片刻后观察导管内液面是否升高
(4)排出装置中的N2,防止生成氮氧化物干扰实验结果
导入O2进行对比实验,保证结果的准确性 无色溶液变蓝色,导管口产生气泡,试剂瓶上部有淡蓝色气体,证明O3有强氧化性 品红溶液褪色,导管口产生气泡,试剂瓶上部有淡蓝色气体,证明O3有漂白性
(5)没有尾气处理装置,应在E的导管口连接尾气处理装置
【解析】 (1)①装置的作用是利用氧气产生臭氧,②装置的作用是制备氧气,③装置的作用是检验臭氧的强氧化性和漂白性,④装置的作用是除去氧气中混有的水蒸气,故装置的连接顺序为②④①③。(2)②装置的作用是制备氧气,可以利用反应2H2O2催化剂,2H2O+O2↑或2Na2O2+2H2O=4NaOH+O2↑来制备。(4)“持续通入气体一段时间”,通入的是氧气,可以排出装置中的N2,防止生成氮氧化物干扰实验结果。KI具有还原性,若无色溶液变蓝色,则证明O3有强氧化性;若品红溶液褪色,则证明O3有漂白性。(5)臭氧“也可用作饮用水的消毒和杀菌剂,但浓度超标时会因其强氧化性而对人体产生毒副作用”,故没有反应完的臭氧应进行处理,在E的导管口连接尾气处理装置。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源:2014年高考化学苏教版一轮复习1-2-2溶液的配制及误差分析练习卷(解析版) 题型:选择题
下列叙述正确的是 ( )。
A.1 L 0.1 mol·L-1碳酸钠溶液的阴离子总数等于0.1NA
B.将1体积c mol·L-1硫酸用水稀释为5体积,得到0.2c mol·L-1硫酸
C.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol·L-1
D.将w g a%NaCl溶液蒸发掉 g水,得到4a% NaCl溶液
g水,得到4a% NaCl溶液
查看答案和解析>>
科目:高中化学 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:选择题
下列与化学反应能量变化相关的叙述正确的是 ( )。
A.应用盖斯定律,可计算某些难以直接测量的反应焓变
B.1 mol S完全燃烧放热297.3 kJ,其热化学方程式:S+O2=SO2 ΔH=-297.3 kJ·mol-1
C.1 mol H2SO4与1 mol Ba(OH)2反应生成1 mol BaSO4沉淀时放出的热量叫做中和热
D.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
查看答案和解析>>
科目:高中化学 来源:2014年高考化学考前题型专练 保温训练(一)(解析版) 题型:填空题
[物质结构与性质]碳是形成化合物种类最多的元素。
(1)CH2=CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为________(填最简整数比),写出该分子中所有碳原子的杂化方式:________________。
(2)乙醇(CH3CH2OH)和二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是_______________________________。
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为________________。
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。如图所示为碳化硅的晶胞(其中 为碳原子,
为碳原子,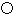 为硅原子)。每个碳原子周围与其距离最近的硅原子有________个。设晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为________(用含a、b的式子表示)。
为硅原子)。每个碳原子周围与其距离最近的硅原子有________个。设晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为________(用含a、b的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学考前题型专练 保温训练(一)(解析版) 题型:选择题
下列反应中,与乙醛生成乙酸属于同一种反应类型的是 ( )。
A.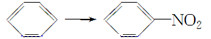
B.CH2=CHCl―→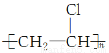
C.CH3CH2OH―→CH3CHO
D.CH3COOH―→CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第9练非金属及其化合物练习卷(解析版) 题型:选择题
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )
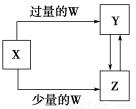
选项WX
A盐酸Na2CO3溶液
B稀HNO3Fe
CCO2Ca(OH)2溶液
DO2Na
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第8练金属及其化合物练习卷(解析版) 题型:填空题
铜单质及其化合物是应用极其广泛的物质。
(1)铜是氢后金属,不能与盐酸发生置换反应,但将单质铜置于浓氢碘酸中,会有可燃性气体及白色沉淀生成,又知氧化性:Cu2+>I2,则铜与氢碘酸反应的化学方程式为____________________________________________________。
(2)已知Cu2O能溶于醋酸溶液或盐酸中,同时得到蓝色溶液和红色固体,则Cu2O与稀硫酸反应的离子方程式为____________________________________;
Cu2O与稀硝酸反应的离子方程式为_____________________________;
只用稀硫酸来确定某红色固体是 Cu2O与Cu组成的混合物的方法:称取m g该红色固体置于足量稀硫酸中,充分反应后过滤,然后___________________。
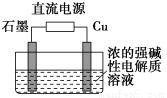
(3)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解装置如图所示,电解总反应:2Cu+H2O电解,Cu2O+H2↑,则石墨应与电源的________极相连,铜电极上的电极反应式为________;电解过程中,阴极区周围溶液pH________(填“变大”、“变小”或“不变”)。
(4)现向Cu、Cu2O、CuO组成的混合物中加入1 L 0.6 mol/L HNO3恰好使混合物溶解,同时收集到2 240 mL NO(标准状况)。若将上述混合物用足量的氢气还原,所得固体的质量为________;若混合物中含有0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗硫酸的物质的量为________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第7练电化学原理练习卷(解析版) 题型:选择题
研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水”电池在海水中放电时的有关说法正确的是( )
A.正极反应式:Ag+Cl--e-=AgCl
B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Na+不断向“水”电池的负极移动
D.AgCl是还原产物
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第4练物质结构与元素周期律练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.氘原子中的质子数和中子数之比为1∶1
B.Na2O2、Na2O中均只含离子键
C.NH4Cl属于离子化合物,不含共价键
D.18 g重水(D2O)中含有的电子数为10 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com