
| A. | Ba(OH)2•8H2O与NH4C1反应 | B. | 水解反应 | ||
| C. | 醋酸的电离 | D. | 盐酸与NaOH溶液的反应 |
分析 根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:A.BBa(OH)2•8H2O晶体与NH4Cl晶体反应是吸热反应,故A错误;
B.水解反应是吸热反应,故B错误;
C.电离是吸热过程,不是化学反应,故C错误;
D.中和反应是放热反应,故D正确.
故选D.
点评 本题考查化学反应的热量变化,难度不大,学生应注重归纳中学化学中常见的吸热或放热的反应,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.


科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{16}$O、${\;}_{8}^{18}$O为不同的核素,有不同的化学性质 | |
| B. | H2、SO2、NH3三种气体都可用浓硫酸干燥 | |
| C. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| D. | 陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.500 mol/L | B. | 1.00 mol/L | C. | 2.00 mol/L | D. | 3.00 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的电解液可以选用KOH溶液,负极是Cd,正极是NiOOH | |
| B. | 该电池放电时,负极反应为:Cd-2e-+2OH-=Cd(OH)2 | |
| C. | 该电池充电过程中,阴极附近的溶液PH降低 | |
| D. | 该电池充电时,阳极反应为:2Ni(OH)2-2e-+2OH-=2NiOOH+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
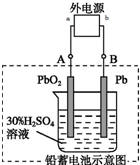 铅蓄电池是典型的可充电电池,电池的两极材料分别是Pb、PbO2,电解质H2SO4.请回答下列问题.
铅蓄电池是典型的可充电电池,电池的两极材料分别是Pb、PbO2,电解质H2SO4.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol•L-1 | B. | 2 mol•L-1 | C. | 3 mol•L-1 | D. | 4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com