
【题目】能正确表示下列反应的离子方程式是
A. NaNO2溶液中加入酸性KMnO4溶液:2MnO4﹣+5NO2﹣+6H+═2Mn2++5NO3﹣+3H2O
B. 碳酸氢铵溶液中加入足量氢氧化钡溶液:NH4++HCO3﹣+2OH﹣═CO32﹣+NH3H2O+H2O
C. Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I﹣═2Fe2++I2
D. 用惰性电极电解熔融氯化钠:2Cl﹣+2H2O═Cl2↑+H2↑+2OH﹣
【答案】A
【解析】
NaNO2有强还原性,KMnO4有强氧化性,两者在酸性溶液中发生氧化还原反应;Ba2+与CO32﹣反应生成碳酸钡沉淀,加入足量氢氧化钡溶液,反应后溶液中不可能存在CO32﹣;I-在酸性溶液中能被硝酸和Fe3+氧化;用惰性电极电解熔融氯化钠得到金属钠和氯气。
NaNO2有强还原性,KMnO4有强氧化性,两者在酸性溶液中发生氧化还原反应,反应的离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O,A正确;碳酸氢铵溶液中加入足量氢氧化钡溶液,反应后溶液中不可能存在CO32﹣,正确的离子方程式为NH4++HCO3-+2OH-+Ba2+=BaCO3↓+NH3·H2O+H2O,B错误;硝酸铁溶液中滴加足量HI溶液,溶液中的Fe3+和NO3-离子都参与反应,正确的离子方程式为:Fe3++3NO3-+12H++10I-=Fe2++5I2+3NO↑+6H2O,C错误;用惰性电极电解熔融氯化钠得到金属钠和氯气,正确的离子方程式方程式应为:2Cl-+2Na+ ![]() Cl2↑+2Na,故D错误
Cl2↑+2Na,故D错误


科目:高中化学 来源: 题型:
【题目】利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是( )
A.电解时以精铜作阳极
B.电解时阳极发生还原反应
C.精铜连接电源负极,其电极反应是Cu-2e-=Cu2+
D.电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢(H2O2)溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。H2O2能与SO2反应生成H2SO4, H2O2的分子结构如图所示。下列说法错误的是( )

A. H2O2的结构式为H—O—O—H
B. H2O2为含有极性键和非极性键的共价化合物
C. 与SO2在水溶液中反应的离子方程式为SO2+ H2O2=2H++SO42-
D. H2O2与SO2反应过程中有共价键断裂,同时有共价键和离子键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
(1)生成物能量总和__________(填"大于""小于"或"等于")反应物能量总和
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量__________(填">""<"或"=")570kJ。
(3)现有25°C、1.013×105Pa下的H2和CH4的混合气体0.5mol,完全燃烧生成一定质量的CO2气体和10.8g H2O(l),放出203kJ的热量,则1mol CH4完全燃烧生成CO2气体和H2O(l)放出的热量为__________kJ。
(4)美国阿波罗宇宙飞船上使用了一种新型电池装置,其构造如图所示,A、B两个电极均由多孔的炭块组成。该电池的正极反应式为:__________
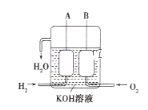
若该电池工作时增加了1mol H2O,电路中转移电子的物质的量为__________
(5)如果将上述装置中通入的氢气改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH==K2CO3+3H2O,则该电池的负极反应式为:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:
Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后获得试样溶液,设计并完成了如下的实验:

已知:3NO3-+8Al+5OH—+2H2O ![]() 3NH3↑+8A1O2—
3NH3↑+8A1O2—
根据以上的实验操作与现象,该同学得出的结论正确的是
A. 不能确定试样中是否含Al3+
B. 试样中肯定存在NH4+、Mg2+和SO42-,其他离子都不能确定
C. 要确定试样中是否有Na+存在,可做焰色反应实验,若焰色为紫色,则存在Na+
D. 沉淀2只可能是碳酸钡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①﹣⑩在表中的位置,回答下列问题:
IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
3 | ⑧ | ⑨ | ⑩ |
(1)自然界物质种类最多的元素在周期表中的位置是______
(2)⑧⑨⑩的离子半径由大到小的顺序为______(填化学用语).
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式______
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式____________
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨是碳元素的两种同素异形体,在100 kPa时,1 mol石墨转化为金刚石,要吸收1.895 kJ的热量.试判断在100 kPa压强下,下列结论正确的是( )
A.石墨比金刚石稳定
B.金刚石比石墨稳定
C.1 mol石墨比1 mol金刚石的总能量高
D.石墨转化为金刚石是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.分散质微粒直径介于1~10 nm之间的分散系称为胶体
B.Fe(OH)3胶体是纯净物
C.利用丁达尔现象可以区别溶液与胶体
D.胶体微粒不能透过滤纸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com