
| A.在中和热测定的实验中,将氢氧化钠和盐酸混合反应后的最高温度作为末温度 |
| B.纸层析法分离Fe3+和Cu2+ 的实验中,点样后的滤纸无需晾干就可将其浸入展开剂中 |
| C.将KNO3和NaCl的混合液加热并浓缩至有晶体析出时,趁热过滤可分离得NaCl晶体 |
| D.当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,借此可判断锌镀层是否反应完全 |


科目:高中化学 来源:不详 题型:单选题
| A.配制一定物质的量浓度的溶液时,定容时仰视刻度线会导致所配溶液浓度偏高 |
| B.用托盘天平称取25.20 g NaCl |
| C.用100 mL的量筒量取5.2 mL的盐酸 |
| D.用浓盐酸配制一定物质的量浓度的稀盐酸,量取浓盐酸时仰视量筒的刻度线会导致所配溶液浓度偏高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 温度 | 283K | 293K | 303K |
| 溶解度(g/100g H2O) | 2.5 | 3.9 | 5.6 |
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 | ###### |
| 步骤2:取适量滤液于试管中,滴加稀硫酸。 | _______________________ |
| 步骤3:取适量步骤1中的沉淀于试管中, ,连接带塞导气管将产生的气体导入澄清石灰水中。 | _______________________ ______________________ |
| 步骤4:取步骤1中的滤液于烧杯中,______________________________ | _______________________,说明该试剂中含有Ba(OH)2。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
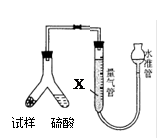
| A.可用稀盐酸代替稀硫酸 |
| B.量气管中液体为水 |
| C.反应完全后,冷却,读取量气管体积数,再减去所加硫酸的体积,即为生成的气体体积 |
| D.实验测得该试样中碳酸氢钠质量分数偏高,可能是测定气体体积时未冷却至室温 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| B.在船底镶嵌锌块和将船体与电源负极相连,二者防腐的方法都称为阴极电保护法 |
| C.不能用带玻璃塞的玻璃瓶和酸式滴定管盛取碱液,二者的原因是相同的 |
| D.12C和14C与O2和O3,两组物质的相互关系是相同的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
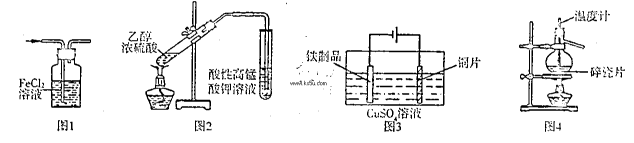
| A.用图1所示装置除去HCI气体中的少量C12 |
| B.用图2所示装置检验加热时产生的乙烯 |
| C.用图3所示装置在铁制品表面镀铜 |
| D.用图4所示装置分离溴的四氯化碳溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

 8Na2CrO4+2 Fe2O3+8CO2↑;
8Na2CrO4+2 Fe2O3+8CO2↑; 2NaAlO2+CO2↑;
2NaAlO2+CO2↑; 2CrO42-+2H+
2CrO42-+2H+查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。
Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。
| A.BaCl2溶液 | B.浓H2SO4 | C.酸性KMnO4溶液 | D.NaOH溶液 |

 Na2S2O3
Na2S2O3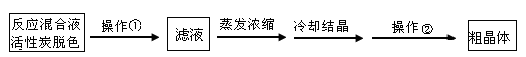
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用水润湿的pH试纸来测量溶液的pH |
| B.实验室需要480 mL 2.0 mol·L-1的氢氧化钠溶液,配制该溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、移液、洗涤、定容、摇匀的步骤进行操作 |
| C.用溴水、淀粉-KI溶液比较Br2与I2的氧化性强弱,所需玻璃仪器主要有:试管、胶头滴管 |
| D.向溶液中滴加硝酸酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com