
【题目】常温下,下列有关电解质溶液的叙述错误的是( )
A. 某H2SO4溶液中![]() =1.0×108,由水电离出的c(H+)=1×10-11 mol·L-1
=1.0×108,由水电离出的c(H+)=1×10-11 mol·L-1
B. 将0.02 mol·L-1 HCl溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合后,溶液pH约为12
C. 将0.1 mol·L-1的NaOH溶液加水稀释后,由水电离产生的c(H+)·c(OH-)保持不变
D. pH=3的H2SO4溶液,稀释105倍后,溶液的pH<7
【答案】C
【解析】A. 某H2SO4溶液中![]() =1.0×108,Kw=c(H+)c(OH-)=1×10-14,得出c(H+)=1×10-3mol/L,c(OH-)=1×10-11mol/L,由水电离出的c(H+)=c(OH-)=1×10-11 mol·L-1,故A正确;B. 将0.02 mol·L-1 HCl溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合后,溶液c(OH-)=
=1.0×108,Kw=c(H+)c(OH-)=1×10-14,得出c(H+)=1×10-3mol/L,c(OH-)=1×10-11mol/L,由水电离出的c(H+)=c(OH-)=1×10-11 mol·L-1,故A正确;B. 将0.02 mol·L-1 HCl溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合后,溶液c(OH-)=![]() =0.01mol/L,pH=12,故B正确;C. 将0.1 mol·L-1的NaOH溶液加水稀释后,碱性减弱,水的电离程度增大,由水电离产生的c(H+)·c(OH-)增大,故C错误;D. pH=3的H2SO4溶液,稀释105倍后,溶液的pH<7,故D正确。故选C。
=0.01mol/L,pH=12,故B正确;C. 将0.1 mol·L-1的NaOH溶液加水稀释后,碱性减弱,水的电离程度增大,由水电离产生的c(H+)·c(OH-)增大,故C错误;D. pH=3的H2SO4溶液,稀释105倍后,溶液的pH<7,故D正确。故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是( )
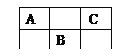
A. B为第二周期的元素
B. C为VA族元素
C. 三种元素都为金属元素
D. C所形成的气态氢化物是三种元素中最稳定的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(该反应△H>0)。某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下。
![]()
(1)吸硫装置如图所示
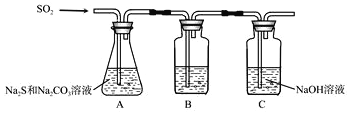
①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是______,表明SO2吸收效率低的实验现象是B中溶液_________。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是___________________。(答一条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。请完成该实验方案。(已知:室温时CaCO3饱和溶液的pH=10.2)
序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解, ______。 | 有白色沉淀生成 | 样品含NaCl |
② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,_____。 | 有白色沉淀生成,上层清液pH>10.2 | 样品含NaOH |
(3)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3(化学式量:214)固体配成溶液;
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂;
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=___mol·L-1。
(4)在(3)的实验中,某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的Na2S2O3浓度可能___________(填“不受影响”、“偏低”或“偏高”),原因是_____________。(用离子方程式表示)。(已知:IO3-+5I-+6H+= 3I2+3H2O,4I-+O2+4H+=I2+2H2O,2S2O32-+I2=S4O62-+2I-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 室温时,1.0LpH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
B. 相同质量的Na2O2和Na2S固体具有不相同的阴阳离子数和质子数
C. 5.8g正丁烷与异丁烷组成的混合气体中含有的C-H键数目为NA
D. 常温下CH3COONH4的pH=7,则0.5 mol﹒L-1的CH3COONH4溶液中,NH4+浓度为0.5 mol﹒L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、CO ![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( ) ①滴加AgNO3溶液;②过滤;③滴加Mg(NO3)2溶液;④滴加Ba(NO3)2溶液.
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( ) ①滴加AgNO3溶液;②过滤;③滴加Mg(NO3)2溶液;④滴加Ba(NO3)2溶液.
A.①②③②④
B.④②①②③
C.①②④②③
D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1) 下图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1_______K2(填 “>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________。
A. 升高温度 B. 将CH3OH(g)从体系中分离
C. 使用合适的催化剂 D. 充入He,使体系总压强增大
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,如图所示

下列说法正确的是________(填序号);
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小 ③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(3)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5时,发生以下两个分解反应:N2O5![]() N2O3+O2,N2O3
N2O3+O2,N2O3![]() N2O+O2,在1 L密闭容器中加热4 mol N2O5达到化学平衡时c(O2)为4.50 mol/L,c(N2O3)为1.62 mol/L,则在该温度下各物质的平衡浓度正确的是
N2O+O2,在1 L密闭容器中加热4 mol N2O5达到化学平衡时c(O2)为4.50 mol/L,c(N2O3)为1.62 mol/L,则在该温度下各物质的平衡浓度正确的是
A. c(N2O5)=1.44 mol/L B. c(N2O5)=0.94 mol/L
C. c(N2O)=1.40 mol/L D. c(N2O)=3.48 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下到分析错误的是
A.酸性:HClO4>H3PO4B.离子半径:F- >Mg2+
C.阴离子还原性:Cl->S2-D.H、N、O三种元素可形成离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com