
【题目】某有机物分子式为C4H8,据此推测其结构和性质不可能的是
A. 它与乙烯可能是同系物
B. 一氯代物只有一种
C. 等质量的CH4和C4H8,分别在氧气中完全燃烧,CH4的耗氧量小于C4H8
D. 分子结构中甲基的数目可能是0、1、2
【答案】C
【解析】
A.某有机物分子式为C4H8,H原子是C原子2倍,则该有机物可能是单烯烃或环丁烷,如果是烯烃,则与乙烯是同系物,故A正确;
B.如果是环丁烷,只有一种氢原子,氢原子种类决定其一氯代物种类,所以如果是环丁烷,其一氯代物只有一种,故B正确;
C.设烃的化学式为CxHy,等质量的烃耗氧量=![]() ×(x+
×(x+![]() )=
)=![]() ×(1
×(1![]() ),根据式子知,如果
),根据式子知,如果![]() 越大相同质量时耗氧量就越多,所以等质量的CH4和C4H8,分别在氧气中完全燃烧,CH4的耗氧量大于C4H8,故C错误;
越大相同质量时耗氧量就越多,所以等质量的CH4和C4H8,分别在氧气中完全燃烧,CH4的耗氧量大于C4H8,故C错误;
D.该物质可能是环丁烷(无甲基)、1-甲基环丙烷(一个甲基)、1-丁烯(一个甲基)或2-丁烯(2个甲基),所以分子结构中甲基的数目可能是0、1、2,故D正确;
故答案为C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA。下列说法正确的是
A.12g金刚石中含有的共价键数目为4NA
B.3.2gCu与足量浓硝酸反应生成的气体分子数为0.1NA
C.标准状况下,2.24LCH3OH中含有的电子数为1.8NA
D.常温常压下,4.4gN2O和CO2的混合气体中含有0.3NA个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )
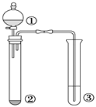
选项 | ① | ② | ③ | 实验结论 |
A | 浓盐酸 | KMnO4 | 紫色石蕊试液 | 氯气具有酸性、漂白性 |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可以生成白色沉淀 |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:N>C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电—Fenton法是用于水体里有机污染物降解的高级氧化技术,其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应,Fe2++H2O2=Fe3++OH-+OH,生成的烃基自由基(OH)能氧化降解有机污染物。下列说法正确的是( )
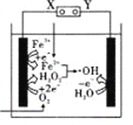
A. 电解池左边电极的电势比右边电极的电势高
B. 电解池中只有O2和Fe3+发生还原反应
C. 消耗1 molO2,电解池右边电极产生4mol OH
D. 电解池工作时,右边电极附近溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室用如图装置(夹持装置略)制取少量的NOSO4H,并检验产品纯度。已知:NOSO4H遇水水解,但溶于浓硫酸而不分解。

(1)利用装置A制取SO2,下列最适宜的试剂是_____(填下列字母编号)
A.Na2SO3固体和20%硝酸 B.Na2SO3固体和20%硫酸
C.Na2SO3固体和70%硫酸 D.Na2SO3固体和18.4mol/L硫酸
(2)装置B中浓HNO3和SO2在浓H2SO4作用下反应制得NOSO4H。
①为了控制通入SO2的速率,可以采取的措施是_______。
②该反应必须维持体系温度不低于20℃。若温度过高,产率降低的可能原因是____。
③开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因可能是______。
(3)在实验装置存在可能导致NOSO4H产量降低的缺陷是______。
(4)测定NOSO4H的纯度
准确称取1.337 g产品加入250 mL碘量瓶中,加入0.1000mol/L、60.00 mL的KMnO4标准溶液和10 mL 25%H2SO4溶液,然后摇匀。用0.2500 mol/L草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00 mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①配平:__MnO4-+___C2O42-+______=___Mn2++____+__H2O
②亚硝酰硫酸的纯度=___%(计算结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原
反应的关系”可用如图表达。

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:_____________________________,其中水为________剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:___CuO+____NH4Cl ![]() ____Cu+____CuCl2+____N2↑+____H2O。
____Cu+____CuCl2+____N2↑+____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是______(填元素名称),氧化剂是________(填化学式)。
③反应中若产生0.2mol的气体,则有________mol的电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出):
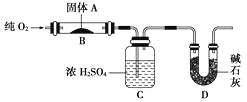
取17.1 g A放入装置中,通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题:
(1)通入过量O2的目的是______________________________________________。
(2)C装置的作用是__________________________________________;
D装置的作用是_____________________________________________。
(3)通过该实验,能否确定A中是否含有氧原子?________。
(4)若A的摩尔质量为342 g/mol,C装置增重9.99 g,D装置增重26.4 g,则A分子式为____________。
(5)写出A燃烧的化学方程式_____________________________________。
(6)A可发生水解反应,1 mol A可水解生成2 mol同分异构体,则A在催化剂作用下水解的化学方程式为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和![]() 、
、![]() 的混合气体,这些气体与
的混合气体,这些气体与![]() (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入
(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入![]() 溶液至
溶液至![]() 恰好完全沉淀,则消耗
恰好完全沉淀,则消耗![]() 溶液的体积是( )
溶液的体积是( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com