
【题目】设NA为阿伏加德罗常数的值,下列叙述错误的是
A. 1.8g18O2分子与1.8g18O3分子中含有的中子数不同
B. 7.8gNa2S和7.8g Na2O2中含有的阴离子数目均为0.1NA
C. 23.4 g NaCl晶体中含有0.1NA个如图所示的结构单元
D. 含16 g氧原子的二氧化硅晶体中含有的δ键数目为2NA
【答案】A
【解析】A、无论氧气还是臭氧,1.8g都是氧原子的质量,即1.8×10/18mol=1mol,因此中子数相同,故说法错误;B、无论是Na2S还是Na2O2,1mol中含有1mol阴离子,因此有7.8/78mol=0.1mol,故说法正确;C、23.4gNaCl合23.4/58.5mol=0.4mol,晶胞中含有4个Na+和4个Cl-,因此0.4molNaCl中含有此结构单元为0.1mol,故说法正确;D、SiO2的物质的量16/(16×2)mol=0.5mol,根据SiO2的结构,1molSi含有4molσ键(Si-O),因此含有σ键物质的量为4×0.5mol=2mol,故说法正确。


科目:高中化学 来源: 题型:
【题目】一种重要的有机化工原料有机物X,下面是以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。Y是一种功能高分子材料。

已知:(1)X为芳香烃,其相对分子质量为92
(2)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:![]()
(3)![]() (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为______________。
(2) 中官能团的名称为____________________;
中官能团的名称为____________________;
(3)反应③的反应类型是___________;已知A为一氯代物,则E的结构简式是____________;
(4)反应④的化学方程式为_______________________;
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有________种:①含有苯环;②既不能发生水解反应,也不能发生银镜反应;③1mol该有机物能与2molNaHCO3完全反应。
(6)请写出以A为原料制备![]() 的合成路线流程图 (无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图 (无机试剂任用)。合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭.导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca =CaCl2+Li2SO4+Pb。

下列有关说法正确的是
A .正极反应式:Ca+2Cl- - 2e- =CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针不偏转
D.每转移0.1mol电子,理论上生成20.7g Pb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,美国正在研究用锌电池取代目前广泛使用的蓄电池,它具有容量大、污染小的特点,其电池反应为:2Zn+O2=2ZnO ,其原料为锌、空气和电解质溶液,则下列叙述正确的是
A.锌为正极,空气在负极反应
B.负极还原反应,正极氧化反应
C.负极的电极反应为:Zn-2e-+2OH-=ZnO+H2O
D.电池工作时溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的学生从网上查得如下信息:①钠能在CO2中燃烧。②常温下CO能与PdCl2溶液反应得到黑色的Pd。经过分析讨论,他们认为钠在CO2中燃烧时,还原产物可能是碳、也可能是CO,氧化产物可能是Na2CO3。为验证上述推断,他们设计如下方案进行实验,请回答下列问题。
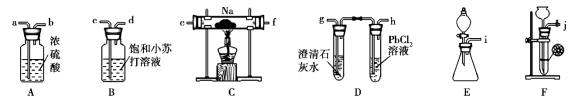
(1)他们欲用上述仪器组装一套装置:用石灰石与盐酸反应制取CO2(能随意控制反应的进行)来证明钠能在CO2中燃烧并检验气态还原产物,所用仪器接口连接顺序为 ,制取CO2反应的离子方程式为 。
(2)装置连接好后,首先要进行的实验操作是 ,点燃酒精灯前,应进行的操作是 ,等装置 (填写装置字母代号及现象)时,再点燃酒精灯,这步操作的目的是 。
(3)若装置D的PdCl2溶液中有黑色沉淀,C中有残留固体(只有一种物质),则C中反应的化学方程式为 ;若装置D的PdCl2溶液中无黑色沉淀,C中有残留固体(有两种物质),则C中反应的化学方程式为 。
(4)后来有一位同学提出,钠的氧化产物也可能是Na2O,因此要最终确定钠的氧化产物是何种物质,还需要检验C中残留的固体是否含有Na2O,为此,他认为应较长时间通入CO2以确保钠反应完,然后按照如下方案进行实验,可确定残留固体中是否含有Na2O,他的实验方案是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对元素周期表说法不正确的是( )
A. 在第ⅥB和第ⅦB族附近可以找到耐高温金属材料
B. 第ⅣA族所有含氧酸的钠盐,溶于水均呈碱性
C. 如果已知元素的最外层电子数为2,由此不能判断该元素在周期表中的位置
D. 目前已知发现的第ⅣA族元素为5种,所以该族元素共有5种单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用比表示阿伏加德罗常数的数值,下列说法正确的是( )
A.ILlmol/L的氯化铁溶液中,若C1-的数目为3 NA,则Fe3+的数目为NA
B.1 molN2和3 molH2在一定条件下充分反应,转移电子数目为6NA
C.常温下,1L0.lmol/L的Na2S溶液中阴离子数目大于0.1 NA
D.0.1 mol Cl2通入水中,转移电子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最高的金属元素,其单质及化合物在生产生活中有广泛的应用。
(1)普通水泥的主要成分之一是铝酸三钙(3CaO·Al2O3),3CaO·Al2O3中Al的化合价为__________;
(2)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉(Al2O3)与炭粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式__________;
(3)现将一定量的铝粉和镁粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐渐加入4mol·L-1的NaOH溶液,加入NaOH溶液的体积(mL)与产生沉淀的质量的关系如图所示。
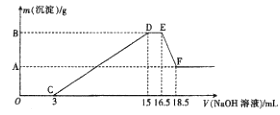
①D→E过程中反应的离子方程式为____________________;
②A点对应纵坐标的数值是__________,原稀硝酸的浓度是__________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,在CuZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1 平衡常数K1 反应Ⅰ
CH3OH(g)+H2O(g)△H1 平衡常数K1 反应Ⅰ
CO2(g)+H2(g)![]() CO(g)+H2O(g)△H2 =+41.2kJmol-8平衡常数K2 反应Ⅱ
CO(g)+H2O(g)△H2 =+41.2kJmol-8平衡常数K2 反应Ⅱ
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性;转化的CO2中生成甲醇的百分比
(1)合成的甲醇可用于燃料电池的燃料,若电解质为稀烧碱溶液时甲醇燃料电池的正极反应式为________;研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在______极,该电极反应式是________________________________。
(2)从表中实验数据可以分析出,提高CO2转化成CH3OH的选择性的方法有______________。
(3)反应CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K3=____________(用K1和K2表示)。
CH3OH(g)的平衡常数K3=____________(用K1和K2表示)。
(4)在恒压密闭容器中,由CO2和H2进行反应I合成甲醇,在其它条件不变的情况下,探究温度对化学平衡的影响,实验结果如图。

①△H1_________0(填“>”、“<”或“=”)
②有利于提高CO2平衡转化率的措施有___________(填标号)。
A.降低反应温度
B.投料比不变,增加反应物的浓度
C
D.混合气体中掺入一定量惰性气体(不参与反应)
(5)在T1温度时,将1.00molCO2和3.00molH2充入体积为1.00L的恒容密闭容器中,容器起始压强为P0,仅进行反应I。
①充分反应达到平衡后,若CO2转化率为a,则容器的压强与起始压强之比为________(用a表示)。
②若经过3h反应达到平衡,平衡后,混合气体物质的量为3.00mol,则该过程中H2的平均反应速率为____________(保留三位有效数字);该温度下反应的化学平衡常数K为____________(保留三位有效数字);平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数。写出上述反应压力平衡常数KP为____________(用P0表示,并化简)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com