
【题目】下列叙述正确的是
A. 硫酸钡难溶于水,故硫酸钡为弱电解质
B. 硝酸钾溶液能导电,故硝酸钾溶液为电解质
C. 二氧化碳溶于水能部分电离,故二氧化碳为弱电解质
D. 石墨虽能导电,但既不是电解质,也不是非电解质
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】右图是周期表中短周期的一部分,A、B、C三种元素原子核外的电子数之和等于B原子的质量数。B原子核内的质子数和中子数相等。下列叙述不正确的是( )
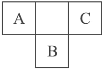
A. 三种元素的原子半径的大小顺序是B>C>A
B. A元素最高价氧化物对应的水化物具有强氧化性
C. B元素的氧化物、氢化物的水溶液都呈酸性
D. C元素是非金属性最强的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下所示:(已知:硫不溶于水,微溶于酒精,易溶于二硫化碳、四氯化碳和苯。)

(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:____________。
(2)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是_____________________。
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为_________________。向“滤液M”中加入(或通入)____(填字母),可得到另一种可循环利用的物质。 a.铁 b.氯气 c.高锰酸钾
(4)“保温除铁”过程中,加入CuO的目的是__________________;“蒸发浓缩、冷却结晶”过程中,加入HNO3调节溶液的pH,其理由是___________。
(5)洗涤硝酸铜晶体的洗涤剂可以使用下列物质中的______________。
a.酒精 b.热水 c.饱和硝酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烷烃和一气态单烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48L,通入足量的溴水,溴水的质量增加2.8g,此2种烃是( )
A.甲烷和丙烯
B.甲烷和2﹣丁烯
C.甲烷和2﹣甲基丙烯
D.乙烯和1﹣丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。

回答下列问题:
(1)元素b在元素周期表中的位置是________。
(2)元素e的负一价离子的结构示意图为________,与元素g的简单离子,二者的离子半径大小顺序为________。(用离子符号表示)
(3)元素i的气态氢化物比元素e的气态氢化物________(填“稳定”或“不稳定”)。
(4)元素i的单质溶于元素f的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的电子式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼(Mo)是一种重要的过渡金属元素,常见化合价为+6、+5、+4,金属钼广泛用于冶金、机械制造、电子、照明及一些高科技领域。钼酸钠(Na2MoO4)是一种无公害型冷却水系统的金属缓蚀剂,也可用于制造生物碱、油墨、化肥、钼红颜料等。如图是化工生产中制备金属钼和钼酸钠的主要流程图,已知钼精矿的主要成分为MoS2,钼酸难溶于水。
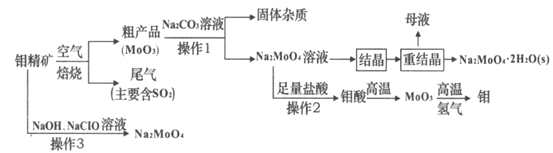
(1)MoS2焙烧时反应的化学方程式为________;产生的尾气对环境的主要危害是_______。
(2)操作1中,粗产品中的MoO3与Na2CO3溶液充分反应后,生成Na2MoO4和另外一种物质,该物质的电子式为_____。粗产品经过充分碱浸后所得的碱浸液中部分离子的浓度:c(MoO42-)=0.40mol·L-1,c(SO42-)=0.05mol·L-1。结晶前应先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当BaMoO4,开始沉淀时,SO42-的去除率为___。已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8
(3)该流程中操作2为过滤,如果在实验室模拟该操作时,发现滤液中有少量浑浊,从实验操作的角度分析,可能的原因是_______________________________。
(4)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因______________________________________。
(5)工业上由MoO3制备Mo粉也常用铝热反应,写出该反应的方程式_______________。
(6)操作3在碱性条件下,将钼精矿加入到足量的NaC1O溶液中,也可以制备钼酸钠。该反应的离子方程式为___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com