
ЁОЬтФПЁПгУNAБэЪОАЂЗќМгЕТТоГЃЪ§ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
ЂйдкБъзМзДПіЯТЃЌNAИіSO3ЗжзгЫљеМЕФЬхЛ§ЮЊ22.4L
ЂкS2КЭS8ЕФЛьКЯЮяЙВ6.4gЃЌЦфжаЫљКЌСђдзгЪ§вЛЖЈЮЊ0.2NA
ЂлБъзМзДзЃЯТЃЌ22.4LNOКЭ11.2LO2ЛьКЯКѓЦјЬхЕФЗжзгзмЪ§ЮЊ1.5 NA
Ђм1molAlCl3Шмгк1LЕФЫЎжаЃЌЫљЕУШмвККЌга1NAAl3+
ЂндкБъзМзДПіЯТЃЌ22.4LCl2гызуСПЕФЧтбѕЛЏМиШмвКЗДгІзЊвЦЕФЕчзгЪ§ЮЊNA
Ђо100mL1mol/LFe2(SO4)3ШмвКжаЃЌFe3+КЭSO42-РызгЪ§ЕФзмКЭЪЧ0.5NA
AЃЎЂкЂн BЃЎЂйЂкЂмЂо CЃЎЂлЂнЂо DЃЎЂйЂкЂнЂо
ЁОД№АИЁПA
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКЂйдкБъзМзДПіЯТSO3ВЛЪЧЦјЬЌЃЌВЛФмРћгУЦјЬхФІЖћЬхЛ§МЦЫуЬхЛ§ЃЌДэЮѓЃЛЂкS2КЭS8ЕФЛьКЯЮяЙВ6.4gЃЌЦфжаЫљКЌСђдзгЪ§вЛЖЈЮЊ![]() ЃН0.2NAЃЌе§ШЗЃЛЂлБъзМзДзЃЯТЃЌ22.4LNOКЭ11.2LO2ЛьКЯКѓЧЁКУЩњГЩ22.4LNO2ЃЌЕЋNO2ДцдкЦНКт2NO2
ЃН0.2NAЃЌе§ШЗЃЛЂлБъзМзДзЃЯТЃЌ22.4LNOКЭ11.2LO2ЛьКЯКѓЧЁКУЩњГЩ22.4LNO2ЃЌЕЋNO2ДцдкЦНКт2NO2![]() N2O4ЃЌЪЧЦјЬхЕФЗжзгзмЪ§аЁгкNAЃЌДэЮѓЃЛЂм1molAlCl3Шмгк1LЕФЫЎжаЃЌгЩгкТСРызгЫЎНтЃЌвђДЫЫљЕУШмвККЌгаЕФAl3+аЁгк1molЃЌДэЮѓЃЛЂндкБъзМзДПіЯТЃЌ22.4LCl2гызуСПЕФЧтбѕЛЏМиШмвКЗДгІзЊвЦЕФЕчзгЪ§ЮЊNAЃЌе§ШЗЃЛЂо100mL1mol/LFe2(SO4)3ШмвКжаЬњРызгЫЎНтЃЌзЂШыFe3+КЭSO42-РызгЪ§ЕФзмКЭаЁгк0.5NAЃЌДэЮѓЃЌД№АИбЁAЁЃ
N2O4ЃЌЪЧЦјЬхЕФЗжзгзмЪ§аЁгкNAЃЌДэЮѓЃЛЂм1molAlCl3Шмгк1LЕФЫЎжаЃЌгЩгкТСРызгЫЎНтЃЌвђДЫЫљЕУШмвККЌгаЕФAl3+аЁгк1molЃЌДэЮѓЃЛЂндкБъзМзДПіЯТЃЌ22.4LCl2гызуСПЕФЧтбѕЛЏМиШмвКЗДгІзЊвЦЕФЕчзгЪ§ЮЊNAЃЌе§ШЗЃЛЂо100mL1mol/LFe2(SO4)3ШмвКжаЬњРызгЫЎНтЃЌзЂШыFe3+КЭSO42-РызгЪ§ЕФзмКЭаЁгк0.5NAЃЌДэЮѓЃЌД№АИбЁAЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪпВЫЁЂЫЎЙћжаИЛКЌЯЫЮЌЫиЃЌЯЫЮЌЫиБЛЪГШыШЫЬхКѓЕФзїгУЪЧ
A. ЮЊШЫЬхФкЕФЛЏбЇЗДгІЬсЙЉдСЯ
B. ЮЊЮЌГжШЫЬхЩњУќЛюЖЏЬсЙЉФмСП
C. МгЧПЮИГІШфЖЏЃЌОпгаЭЈБуЙІФм
D. ШЫЬхжаУЛгаЫЎНтЯЫЮЌЫиЕФУИЃЌЫљвдЯЫЮЌЫидкШЫЬхжаУЛгаШЮКЮзїгУ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПКтСПвЛИіЙњМвЪЏгЭЛЏЙЄЗЂеЙЫЎЦНЕФБъжОЪЧ
AЃЎЪЏгЭВњСП BЃЎввЯЉВњСП CЃЎЬьШЛЦјВњСП DЃЎЦћгЭВњСП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПWЁЂXЁЂYЁЂZЫФжжЖЬжмЦкдЊЫиЕФдзгађЪ§ЃКXЃОWЃОZЃОYЃЎWдзгЕФзюЭтВуУЛгаpЕчзгЃЌXдзгКЫЭтsЕчзгЪ§гыpЕчзгЪ§жЎБШЮЊ1ЃК1ЃЌYдзгзюЭтВуsЕчзгЪ§жЎБШЮЊ1ЃК1ЃЌZдзгЕФpЕчзгЪ§БШYдзгЕФЖр2ИіЃЎ
ЃЈ1ЃЉЫФжждЊЫидзгАыОЖДгДѓЕНаЁЕФЫГађЮЊ ЃЈгУдЊЫиЗћКХБэЪОЃЉЃЎ
ЃЈ2ЃЉЧыгУЁАЃОЁБЛђЁАЃМЁБЬюПеЃК
ЕквЛЕчРыФм | ЕчИКад | ЧтЛЏЮяЗаЕу | зюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФМюад |
WЁЁЁЁЁЁЁЁЁЁЁЁX | ZЁЁЁЁЁЁЁЁЁЁЁЁY | YЁЁЁЁЁЁЁЁЁЁЁЁZ | WЁЁЁЁЁЁЁЁЁЁЁЁX |
ЃЈ3ЃЉаДГіXдЊЫиЕФЕЅжЪгыZЁЂYЫљаЮГЩЕФЛЏКЯЮяЗДгІЕФЛЏбЇЗНГЬЪНЃЌВЂБъГіЕчзгзЊвЦЕФЗНЯђКЭЪ§ФПЃК ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛИідЕчГиЕФзмЗДгІЕФРызгЗНГЬЪНЪЧZnЃЋCu2ЃЋ===Zn2ЃЋЃЋCuЃЌИУдЕчГиЕФКЯРэзщГЩ
е§МЋ | ИКМЋ | ЕчНтжЪШмвК | |
A | Zn | Cu | CuCl2 |
B | Cu | Zn | H2SO4 |
C | Cu | Zn | CuSO4 |
D | Zn | Fe | CuCl2 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІУЛгаЩцМАдЕчГиЕФЪЧЃЈ ЃЉ
AЃЎЩњЬњЭЖШыЯЁбЮЫсжа BЃЎЭЦЌгывјЦЌгУЕМЯпСЌНгКѓЃЌЭЌЪБВхШыFeCl3ШмвКжа
CЃЎДПаПЭЖШыСђЫсЭШмвКжа DЃЎКЌЭЕФТСЦЌЭЖШыХЈСђЫсжа
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГгаЛњЮядкПеЦјжаЭъШЋШМЩежЛЩњГЩЖўбѕЛЏЬМКЭЫЎЃЌдђДЫгаЛњЮя
A. вЛЖЈКЌгабѕдЊЫи
B. вЛЖЈВЛКЌгабѕдЊЫи
C. вЛЖЈКЌгаЬМЁЂЧтЁЂбѕШ§жждЊЫи
D. вЛЖЈКЌгаЬМЁЂЧтСНжждЊЫиЃЌВЛФмШЗЖЈЪЧЗёКЌгабѕдЊЫи
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉгУO2НЋHC1зЊЛЏЮЊCl2ЃЌПЩЬсИпаЇвцЃЌМѕЩйЮлШОЃЌДЋЭГЩЯИУзЊЛЏЭЈЙ§ШчЯТЭМЫљЪОЕФДпЛЏМСбЛЗЪЕЯжЃЌ

ЦфжаЃЌЗДгІЂйЮЊЃК2HCl(g)+CuO(s) ![]() H2O(g)+CuCl2ЃЈsЃЉ ЁїH1ЃЌЗДгІЂкЩњГЩ1 mol Cl2 (g)ЕФЗДгІШШЮЊЁїH2ЃЌдђзмЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ____________________________ЁЃЃЈЗДгІШШгУЁїH1КЭЁїH2БэЪОЃЉЁЃ
H2O(g)+CuCl2ЃЈsЃЉ ЁїH1ЃЌЗДгІЂкЩњГЩ1 mol Cl2 (g)ЕФЗДгІШШЮЊЁїH2ЃЌдђзмЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ____________________________ЁЃЃЈЗДгІШШгУЁїH1КЭЁїH2БэЪОЃЉЁЃ
ЃЈ2ЃЉвЛЖЈЬѕМўЯТВтЕУЩЯЪіЗДгІЙ§ГЬжаc(Cl2)ЕФЪ§ОнШчЯТЃК
tЃЈminЃЉ | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
c(Cl2)/10-3(mol/L) | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
МЦЫу2.0ЁЋ6.0minФквдHClЕФЮяжЪЕФСПХЈЖШБфЛЏБэЪОЕФЗДгІЫйТЪ _________ЁЃ
ЃЈ3ЃЉГЃЮТЯТЃЌНЋГ§ШЅБэУцбѕЛЏФЄЕФAlЁЂCuЦЌВхШыХЈHNO3жазщГЩдЕчГиЃЈЭМ1ЃЉЃЌВтЕУдЕчГиЕФЕчСїЧПЖШЃЈIЃЉЫцЪБМфЃЈtЃЉЕФБфЛЏШчЭМ2ЫљЪОЃЌЗДгІЙ§ГЬжагаКьзиЩЋЦјЬхВњЩњЁЃ

0ЁЋtlЪБЃЌдЕчГиЕФИКМЋЪЧAlЦЌЃЌДЫЪБЃЌе§МЋЕФЕчМЋЗДгІЪНЪЧ______________ЃЌШмвКжаЕФH+Яђ______МЋвЦЖЏЃЌtlЪБЃЌдЕчГижаЕчзгСїЖЏЗНЯђЗЂЩњИФБфЃЌЦфдвђЪЧ_____________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПаЁУїАДгвЭМзАКУСЫЪЕбщзАжУ(СННКЭЗЕЮЙмжаЕФЙ§бѕЛЏЧтШмвКЬхЛ§ЯрЕШЃЌХЈЖШЗжБ№ЮЊ5%КЭ10%)ЃЌЪЕбщЪБЃЌЭЌЪБЭъШЋФѓБтСНЕЮЙмЕФНКЭЗЃЌВЂЙлВьЪЕбщЯжЯѓЁЃ
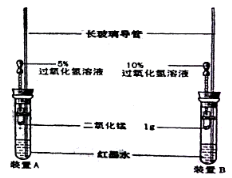
ЃЈ1ЃЉаЁУїЕФЪЕбщФПЕФЪЧЃК__________________________ЁЃ
ЃЈ2ЃЉзАжУжаГЄВЃСЇЕМЙмЕФзїгУЪЧЃК____________________ЃЛКьФЋЫЎЕФзїгУЪЧ_________________ЁЃ
ЃЈ3ЃЉФуЙРМЦСНИљВЃСЇЕМЙмжаЕФЪЕбщЯжЯѓЪЧ____________________ЃЛРэгЩЪЧ___________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com